USO DE BIOSÓLIDOS COMO REACTIVO ESPUMANTE EN PROCESOS DE FLOTACIÓN: CARACTERIZACIÓN FÍSICA Y QUÍMICA
USO DE BIOSÓLIDOS COMO REACTIVO ESPUMANTE EN PROCESOS DE FLOTACIÓN: CARACTERIZACIÓN FÍSICA Y QUÍMICA
USE OF BIOSOLIDS AS FROTH REAGENT IN FLOTATION PROCESS: CHEMICAL AND PHYSICAL CHARACTERIZATION
LORENZO REYES-BOZO
Departamento de Ingeniería Química y Bioprocesos, Pontificia Universidad Católica de Chile, Santiago, Chile, lcreyes@ing.puc.cl Escuela de Industrias, Facultad de Ingeniería, Universidad Andres Bello, Santiago, Chile, lreyes@unab.cl
RONALDO HERRERA-URBINA
Departamento de Ingeniería Química y Metalurgia, Universidad de Sonora, Hermosillo, Sonora, México, rherrera@guaymas.uson.mx
ALEX GODOY-FAÚNDEZ
Facultad de Ecología y Recursos Naturales, Universidad Andres Bello, Santiago, Chile, agodoy@unab.cl
CÉSAR SÁEZ-NAVARRETE
Departamento de Ingeniería Química y Bioprocesos, Pontificia Universidad Católica de Chile, Santiago, Chile, csaez@ing.puc.cl
MIGUEL HERRERA
Centro de Investigación Minera y Metalúrgica, CIMM, Santiago, Chile, mherrera@cimm.cl
ROSANNA GINOCCHIO
Centro de Investigación Minera y Metalúrgica, CIMM, Santiago, Chile, rginocc@cimm.cl
Recibido para revisar marzo 15 de 2011, aceptado abril 14 de 2011, versión final abril 26 de 2011
RESUMEN: La flotación espumosa usa diversos reactivos, orgánicos e inorgánicos, para aumentar el rendimiento y selectividad del proceso. La flotación utiliza sustancias tensoactivas que se adsorben en la interfase aire/agua. Como potenciales sustitutos de los espumantes usados actualmente, se consideran los residuos orgánicos de origen animal, como los biosólidos. Este estudio, evalúa el uso de biosólidos y ácidos húmicos como agentes espumantes para flotación espumosa, cuantificándose su capacidad tensoactiva y para formar y estabilizar espumas. Biosólidos son capaces de cambiar la tensión superficial de una solución, crear y estabilizar espumas. Dosis menores a 4 g L-1 muestran un afecto tensoactivo mayor comparado con reactivos espumantes, tipo MIBC. Para un uso efectivo de biosólidos, se requiere realizar una etapa de preacondicionamiento, que permita separar la fracción soluble y coloidal que tiene la capacidad tensoactiva. El uso de biosólidos a gran escala necesita investigación adicional para escalar los resultados obtenidos en laboratorio.
PALABRAS CLAVE: espuma, lodos sanitarios, materia orgánica, concentrado.
ABSTRACT: Froth flotation uses various organic and inorganic reagents to increase performance and selectivity of the flotation process. Froth flotation takes place mediated by tensioactive substances that are adsorbed on the air/water interface. Potential substitutes for the currently used frothers, organic wastes of animal origin, like biosolids are found. This study was to evaluate biosolids and humic acids as foaming agents in froth flotation by quantification of their tensioactive capabilities, foam-forming potential and foam stability. Biosolids was able to change the surface tension of a solution, creating and stabilizing foams. Dosages under 4 g L-1 of flotation reagents showed a better tensioactive effect using biosolids instead of conventional flotation reagents, type MIBC. For an effective use of these substances as frothers, it is recommended to consider a preconditioning stage. That stage will permit separating soluble and colloidal fractions that show a tensioactive effect. Further research will be needed in order to scale-up current laboratory assays to operational mining scales.
KEYWORDS: foam; sewage sludge; organic matter; concentrates
1. INTRODUCCIÓN
La principal tecnología de alta escala para obtener concentrados de cobre a partir de minerales sulfurados, es la flotación espumosa. La flotación espumosa emplea diversos reactivos químicos, clasificados como reactivos colectores, depresantes, activadores, modificadores y espumantes, útiles para incrementar el rendimiento y la selectividad del proceso. Durante la flotación, las especies mineralógicas de interés con un tamaño de partícula del orden de micrómetros, son recuperadas desde una mezcla de materiales a partir de una suspensión acuosa con la ayuda de aireación y mezcla controlada. Posterior a la etapa de colección, asociada principalmente a fenómenos de superficie inducidos por los reactivos colectores, se produce la flotación espumosa mediada por sustancias tensoactivas que se adsorben en la interfase aire/agua. Estas sustancias facilitan la captura de pequeñas partículas del mineral de interés por las burbujas generadas en las unidades del proceso. En la flotación espumosa, el uso de reactivos que puedan actuar en la interfase sólido/líquido y líquido/gas, son esenciales para poder realizar una exitosa separación de las especies mineralógicas de interés desde la pulpa. Sin estos reactivos, que controlan la mojabilidad de las superficies sólidas, la electroquímica de la solución, la dispersión y agregación de las partículas sólidas, y la generación y estabilidad de la espuma, sería imposible la recuperación de las partículas que contienen las especies mineralógicas de interés [1].
Los reactivos colectores y espumantes que se emplean actualmente en la minería del cobre presentan diversas características de toxicidad y de persistencia. Por ejemplo, el etil xantato de sodio presenta un alto nivel de peligrosidad en seres humanos y un nivel medio de toxicidad para los seres vivos [2]. Otros reactivos, como son el ditiofosfato-1404, metilisobutilcarbinol (MIBC) y Dawfroth 250, entre otros, están considerados como sustancias químicas tóxicas, mostrando diversos riesgos potenciales para la salud de las personas y el medio ambiente [3]. De esta forma, es de alta relevancia considerar la incorporación de nuevos reactivos de flotación que permitan reducir los costos operacionales y los potenciales impactos ambientales de las operaciones mineras.
Dentro de las alternativas interesantes de evaluar como potenciales sustitutos de los espumantes usados actualmente están los residuos orgánicos de origen animal, como los lodos (biosólidos, BS) producidos en las plantas de tratamiento de aguas servidas domiciliarias que utilizan sistemas biológicos para la remoción de la materia orgánica fácilmente biodegradable mediante tecnologías convencionales como Lodos Activados, Lagunas y Digestores Anaeróbicos. Específicamente, las aguas servidas domiciliarias y en consecuencia los biosólidos generados en sus procesos de tratamiento, contienen biopolímeros solubles como proteínas, lípidos, polisacáridos, sustancias húmicas y ácidos nucleicos [4], que podrían actuar como sustancias tensoactivas que resultarían en la formación de espuma [5]. Aunque esta característica no ha sido estudiada en profundidad, conferiría a los biosólidos un uso potencial de muy alto impactos social y ambiental como reactivo espumante en procesos de flotación de minerales sulfurados de cobre.
Se ha reportado que las sustancias poliméricas extracelulares (SPE) son el principal componente orgánico de los lodos activados, comprendiendo compuestos orgánicos e inorgánicos de distinto peso molecular. Las proteínas y azúcares representan los principales constituyentes orgánicos de las SPE [6,7]. Las proteínas podrían influir en las propiedades superficiales de los BS, pudiendo modificar la tensión superficial de soluciones acuosas [8,9].
El objetivo de este trabajo fue evaluar la factibilidad de uso de BS y de las sustancias húmicas (ácidos húmicos y ácidos fúlvicos) como reactivos espumantes en procesos de flotación espumosa de minerales sulfurados de cobre a escala de laboratorio, cuantificando su capacidad tensoactiva y la generación y estabilización de espumas.
2. MATERIALES Y MÉTODOS
2.1 Obtención, análisis físicos y químicos de biosólidos
Los biosólidos (BS) usados en el presente estudio fueron obtenidos desde las plantas de tratamiento de aguas servidas El Trebal (Aguas Andinas S.A., Santiago, Chile) y Tongoy (Aguas del Valle, Región de Coquimbo, Chile). En ambos casos, la remoción biológica de la carga orgánica se realizó empleando la tecnología de lodos activados. Las muestras fueron previamente molidas empleando morteros, homogenizadas y tamizadas a una fracción menor a 2 mm. Adicionalmente, como reactivo representativo de las sustancias húmicas presentes en el BS, se utilizó una sal comercial de ácidos húmicos (AHc, Sigma-AldrichTM).
Las muestras de BS fueron analizadas física y químicamente en laboratorios acreditados (Análisis Ambientales, ANAM Ltda. y Laboratorio de Suelos y Plantas del Centro de Investigación Minera y Metalúrgica, CIMM). Se determinaron los siguientes parámetros: pH en solución (1:2,5 p/v), conductividad eléctrica (CE) por conductivimetría, carbono orgánico total por el método de Walkey y Black, nitrógeno total por el método de Kjeldahl y el contenido total de metales por digestión y extracción ácida (HNO3–HF–H2O2) en un horno microondas Milestone 1200 (U.S. EPA, método 3052) seguida por cuantificación en un equipo de plasma asociado a espectrometría de masas (ICP-MS, Perkin Elmer ELAN 6100) con automuestrador AS90 (U.S EPA, método 200.8).
2.2 Espectroscopia Infrarroja con Transformada de Fourier (FTIR)
Las muestras de biosólidos y las sales de ácidos húmicos empleadas fueron secadas a 50 ºC por 48 horas. Las pastillas para análisis se prepararon mezclando 1 mg de muestra a analizar con 100 mg de KBr seco. Tanto las muestras de BS como las sales de ácidos húmicos empleadas fueron homogenizadas en un mortero de ágata. Las pastillas se formaron en un contenedor, aplicando una presión de 6000 kg cm-2, durante 30 segundos, para lograr un espesor comprendido entre 0,1-1 mm. Las muestras fueron analizadas en triplicado en un equipo Bruker Vector 22, en el rango de 4000 a 250 cm-1, utilizando 16 scans cada 10 segundos.
Los espectros fueron analizados de acuerdo a lo reportado en la literatura [10-13]. Se ha reportado que la principal absorbancia en los espectros IR de los BS (mínima transmitancia en las gráficas), se encuentran en la región 1030-1080 cm-1, la cual es asignada a la tensión C-O de polisacáridos, Si-O de impurezas de silicatos y arcillas minerales formando complejos con las sustancias húmicas [11,12]. También se ha reportado que los espectros IR de residuos que contienen BS difieren de otros desechos orgánicos por su intensidad y amplitud, mostrando bandas de absorción asimétricas con un máximo en 1034 cm-1 [13].
2.3 Medición de la tensión superficial
Las mediciones de tensión superficial fueron realizadas en un tensiómetro Krüss K8, según el método de Du Nouy a temperatura ambiente de 18 ºC. Se prepararon soluciones de BS, AHc y metilisobutilcarbinol (MIBC) con agua desionizada ultrafiltrada, con una conductividad eléctrica de 5,55·10-2 mS cm-1, y una tensión superficial de 72,1 mN m-1. Las concentraciones ensayadas para BS fueron: 0; 1; 10; 25; 50 y 100 g L-1, para AHc: 0; 0,1; 1; 5; 10 y 25 g L-1 y para MIBC: 0; 0,1; 0,5; 1; 2,5; 5 y 7,5 g L-1. Las concentraciones ensayadas expresadas en gramos de ácidos húmicos por litro son equivalentes para BS y AHc. Posteriormente, se realizó un ajuste de pH para cada una de las soluciones de BS, AHc y MIBC a pH 7 y 10, agregando pequeñas alícuotas de solución de NaOH y HCl 0,1M. Para las concentraciones ensayadas, las muestras se midieron al menos 4 veces.
2.4 Medición del poder espumante y estabilidad de la espuma
Los test de espumación fueron realizados usando 20 mL de solución, según las siguientes concentraciones de espumantes MIBC, AHc y BS: 0.1, 1, 5 y 10 g L-1. Las muestras se prepararon con agua bidestilada, ajustando el pH inicial de las soluciones con pequeñas alícuotas de solución de NaOH y HCl 0,1M hasta alcanzar valores de pH 10 y 7, agitando y homogenizando las muestras por 10 minutos, a 200 rpm. Todos los ensayos se realizaron en duplicado, a temperatura ambiente (18 ± 2 ºC).
El método de Bikerman fue usado para determinar la generación dinámica de espuma (e) y la estabilidad estática t [14-16]. En el método dinámico, la espuma se produce de manera continua por inyección de aire atmosférico. Para ello, se usó un compresor de aire seco a 4 flujos de aire: 1, 2, 3 y 4 L min-1. El aire se hizo pasar a través del líquido en una columna y, para cada caudal de aire inyectado, se determinó la altura de la espuma en estado estacionario. La altura medida corresponde a la distancia entre la interfase líquido-espuma y la máxima altura de la espuma en estado estacionario, alcanzada después de aproximadamente 3 minutos de operación. Para contener la espuma producida se usó una columna de vidrio de sección recta, de 60 cm de altura y 3,4 cm de diámetro interno. Considerando la altura en estado estacionario y la geometría de la columna, se obtuvo el volumen de espuma producido para cada flujo de aire empleado y para cada concentración conocida de espumante (MIBC, AHc y BS). La incerteza en la medida de la altura de la espuma en estado estacionario fue de ± 1 cm dependiendo del tipo y concentración de espumante y del flujo de aire empleado [15].
Para ciertos rangos de flujo de aire, la generación de espuma tiene una dependencia lineal con el flujo de aire [16]. La pendiente de la curva, e, que representa el tiempo de vida media de una burbuja de gas en el sistema, es expresada en unidades de tiempo. El tiempo de vida media de una burbuja es una medida de la estabilidad dinámica de la espuma, siendo independiente del flujo de gas, geometría de la columna, volumen de líquido y porosidad del difusor usado.
En el sistema experimental usado, el flujo de aire empleado fue regulado en un flujómetro de aire (Gilmont Instruments, Inc., USA) con regulador antes de ingresar al difusor del sistema experimental fabricado en vidrio Pyrex poroso de porosidad grado 2, correspondiente a un diámetro medio comprendido entre 40 y 100 mm que contenía la muestra a ensayar (20 mL de solución). La estabilidad estática t de la espuma se cuantificó como el tiempo necesario para que la espuma producida descendiera completamente, luego que es apagado el flujo de gas.
3. RESULTADOS Y DISCUSIÓN
3.1 Características físicas y químicas de los biosólidos y de la sal de ácidos húmicos
comercial empleada
Las características físicas y químicas de los BS provenientes de las plantas El Trebal y Tongoy, son descritas en la Tabla 1. El BS de la planta El Trebal presenta un porcentaje de materia orgánica del 55% sobre base seca, mientras que el BS de la planta Tongoy contiene un 81% de materia orgánica.
Tabla 1: Características físicas y químicas de los biosólidos (BS) de las plantas El Trebal (Región Metropolitana, Chile) y Tongoy (Región de Coquimbo, Chile).
Table 1: Physical and chemical characteristics of biosolids from wastewater treatment plants El Trebal (Metropolitan Region, Chile) and Tongoy (Coquimbo Region, Chile).
Los resultados de la Tabla 1 muestran heterogeneidad entre los BS, particularmente en cuanto al contenido de metales (hierro y cinc), de macronutrientes totales (nitrógeno, fósforo y potasio) y de sulfato. Estas diferencias podrían tener su origen en el tipo de tratamiento de aguas servidas empleado, el origen y composición de los residuos domiciliarios a tratar en dichos sistemas y la distinta composición del agua potable en ambas regiones.
El ácido húmico comercial (AHc) presenta una composición característica de 44,67% de carbono orgánico; 5,87% de hidrógeno; 4,88% de nitrógeno total; 43,9% de oxígeno y 0,58% de ceniza, con una acidez total de 12,3 mol kg-1. La concentración de grupos funcionales tales como COOH y OH fenólico, son de 4,1 y 8,2 mol kg-1, respectivamente [17].
3.2 Espectroscopia Infrarroja con Transformada de Fourier FTIR
Las muestras de AHc y de BS de las plantas El Trebal y Tongoy fueron analizadas en triplicado, obteniéndose en todos los casos espectros con idénticas formas de intensidades de transmitancia, siendo diferentes sólo en algunos máximos la intensidad de transmitancia. Al comparar las muestras de BS y AHc, sólo se encontraron distintos grupos funcionales en la región de 500 a 2000 cm-1.
Para BS de El Trebal, la Figura 1 muestra una intensa banda en la región de 1650 cm-1, la cual se atribuye a la tensión C=O de ácidos carboxílicos, aldehídos conjugados, quinonas y/o grupos carbonilos de amida I. Bandas en la región de 1540 cm-1, se deben a la tensión C=C de compuestos aromáticos (pirroles) y/o vibraciones de flexión N-H y tensión C=N (amidas II). Otra banda de intensidad media se puede distinguir en las proximidades de 1420 cm-1, la cual corresponde a la tensión O-H de alcohol primario (CH3OH) y/o tensión C=N (amidas III). De acuerdo a lo reportado, la mínima transmitancia se encuentra en la región de 1034 cm-1, por lo tanto, los BS de la planta El Trebal tienen un comportamiento acorde a lo publicado [13].
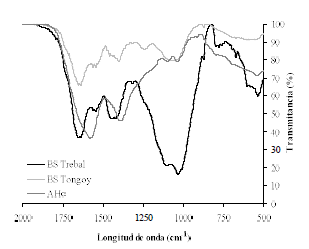
Figura 1: Espectros infrarrojos (IR) de los biosólidos (BS) de las planta El Trebal y Tongoy, además de un ácido húmico comercial (AHc).
Figure 1: Fourier Transformed Infrared Spectroscopy (FT-IR) for biosolids (BS) samples from El Trebal and Tongoy plants and commercial humic acid.
Otros máximos de intensidades débiles y variables se pueden apreciar en las regiones de 900 cm-1, la cual corresponde a la tensión C-H (grupos alcanos) y/o tensión S-H (grupos sulfuros) y los máximos en 798 cm-1 y 535 cm-1 corresponderían a la tensión C-H (grupos aromáticos sustituidos) y tensión Si-O, Si-O-Me (Al, Fe, Mg). Otra banda débil se encuentra en la región de 600 cm-1, la cual, se asocia a nitrocompuestos y/o tensión C-H (grupos alcanos, alquenos) y carbonilos.
Para el BS de la planta Tongoy, el FTIR muestra que el número de grupos funcionales identificados es menor comparado a lo descrito para el BS de El Trebal. Las principales diferencias, en cuanto a número e intensidades de bandas, se encuentran en la región de 1500 a 250 cm-1. Para los BS de Tongoy, la Figura 1 muestra una intensa banda en la región de 1650 cm-1 se atribuye a la tensión C=O de ácidos carboxílicos, aldehídos conjugados, quinonas y/o grupos carbonilos de amida I. Bandas en la región de 1540 cm-1, se deben a la tensión C=C de compuestos aromáticos (Pirroles) y/o vibraciones de flexión N-H y tensión C=N (amidas II). Otra banda de intensidad media se puede distinguir en las proximidades de 1420 cm-1, la cual corresponde a la tensión O-H de alcohol primario (CH3OH) y/o tensión C=N (amidas III). El máximo de intensidad media en la región de 1400 cm-1, se puede asociar a la tensión C-H (grupos alcanos o alquenos), tensión O-H de grupos fenólicos y/o tensión COO- antisimétrica. Otras bandas en la región de 1250 cm-1 y 1100-1050 cm-1, corresponden a la tensión C-O y deformación O-H de COOH, tensión C–O de aril-éter y/o fenoles y, a la tensión C–O de polisacáridos y a la tensión Si-O de impurezas de silicato, respectivamente. Contrariamente a lo reportado en la literatura, el mínimo de transmitancia para el BS de Tongoy no se encuentra en 1034 cm-1, sino que en la región de 1650 cm-1. Esta diferencia podría deberse al tipo de tratamiento de aguas servidas empleado, la composición del agua potable y la proporción de ácidos húmicos y fúlvicos presentes en cada muestra de BS.
Para el ácido húmico comercial (AHc), las principales bandas y máximos se podrían asociar a los siguientes grupos funcionales: 1400 cm-1 (tensión O-H de grupos alcohol y fenol). Otros máximos de intensidad leve en la región de 1100-1000 cm-1 corresponden a la tensión C-O de alcohol y/o C-O-C de éteres y a la tensión C-H aromático, C-O de alcohol y/o C-O-C de aril-éteres, respectivamente. Los máximos de intensidades débiles y variables que se aprecian en la región de 540 cm-1, corresponderían a alcanos.
3.3 Ensayos de tensión superficial
El AHc, los BS y el MIBC muestran una actividad tensoactiva en todo el rango de concentraciones medido (Figura 2). La tensión superficial de AHc es dependiente del pH, mostrando que a pH 10 las soluciones son más tensoactivas que a pH 7. Un comportamiento similar muestran los BS y el MIBC, sin embargo, para altas concentraciones de BS el efecto es cada vez menor debido al efecto buffer que presenta este tipo de sustancias.
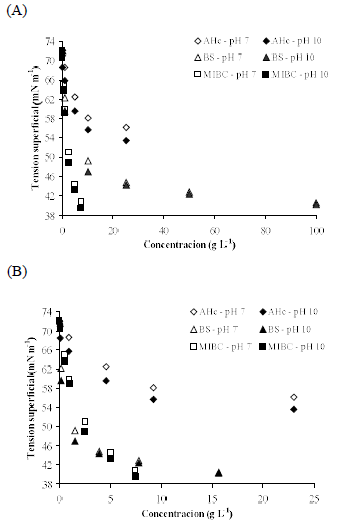
Figura 2: Tensión superficial para pH 7 y 10 a distintas concentraciones de ácido húmico comercial (AHc), biosólidos (BS) y metilisobutilcarbinol (MIBC): (A) Concentración total de espumante (AHc, BS, MIBC); (B) Concentraciones corregidas por la fracción de material sedimentada. En ambas gráficas se muestran los valores promedio (n>=4); las barras de error quedan dentro de los símbolos.
Figure 2: Surface tension measurements for pH 7 and 10 by different concentrations of commercial humic acid, biosolids and Methyl Isobutyl Carbinol (MIBC). (A) Total concentration of foam tested; (B) Correcting the concentrations according to the sedimented fraction. Both graphs shows average values (n>=4); error bars are within symbols.
La Figura 2A muestra que las tensiones superficiales de las soluciones de BS son significativamente menores a aquellas obtenidas con AHc, para concentraciones de sustancias húmicas y condiciones de la solución (pH, temperatura) equivalentes. En la referencia [9], se reporta un comportamiento similar para la tensión superficial de soluciones de suelos y ácido húmico. Los BS permiten cambiar la tensión superficial al igual que el MIBC, determinándose que para una concentración de 100 g L-1 de BS la tensión superficial es 40 mN m-1, en tanto que el MIBC permite obtener una tensión superficial similar con una concentración de 7,5 g L-1.
Para las sustancias húmicas (SH) se ha reportado que la concentración micelar crítica (CMC) estaría en el rango de 5 a 10 g L-1 [18,19], siendo la CMC dependiente del pH, temperatura, naturaleza y composición de las especies catiónicas y de las distintas composiciones químicas de las SH. Para el AHc la CMC esta en el rango de 10 a 25 g L-1, mientras que los BS y el MIBC presentan una CMC de 75 g L-1 y 7,5 g L-1, respectivamente. Para los BS también se espera que la CMC dependa principalmente del origen y composición química elemental de este tipo de sustancias.
Al corregir las concentraciones de AHc y BS por la fracción sedimentada de dichas sustancias, se tiene que los BS tienen un comportamiento similar al MIBC (Figura 2B). Las dosificaciones menores a 4 g L-1 de BS muestran ser más tensoactivas para ambos pH ensayados, comparadas con el MIBC. Por lo tanto, desde el punto de vista operacional, el uso de los BS como espumante es factible, considerando concentraciones equivalentes a las del MIBC. Sin embargo, el uso de los BS debería considerar una etapa de preacondicionamiento que permita separar las fracciones solubles y coloidales que muestran un efecto tensoactivo, de aquellas fracciones sedimentables.
3.4 Ensayo de Bikerman
Las distintas concentraciones de AHc y BS empleadas producen una cantidad significativa de espuma (Figura 3).

Figura 3: Generación de espuma para distintas concentraciones de ácido húmico comercial (AHc), biosólidos (BS) y metilisobutilcarbinol (MIBC), pH 7 y pH 10 y flujos de aire (1 a 4 L min-1). Se muestran los valores promedio (n=4), las barras de error quedan dentro de los símbolos.
Figure 3: Volume of foam generated by different concentrations of humic acids, biosolids and Methyl Isobutyl Carbinol, pH 7 and pH 10 and air flows (1 a 4 L min-1). Graphs shows average values (n>=4), error bars are within symbols.
Para ambas sustancias, el pH tiene un efecto sobre el volumen de espuma generado, obteniéndose que a pH 7 -para una misma concentración- el volumen de espuma es mayor comparado con el obtenido a pH 10. En el caso del MIBC, el pH no muestra un efecto sobre el volumen de espuma; sólo para 10 g L-1 hay diferencia entre el volumen de espuma generado a ambos pH ensayados. En todos los casos, el volumen de espuma muestra tener una dependencia lineal respecto del flujo de gas lo que resulta coherente con lo reportado [16].
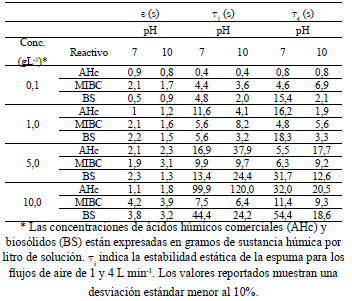
La Tabla 2 resume los índices de generación dinámica de espuma (e) y de estabilidad estática (t), para 2 de los 4 flujos de aire ensayados. Para el AHc, los BS y el MIBC se observa una relación positiva entre la concentración y la generación y estabilidad estática de la espuma.
Tabla 2: Parámetros de Bikerman para ácido húmico comercial (AHc), biosólidos (BS) y metilisobutilcarbinol (MIBC).
Table 2: Bikerman parameters for commercial humic acids, biosolids and Methyl Isobutyl Carbinol.

Los valores de e para el AHc son mayores a pH 10, mientras que los BS y el MIBC muestran un comportamiento distinto, obteniéndose mayores valores a pH 7. La solubilización de distintas sustancias en el AHc y los BS no permiten correlacionar de manera directa los resultados de tensión superficial con los índices de espumación de Bikerman.
En general, las concentraciones de 0,1 y 1 g L-1 de AHc, BS y MIBC presentan valores de t que aumentan según el flujo de aire. Sin embargo, para concentraciones de 5 y 10 g L-1 de AHc y BS, dicha relación es inversa, mostrando que para una concentración fija, al aumentar el flujo de aire el t disminuye drásticamente. Al incrementar el flujo de aire, la espuma es más inestable, favoreciendo la coalescencia de las burbujas producidas.
Los resultados obtenidos muestran que el AHc y los BS tienen una actividad tensoactiva y pueden generar espuma, mostrando distintas estabilidades. Para ambas sustancias, el pH de las respectivas soluciones tiene un efecto significativo, lo que permite obtener distintas especiaciones de los grupos funcionales que fueron determinados mediante FTIR para ambas sustancias. La referencia [20] describe el efecto de la materia orgánica natural, principalmente de sustancias húmicas, sobre la estabilidad de un film líquido entre dos burbujas colindantes, encontrando que las sustancias húmicas en bajas concentraciones (2 mg L-1) reducen o inhiben la coalescencia de las burbujas e incrementan el tiempo de coalescencia, siendo menor dicho efecto para concentraciones superiores a 25 mg L-1.
4. CONCLUSIONES
Al igual que los reactivos químicos usados como espumantes en la industria minera, el AHc y los BS son capaces de cambiar la tensión superficial de una solución, además de generar y estabilizar espumas de manera transiente. El pH afecta fuertemente el cambio en la tensión superficial obtenida con las especies estudiadas (AHc, BS y MIBC), determinándose que su efecto es mayor en el AHc. Sin embargo, sólo los BS permiten obtener un cambio de tensión superficial similar al obtenido con el MIBC, considerando concentraciones y condiciones de solución equivalentes. Adicionalmente, los BS muestran parámetros de Bikerman (e y t) del mismo orden de magnitud a los obtenidos para el MIBC, para las concentraciones y flujos de aire ensayados.
Los BS de distintos orígenes presentan composiciones químicas (macronutrientes y metales), propiedades físicas y grupos funcionales diversos. Sin embargo, los BS estudiados muestran en común la existencia de polímeros solubles como proteínas y azúcares. Además, los ensayos FTIR muestran que los BS presentan grupos funcionales cargados negativamente (OH- y –COO-). Estas sustancias, son capaces de producir espuma y poseen regiones de hidrofobicidad que podrían ser las responsables del efecto tensoactivo observado.
A diferencia del AHc, los BS son capaces de cambiar en forma importante la tensión superficial de una solución, generando y estabilizando espumas. Sin embargo, para un uso efectivo de estas sustancias como espumante, se recomienda considerar una etapa de preacondicionamiento, la que permita separar las fracciones solubles y coloidales que muestran un efecto tensoactivo, de aquellas fracciones sedimentables.
AGRADECIMIENTOS
Esta investigación fue parcialmente financiada por la Comisión Nacional de Investigación Científica y Tecnológica, CONICYT, del Gobierno de Chile, a través del proyecto Nº AT-24080010.
REFERENCIAS
[1] HERRERA-URBINA, R. Recent developments and advances in formulations and applications of chemical reagents used in froth flotation. Miner. Process. Extr. M., 24, 139-182, 2003.
[2] CHOCKALINGAM, E., SUBRAMANIAN, S. AND NATARAJAN, K.A. Studies on biodegradation of organic flotation collectors using Bacillus polymyxa. Hydrometallurgy, 71, 249-256, 2003.
[3] DOPSON, M., SUNDKVIST, J. AND LINDSTROM, E. Toxicity of metal extraction and flotation chemicals to Sulfolobus metallicus and chalcopyrite bioleaching. Hydrometallurgy, 81, 205-213, 2006.
[4] GUELLIL, A., BOUALAM, M., QUIQUAMPOIX, H., GINESTET, P., AUDIO, J.M. AND BLOCK, J.C. Hydrolysis of wastewater colloidal organic matter by extra-cellular enzymes extracted from activated sludge flocs. Water Sci. Technol., 43(6), 33-40, 2001.
[5] MURPHY, S.N., NOVAK, J.T., HOLBROOK, R.D. AND SUROVIK, F. Mesophilic aeration of autothermal thermophilic aerobically digested biosolids to improve plant operations. Water Environ. Res., 72(4), 476-483, 2000.
[6] FROLUND, B., PALMGREN, R., KEIDING, K. AND NIELSEN, P.H. Extraction of extracellular polymers from activated sludge using a cation exchange resin. Water Res., 30, 1749-1758, 1996.
[7] DIGNAC, M.F., URBAIN, V., RYBACKI, D., BRUCHET, A., SNIDARO, D. AND SCRIBE, P. Chemical description of extracellular polymers: Implication on activated sludge flor structure. Water Sci. Technol., 38(8-9), 45-53, 1998.
[8] PARK, C., NOVAK, J.T., HELM, R.F., AHN, Y. AND ESEN, A. Evaluation of the extracellular proteins in full-scale activated sludges. Water Res., 42, 3879-3889, 2008.
[9] ANDERSON, M.A., HUNG, A.Y.C., MILLS, D. AND SCOUT, M.S. Factors affecting the surface tension of soils solutions and solutions of humic acid. Soil Sci., 160(2), 111-116, 1995.
[10] STEVENSON, F.J. Humus Chemistry: Genesis, composition, reaction. John Wiley & Sons, Inc., 1994.
[11] FILIP, Z. AND BIELEK, P. Susceptibility of humic acids from soils with various contents of metals to microbial utilization and transformation. Biol. Fert. Soils., 36,426-433, 2002.
[12] SENESI, N., D'ORAZIO, V. AND RICCA, G. Humic acids in the first generation of EUROSOILS. Geoderma, 116, 325- 344, 2003.
[13] GRUBE, M., LIN, J.G., LEE, P.H. AND KOKOREVICHA, S. Evaluation of sewage sludge-based compost by FT-IR spectroscopy. Geoderma, 130, 324-333, 2006.
[14] BIKERMAN, J.J. Foams, Springer-Verlag, New York, 1973.
[15] GUPTA, A.K., BANERJEE, P.K., MISHRA, A., SATISH, P. AND PRADIP. Effect of alcohol and polyglycol ether frothers on foam stability, bubble size and coal flotation. Int. J. Miner. Process., 82, 126-137, 2007.
[16] BLUTE, I., PUGH, R.J., VAN DE PAS, J. AND CALLAGHAN, I. Industrial manufactured silica nanoparticle sols. 2. Surface tension, particle concentracion, foam generation and stability. Colloids and Surfaces A: Physicochem. Eng. Aspects., 337, 127-135, 2009.
[17] PANDEY, A.K., PANDEY, S.D., MISRA, V. AND VISWANATHAN, P. N. Formation of Soluble Complexes of Metals with Humic Acid and Its Environmental Significance. Chem. Ecol., 16(4), 269-282, 1999.
[18] CHILOM, G., BRUNS, A.S. AND RICE, J.A. Aggregation of humic acid in solution: Contributions of different fractions. Organic Geochemistry, 40, 455-460, 2009.
[19] TOMBÁCZ, E. Colloidal properties of humic acids and spontaneous changes of their colloidal state under variable solution conditions. Soil Sci., 164(11), 814-824, 1999.
[20] SPYRIDOPOULOS, M.T. AND SIMONS, S.J.R. Particulate interactions in water flotation froths: a micro-mechanistic approach. Int. J. Miner. Process., 74, 115-120, 2004.
Cómo citar
IEEE
ACM
ACS
APA
ABNT
Chicago
Harvard
MLA
Turabian
Vancouver
Descargar cita
Visitas a la página del resumen del artículo
Descargas
Licencia
Derechos de autor 2011 DYNA

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial-SinDerivadas 4.0.
El autor o autores de un artículo aceptado para publicación en cualquiera de las revistas editadas por la facultad de Minas cederán la totalidad de los derechos patrimoniales a la Universidad Nacional de Colombia de manera gratuita, dentro de los cuáles se incluyen: el derecho a editar, publicar, reproducir y distribuir tanto en medios impresos como digitales, además de incluir en artículo en índices internacionales y/o bases de datos, de igual manera, se faculta a la editorial para utilizar las imágenes, tablas y/o cualquier material gráfico presentado en el artículo para el diseño de carátulas o posters de la misma revista.

















