Biología del áfido negro (Aphis craccivora: Aphididae) sobre fríjol caupi (Vigna unguiculata, Fabaceae)
Biology of Black Aphid (Aphis Craccivora: Aphididae) on Cowpea (Vigna Unguiculata, Fabaceae)
DOI:
https://doi.org/10.15446/abc.v20n3.43064Palabras clave:
estadísticos vitales, parámetros poblacionales, tasa intrínseca de crecimiento, tabla de vida (es)intrinsic rate of increase, life table, population parameters, vital statistics (en)
Este trabajo describe los parámetros biológicos y poblacionales del pulgón negro, Aphis craccivora Koch, sobre fríjol caupí (Vigna unguiculata (L. Walp.)), bajo condiciones de laboratorio. Los insectos se criaron sobre plántulas individualizadas a una temperatura promedio de 28 °C, humedad relativa de 70 % y fotoperiodo de 12 horas. Los parámetros medidos fueron periodo ninfal, fecundidad, supervivencia, periodo pre-reproductivo y aspectos relativos a la tasa de crecimiento del áfido. La tasa reproductiva neta R (0) fue 66,00, la tasa intrínseca de crecimiento del áfido (rm) fue 0,51, el tiempo de duplicación de la población (TD) fue 2,3. Se analizaron las curvas de supervivencia (lx), fecundidad (mx), la duración del período ninfal y reproductivo del áfido. Los resultados difieren de los realizados en otras variedades de fríjol caupí, evidenciándose la susceptibilidad de la variedad criolla usada por los agricultores en la costa Caribe colombiana.
This research describes the population and biological parameters of the black aphid (Aphis craccivora Koch) on cowpea bean (Vigna unguiculata (L. Walp.)), under laboratory conditions. The insects were raised on individualized seedlings in an average temperature of 28 °C, at 70 % relative humidity during a photoperiod of 12 hours. The parameters measured were the nymphal period, fecundity, longevity, pre-reproductive period and aspects of aphid growth rate. The net reproductive rate R (0) was 66.00, the intrinsic g rate of increase of the aphid (rm) was 0.51, and the population doubling time (TD) was 2.3. Survival curves (lx), fecundity (mx), the duration of nymphal and the reproductive period of the aphid were analyzed. The results differ from those found in other varieties of cowpea beans, demonstrating the susceptibility of the native variety used by farmers in the Colombian Caribbean coast.
Doi: https://doi.org/10.15446/abc.v20n3.43064.
Artículo de investigación/Original research paper
BIOLOGÍA DEL ÁFIDO NEGRO (Aphis craccivora: APHIDIDAE) SOBRE FRÍJOL CAUPI (Vigna unguiculata, FABACEAE)
Biology of Black Aphid (Aphis Craccivora: Aphididae) on Cowpea(Vigna Unguiculata, Fabaceae)
Nataly DE LA PAVA S1, Paula A. SEPÚLVEDA-CANO1.
1 Laboratorio de Entomología, Universidad del Magdalena. Carrera 32 n.° 22-08 Hangar B. Santa Marta, Colombia.
For correspondence. natalydlp@gmail.com.
Received: 17th March 2014, Returned for revision: 20th August 2014, Accepted: 9th January 2015.
Associate Editor: Víctor López Martínez.
Citation / Citar este artículo como: De La Pava S N, Sepúlveda-Cano PA. Biología del áfido negro (Aphis craccivora: Aphididae) sobre fríjol caupi (Vigna unguiculata, Fabaceae). Acta biol. Colomb. 2015;20(3):93-97. doi: https://doi.org/10.15446/abc.v20n3.43064.
RESUMEN
Este trabajo describe los parámetros biológicos y poblacionales del pulgón negro, Aphis craccivora Koch, sobre fríjol caupí (Vigna unguiculata (L. Walp.)), bajo condiciones de laboratorio. Los insectos se criaron sobre plántulas individualizadas a una temperatura promedio de 28 °C, humedad relativa de 70 % y fotoperiodo de 12 horas. Los parámetros medidos fueron periodo ninfal, fecundidad, supervivencia, periodo pre-reproductivo y aspectos relativos a la tasa de crecimiento del áfido. La tasa reproductiva neta R (0) fue 66,00, la tasa intrínseca de crecimiento del áfido (rm) fue 0,51, el tiempo de duplicación de la población (TD) fue 2,3. Se analizaron las curvas de supervivencia (lx), fecundidad (mx), la duración del período ninfal y reproductivo del áfido. Los resultados difieren de los realizados en otras variedades de fríjol caupí, evidenciándose la susceptibilidad de la variedad criolla usada por los agricultores en la costa Caribe colombiana.
Palabras clave: estadísticos vitales, parámetros poblacionales, tasa intrínseca de crecimiento, tabla de vida.
ABSTRACT
This research describes the population and biological parameters of the black aphid (Aphis craccivora Koch) on cowpea bean (Vigna unguiculata (L. Walp.)), under laboratory conditions. The insects were raised on individualized seedlings in an average temperature of 28 °C, at 70 % relative humidity during a photoperiod of 12 hours. The parameters measured were the nymphal period, fecundity, longevity, pre-reproductive period and aspects of aphid growth rate. The net reproductive rate R (0) was 66.00, the intrinsic g rate of increase of the aphid (rm) was 0.51, and the population doubling time (TD) was 2.3. Survival curves (lx), fecundity (mx), the duration of nymphal and the reproductive period of the aphid were analyzed. The results differ from those found in other varieties of cowpea beans, demonstrating the susceptibility of the native variety used by farmers in the Colombian Caribbean coast.
Keywords: intrinsic rate of increase, life table, population parameters, vital statistics.
INTRODUCCIÓN
El fríjol caupí (Vigna unguiculata L. Walp.) es una de las leguminosas más usadas en los trópicos y subtrópicos para el consumo humano y para la alimentación de animales (Jackai y Daoust, 1986), es un sistema de cultivo importante en las regiones más secas de los trópicos cubriendo partes de Asia, Oceanía, Oriente Medio, el sur de Europa, África, el sur de EE.UU, y América Central y del Sur (Singh et al., 2002; Diouf y Hilu, 2005). El fríjol caupí ocupa el primer lugar en importancia económica en el Caribe colombiano, donde es cultivado por pequeños agricultores en áreas que van desde 1.000 a 10.000 m2 (Araméndiz-Tatis et al., 2011). La principal plaga de este cultivo es el pulgón negro, Aphis craccivora Koch, reportado en regiones de África, Asia y América Latina (Pettersson et al., 1998). Los adultos son en su mayoría de color negro brillante o marrón oscuro, de tamaño variable entre 1,5 y 2 mm de largo. Las ninfas son ápteras, de color marrón oscuro y de forma redondeada (Obopile y Ositile, 2010). La mayoría de los cultivos agrícolas sirven como plantas hospederas de varias especies de áfidos cuya alimentación reduce el rendimiento de las cosechas (Hales et al., 1997). El daño que ocasiona A. craccivora al fríjol es causado por los adultos y ninfas (Ofuya, 1997), que se alimentan succionando la sabia de los brotes terminales, pecíolos, flores y vainas (Asiwe, 2009) y en ataques severos pueden matar las plantas jóvenes, mientras que causa reducción en la tasa de crecimiento, distorsión de las hojas y retraso en el inicio de la floración y en el tamaño de las vainas de las plantas que sobreviven (Jackai y Daoust, 1986). No obstante, el efecto perjudicial más notable de A. craccivora es la transmisión del virus del mosaico (Cowpea aphid borne mosaic virus, CABMV) en hasta el 40 % de las semillas, ocasionando pérdida en el rendimiento del cultivo (Bashir et al., 2002; Ojuederie et al., 2009; González, 2012;), en Nigeria es considerada la enfermedad viral mas importante en Caupí (Ojuederie et al., 2009).
Uno de los mecanismos empleados en el manejo integrado de esta plaga, es el uso de variedades resistentes, método ambientalmente adecuado y económico que ofrece a los agricultores el control de insectos mediante el uso mejorado de las características genéticas de la planta (Obopile y Ositile, 2010). Sin embargo, en Colombia la calidad de la semilla de fríjol ha sido un factor que ha limitado el cultivo, debido a la baja oferta en el mercado de semilla certificada, hecho que obligó a los productores a producir sus propias semillas (Restrepo et al., 2007). Cuando los agricultores cultivan semillas sin selección o certificación, a menudo sufren pérdidas en la producción debido a los daños causados por plagas, por lo que se hace importante conocer los aspectos biológicos y parámetros poblacionales de estos insectos sobre las variedades sembradas en cada región, estimados a partir de las tablas de vida desarrolladas en laboratorio (Southwood, 1994; La Rossa et al., 2005), permitiendo esto implementar medidas para el manejo de las poblaciones en campo, estableciendo los tiempos de desarrollo de la plaga y la calidad de las variedades a usar.
El objetivo de este estudio fue evaluar la biología y los parámetros demográficos de A. craccivora sobre una variedad criolla de fríjol caupí en condiciones de laboratorio. Se estudió la fecundidad, supervivencia, tasa intrínseca de crecimiento natural, el período de pre-reproducción y tasa de crecimiento relativo, para la estimación de los parámetros biológicos y demográficos de la población de A. craccivora.
MATERIALES Y MÉTODOS
El trabajo se realizó en las instalaciones del laboratorio de Entomología de la Universidad del Magdalena, bajo condiciones controladas, a una temperatura promedio de 28 °C, 70 % de humedad relativa y 12 horas luz. Se trabajó con dos cohortes de A. craccivora sobre una variedad criolla de V. unguiculata.
Para la obtención del pie de cría del insecto se establecieron en el Centro de Desarrollo Agrícola y Forestal de la Universidad del Magdalena (74°11'5,33" W; 11°13'28,98'' N, 21 m.s.n.m.) tres parcelas de 1 m2 con una variedad criolla de semilla de fríjol caupí. Conjuntamente se realizó una siembra en semillero, siendo individualizadas las plántulas de 15 cm de altura en vasos de icopor de 14 oz, usando como sustrato turba y arena en proporción 1:1. Una vez obtenidas las plántulas se trasladaron al laboratorio para la cría del pulgón. El material de estudio se aisló en jaulas de cría artesanales fabricadas de acetato con pequeñas ventanas para ventilación, cubiertas con una fina malla para permitir la respiración tanto de la planta como del áfido. Se transfirió una hembra adulta de A. craccivora por planta, para una población total de 20 hembras adultas de la misma cohorte, en ambos ensayos. Transcurridas 24 horas se retiraron todas las hembras y las ninfas neonatas, menos una, de cada planta. Diariamente se registraron por observación directa con una lupa (Triplet Magnifier 10X) los cambios de instar, el número de insectos muertos y los nacimientos una vez que alcanzaron el estado adulto.
Se observaron los parámetros de: periodo ninfal, los periodos pre-reproductivo y reproductivo y la supervivencia. Con la información obtenida se elaboró la tabla de vida correspondiente siguiendo la metodología propuesta por Southwood (1994) y La Rossa et al. (2005).
A partir de la elaboración de la tabla de vida y basándose en el trabajo de Godoy y Cividanes (2002) se estimaron los estadísticos vitales: intervalo de edad (x), supervivencia por edades (lx); fecundidad por edades (mx); y los siguientes parámetros poblacionales: tasa neta de reproducción (Ro), intervalo de tiempo entre cada generación (T), tasa intrínseca de incremento natural (r ), la razón finita de aumento (À) y el tiempo necesario para la duplicación en número de la población (DT), donde:
R0 - Σ (mx.lx)
T-(Σx.mx.lx)/(Σmx.lx)
rm - ln R0/T
λ-erm
DT - Ln (2)/rm
RESULTADOS
Ciclo de vida
El ciclo de vida de A. craccivora sobre la variedad criolla de fríjol caupí utilizada presentó tres ínstares ninfales previos a la emergencia del adulto de la primera cohorte, tardando 1,40 ± 0,49, 1,44 ± 0,53 y 1,80 ± 0,72 días el primer, segundo y tercer instar, respectivamente. El periodo pre-reproductivo fue de 0,57 ± 0,18 días y el tiempo de vida promedio de 16,5 ± 5,15 días.
Supervivencia y fecundidad
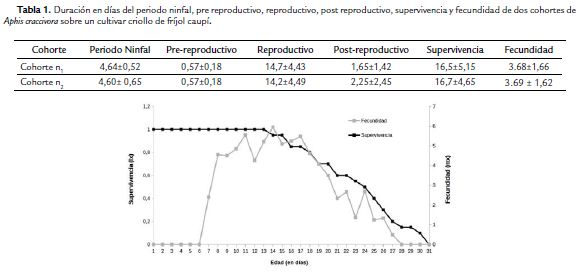
La duración de los periodos de desarrollo y fecundidad entre las dos cohortes (n1:20; n2:20) no variaron significativamente, alcanzando el estado adulto a los 4,64 (± 0,52) y 4,60 (± 0,65) días respectivamente. El periodo reproductivo de A. craccivora inició el mismo día en que los afidos se tornaron a adultos. Los resultados de las variables de supervivencia y fecundidad evaluados para cada cohorte se registran en la Tabla 1.
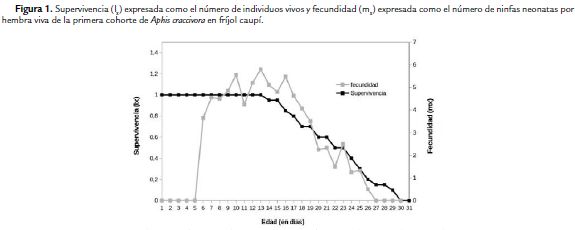
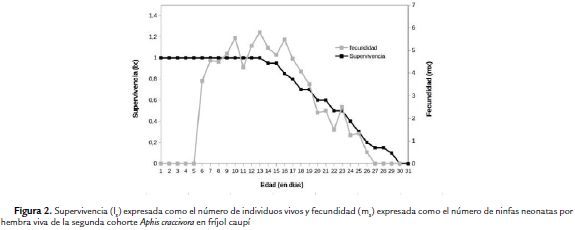
En las figuras 1 y 2 se muestran las curvas de supervivencia (lx) y fecundidad (mx) de las dos cohortes evaluadas. En la curva de supervivencia por edades se observa que existe un comportamiento similar para ambas cohortes iniciando la mortalidad a edades similares (14 días a partir del nacimiento) y describen una pendiente abrupta con la muerte de al menos un individuo diariamente.
Parámetros de la tabla de vida
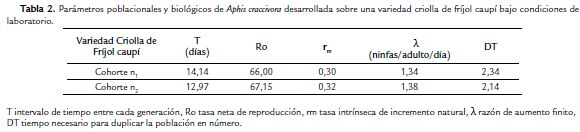
El intervalo de tiempo entre cada generación (T) de A. craccivora disminuyó entre cada cohorte, reduciéndose el tiempo que transcurre entre el nacimiento de un individuo y el nacimiento de sus descendientes. Con relación a la tasa neta de reproducción (Ro) se evidenció mayor tasa en la cohorte n2 (67,15 ninfas/adulto) con respecto a la cohorte n1 (66,00 ninfas/adulto). La tasa intrínseca de incremento natural (rm) mostró una tendencia similar para Ro corroborando el potencial biótico de la especie. La razón finita de aumento (λ) fue de 1,34 y 1,38 ninfas/adulto/día para la cohorte n1 y n2 respectivamente. El tiempo necesario para duplicar la población fue de 2,34 y 2,14 días (Tabla 2). Todos estos parámetros poblacionales muestran la eficiencia de la especie para la colonización de esta variedad de V. unguiculata y evidencian una reducción paulatina en los tiempos de desarrollo del áfido.
DISCUSIÓN
En este estudio, el áfido criado sobre la variedad criolla de fríjol caupí que los agricultores tradicionalmente usan en la parte norte del Caribe Colombiano, mostró un periodo reproductivo corto comparado con los 22, 33, 16 días obtenidos por Kuo y Chen (2004), Hafiz (2006), Obopile y Ositile (2010), sobre las variedades espárrago, pinkeye y BYE blackeye de frijol caupí, respectivamente. El desarrollo de los instares ninfales de una especie, su crecimiento y reproducción dependen de la variedad del hospedero y las condiciones en las cuales se desarrolla la cría (Annan et al., 1997; Awmack y Leather, 2002; Asiwe, 2009; Obopile y Ositile, 2010). La tasa de crecimiento, reproducción y el número de instares en diferentes especies de áfidos dependen de la interacción de factores bióticos y abióticos como la temperatura, humedad, lluvia y viento, siendo los dos primeros relevantes en condiciones de laboratorio (Hales et al., 1997), lo que puede explicar las diferencias entre los estudios mencionados. La temperatura por sí sola puede causar diferencias en el tiempo de desarrollo ninfal de las especies, Kuo y Chen (2004) demostraron que el incremento gradual de la temperatura disminuye el tiempo de desarrollo de las ninfas, alcanzándose a desarrollar un instar diario a los 30 °C, al igual que lo reportado en este estudio.
Los resultados muestran que la variedad criolla usada tuvo un efecto positivo en el crecimiento y reproducción de A. craccivora, lo que indica una alta susceptibilidad de la planta al ataque de esta plaga. En los insectos chupadores, los cortos periodos pre-reproductivos y el incremento de la tasa reproductiva de la especie en un hospedero refleja la idoneidad de la planta para el desarrollo del insecto (Van Lenteren y Noldus, 1990). Esta variedad criolla como hospedero permitiría el desarrollo de la cría de áfidos para futuros estudios, pero representa un riesgo alto para el agricultor.
La curva de supervivencia y fecundidad de A. craccivora describen un comportamiento similar al encontrado en algunas variedades susceptibles de fríjol espárrago y fríjol caupí trabajadas por Kuo y Chen (2004) y Obopile y Ositile (2010). Sin embargo, la tasa neta de reproducción (Ro) fue mayor en este estudio que la Ro de 62,7 y 43,8, reportada en los trabajos antes mencionados. La tasa intrínseca de crecimiento natural (rm) en función de la supervivencia por edad (lx) y fecundidad (mx) ha sido usada para medir el rendimiento de los áfidos en diferentes vegetales (Ricci y Kahan, 2001; Michelotto et al., 2004). El alto valor de rm indica el potencial que tiene una especie para reproducirse en una variedad (Schowalter, 2006) y el incremento que la especie A. craccivora tendrá se observa en la cohorte n2 donde el tiempo necesario para el desarrollo reproductivo de ésta disminuyó.
De acuerdo con la tabla de vida y los parámetros poblacionales encontrados para la especie A. craccivora, la variedad criolla de fríjol caupí muestra una baja resistencia favoreciendo el desarrollo de la plaga, lo que puede deberse probablemente a características nutricionales ligadas a la variedad (Asiwe, 2009; Obopile y Ositile, 2010). Investigaciones futuras podrían evaluar la interacción de A. craccivora entre las variedades resistentes de la zona y las diferentes condiciones ambientales, detectando variedades de fríjol caupí con potencial de resistencia a la plaga.
CONCLUSIONES
La especie Aphis craccivora sobre la variedad criolla de frijol caupí presenta un crecimiento poblacional que implica una reducción en el intervalo de tiempo entre la aparición de cada generación (T), y por ende una disminución del tiempo necesario para duplicar la población (DT). Se evidencia una baja resistencia de la variedad criolla de fríjol caupí al ataque de este pulgón, que dadas las características nutricionales de la variedad y el manejo de la misma en campo, están favoreciendo el desarrollo de la plaga .
Las características intrínsecas de la especie reflejadas en los valores de rm y λ en las dos generaciones de Aphis craccivora son un mecanismo para establecer la susceptibilidad de la variedad de fríjol caupí a esta plaga.
AGRADECIMIENTOS
Esta investigación ha sido realizada gracias al apoyo de la Universidad del Magdalena, Colciencias y el Programa Jóvenes Investigadores e Innovadores - convenio Colciencias-UNIMAGDALENA No. 0739 de 2012.
REFERENCIAS
Annan IB, Schaefers GA, Tingey WARD, Tjallingii WF. Effects of treatments for electrical penetration graph recordings on behaviour and biology of Aphis craccivora (Aphididae). Physiol Entomol. 1997;22(2):95-101. Doi:10.1111/j.1365-3032.1997.tb01145.x.
Araméndiz-Tatis A, Espitia-Camacho M, Sierra C M. Comportamiento agronómico de líneas promisorias de fríjol caupí, Vigna unguiculata L. Walp en el valle del Sinú. Temas Agrarios. 2011;16(2):9-17.
Asiwe JAN. The impact of phosphate fertilizer as a pest management tactic in four cowpea varieties. Afr J Biotechnol. 2009;24(8):7182-7186.
Awmack CS, Leather SR. Host plant quality and fecundity in herbivorous insects. Annu Rev Entomol. 2002;47(1):817-844. Doi: 10.1146/annurev.ento.47.091201.145300.
Bashir M, Ahmad Z, Ghafoor A. Cowpea germplasm evaluation for virus resistance under greenhouse conditions. Asian J Plant Sci. 2002;1(5):585-587. Doi:10.3923/ajps.2002.585.587.
Diouf D, Hilu KW. Microsatellites and RAPD markers to study among cowpea breeding lines and local varieties in Senegal. Genet Resour Crop Evol. 2005;52:1057-1067. Doi:10.1007/s10722-004-6107-z.
Godoy KB, Cividanes FJ. Tabelas de esperança de vida e fertilidade para Lipaphis erysimi (Kalt.) (Hemiptera: Aphididae) em condições de laboratório e campo. Neotrop Entomol. 2002;31(1):41-48. Doi: https://doi.org/10.1590/S1519-566X2002000100006.
González G. Enfermedades virales cuarentenarias para Cuba en los cultivos de frijol (Phaseolus vulgaris, L.) y soya (Glycinemax (L.) Merrill). Fitosanidad. 2012;16(1):13-17.
Hafiz NA. Use of life tables to asses host plant resistance in cowpea to Aphis craccivora Koch (Homoptera: Aphididae). Ass Univ Bull Environ Res. 2006;9(1):1-6.
Hales DF, Tomiuk J, Wõhrmann K, Sunnucks P. Evolutionary and genetic aspects of aphid biology: a review. Eur J Entomol. 1997;94(1):1-55.
Jackai LEN, Daoust RA. Insect pests of cowpeas. Annu Rev Entomol. 1986;31(1):95-119. Doi: 10.1146/annurev. en.31.010186.000523.
Kuo MH, Chen CY. Development and population parameters of the cowpea aphid, Aphis craccivora Koch (Hemiptera: Aphididae), at various constant temperatures. Form Entomol. 2004;24(4):305-315.
La Rossa FR, Vasicek A, López M, Mendy M, Paglioni A. Biología y demografía de Brevicoryne brassicae (L.) (Hemiptera: Aphididae) sobre cuatro variedades de Brassica oleracea (L.) en condiciones de laboratorio. RIA: Revista de Investigaciones Agropecuarias. 2005;34(3):105-114.
Michelotto MD, Da Silva RA, Busoli AC. Tabelas de vida para Aphis gossypii Glover, 1877 (Hemiptera: Aphididae) em três espécies de plantas daninhas. Bol Sanid Veg Plagas. 2004;30(2):211-218.
Obopile M, Ositile B. Life table and population parameters of cowpea aphid, Aphis craccivora Koch (Homoptera: Aphididae) on five cowpea Vigna unguiculata (L. Walp.) varieties. J Pest Sci. 2010;83(1):9-14. Doi: 10.1007/s10340-009-0262-0.
Ofuya TI. Control of the cowpea aphid, Aphis craccivora Koch (Homoptera: Aphididae), in cowpea, Vigna unguiculata (L. Walp.) Integrated Pest Manag Rev. 1997;2(4):199-207. Doi: 10.1023/A:1018461320137.
Ojuederie OB, Odu BO, Ilori CO. Serological detection of seed borne viruses in cowpea regenerated germplasm using protein a sandwich enzyme linked immunorsorbent assay. Afr Crop Sci J. 2009;17(3):125-132. Doi: https://doi.org/10.4314/acsj.v17i3.54212.
Pettersson J, Karunaratne S, Ahmed E, Kumar V. The cowpea aphid, Aphis craccivora, host plant odours and pheromones. Entomol Exp Appl. 1998;88(2):177-184. Doi: 10.1046/j.1570-7458.1998.00360.x.
Restrepo J H A, Martínez T R, Carmona M J. Buenas prácticas agrícolas (bpa) en la producción de fríjol voluble [internet]. 1ª ed. Roma: Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO); 2007 [actualizado 3 nov 2014; citado 9 abr 2014]. Disponible en http://www.fao.org/3/contents/962b5b2f-5e7c-544c-8375-6db3b1d1cd27/a1359s00.pdf.
Ricci E M, Kahan A E j. Fertilidad, tablas de vida y supervivencia de Brevicoryne brassicae L (Homoptera: Aphidoidea) sobre distintas variedades comerciales de repolla (Brassica oleracea var. capitata L.). Bol San Veg Plagas. 2001;27(3):389-394.
Southwood T R E. Ecological methods. 2 ed. London, UK: Chapman & Hall Pub; 1994. p. 404 -434.
Schowalter TD. Insect ecology: an ecosystem approach. 2 ed. Louisiana State University:Academic Press; 2006. p. 149-150.
Singh B B, Ehlers J D, Sharma B, Freire Filho F R. Recent progress in cowpea Breeding. En: Fatokun C A, Tarawali S A, Singh B B, Kormawa P M, Tamo M, editores. Challenges and Opportunities for Sustainable Cowpea Production. 1st ed. Ibadan, Nigeria: International Institute ofTropical Agriculture (IITA); 2002. p.22-40.
Van Lenteren J C, Noldus L P JJ. Whitefly-plant relationships: behavioural and ecological aspects. En: Gerling D, editor. Whiteflies: their Bionomics. Pest Status and Management. Andover, UK: Intercept Ltd; 1990. p. 47-90.
Referencias
Annan IB, Schaefers GA, Tingey WARD, Tjallingii WF. Effects of treatments for electrical penetration graph recordings on behaviour and biology of Aphis craccivora (Aphididae). Physiol Entomol. 1997;22(2):95-101. Doi:10.1111/j.1365-3032.1997.tb01145.x.
Araméndiz-Tatis A, Espitia-Camacho M, Sierra C M. Comportamiento agronómico de líneas promisorias de fríjol caupí, Vigna unguiculata L. Walp en el valle del Sinú. Temas Agrarios. 2011;16(2):9-17.
Asiwe JAN. The impact of phosphate fertilizer as a pest management tactic in four cowpea varieties. Afr J Biotechnol. 2009;24(8):7182-7186.
Awmack CS, Leather SR. Host plant quality and fecundity in herbivorous insects. Annu Rev Entomol. 2002;47(1):817-844. Doi: 10.1146/annurev.ento.47.091201.145300.
Bashir M, Ahmad Z, Ghafoor A. Cowpea germplasm evaluation for virus resistance under greenhouse conditions. Asian J Plant Sci. 2002;1(5):585-587. Doi:10.3923/ajps.2002.585.587.
Diouf D, Hilu KW. Microsatellites and RAPD markers to study among cowpea breeding lines and local varieties in Senegal. Genet Resour Crop Evol. 2005;52:1057-1067. Doi:10.1007/s10722-004-6107-z.
Godoy KB, Cividanes FJ. Tabelas de esperança de vida e fertilidade para Lipaphis erysimi (Kalt.) (Hemiptera: Aphididae) em condições de laboratório e campo. Neotrop Entomol. 2002;31(1):41-48. Doi: https://doi.org/10.1590/S1519-566X2002000100006.
González G. Enfermedades virales cuarentenarias para Cuba en los cultivos de frijol (Phaseolus vulgaris, L.) y soya (Glycinemax (L.) Merrill). Fitosanidad. 2012;16(1):13-17.
Hafiz NA. Use of life tables to asses host plant resistance in cowpea to Aphis craccivora Koch (Homoptera: Aphididae). Ass Univ Bull Environ Res. 2006;9(1):1-6.
Hales DF, Tomiuk J, Wõhrmann K, Sunnucks P. Evolutionary and genetic aspects of aphid biology: a review. Eur J Entomol. 1997;94(1):1-55.
Jackai LEN, Daoust RA. Insect pests of cowpeas. Annu Rev Entomol. 1986;31(1):95-119. Doi: 10.1146/annurev. en.31.010186.000523.
Kuo MH, Chen CY. Development and population parameters of the cowpea aphid, Aphis craccivora Koch (Hemiptera: Aphididae), at various constant temperatures. Form Entomol. 2004;24(4):305-315.
La Rossa FR, Vasicek A, López M, Mendy M, Paglioni A. Biología y demografía de Brevicoryne brassicae (L.) (Hemiptera: Aphididae) sobre cuatro variedades de Brassica oleracea (L.) en condiciones de laboratorio. RIA: Revista de Investigaciones Agropecuarias. 2005;34(3):105-114.
Michelotto MD, Da Silva RA, Busoli AC. Tabelas de vida para Aphis gossypii Glover, 1877 (Hemiptera: Aphididae) em três espécies de plantas daninhas. Bol Sanid Veg Plagas. 2004;30(2):211-218.
Obopile M, Ositile B. Life table and population parameters of cowpea aphid, Aphis craccivora Koch (Homoptera: Aphididae) on five cowpea Vigna unguiculata (L. Walp.) varieties. J Pest Sci. 2010;83(1):9-14. Doi: 10.1007/s10340-009-0262-0.
Ofuya TI. Control of the cowpea aphid, Aphis craccivora Koch (Homoptera: Aphididae), in cowpea, Vigna unguiculata (L. Walp.) Integrated Pest Manag Rev. 1997;2(4):199-207. Doi: 10.1023/A:1018461320137.
Ojuederie OB, Odu BO, Ilori CO. Serological detection of seed borne viruses in cowpea regenerated germplasm using protein a sandwich enzyme linked immunorsorbent assay. Afr Crop Sci J. 2009;17(3):125-132. Doi: https://doi.org/10.4314/acsj.v17i3.54212.
Pettersson J, Karunaratne S, Ahmed E, Kumar V. The cowpea aphid, Aphis craccivora, host plant odours and pheromones. Entomol Exp Appl. 1998;88(2):177-184. Doi: 10.1046/j.1570-7458.1998.00360.x.
Restrepo J H A, Martínez T R, Carmona M J. Buenas prácticas agrícolas (bpa) en la producción de fríjol voluble [internet]. 1ª ed. Roma: Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO); 2007 [actualizado 3 nov 2014; citado 9 abr 2014]. Disponible en http://www.fao.org/3/contents/962b5b2f-5e7c-544c-8375-6db3b1d1cd27/a1359s00.pdf.
Ricci E M, Kahan A E j. Fertilidad, tablas de vida y supervivencia de Brevicoryne brassicae L (Homoptera: Aphidoidea) sobre distintas variedades comerciales de repolla (Brassica oleracea var. capitata L.). Bol San Veg Plagas. 2001;27(3):389-394.
Southwood T R E. Ecological methods. 2 ed. London, UK: Chapman & Hall Pub; 1994. p. 404 -434.
Schowalter TD. Insect ecology: an ecosystem approach. 2 ed. Louisiana State University:Academic Press; 2006. p. 149-150.
Singh B B, Ehlers J D, Sharma B, Freire Filho F R. Recent progress in cowpea Breeding. En: Fatokun C A, Tarawali S A, Singh B B, Kormawa P M, Tamo M, editores. Challenges and Opportunities for Sustainable Cowpea Production. 1st ed. Ibadan, Nigeria: International Institute ofTropical Agriculture (IITA); 2002. p.22-40.
Van Lenteren J C, Noldus L P JJ. Whitefly-plant relationships: behavioural and ecological aspects. En: Gerling D, editor. Whiteflies: their Bionomics. Pest Status and Management. Andover, UK: Intercept Ltd; 1990. p. 47-90.
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
CrossRef Cited-by
1. Gilson Lages Fortes Portela, Paulo Roberto Ramalho Silva, José Edmir Girão Filho, Luiz Evaldo de Moura Pádua, Luiz Carlos de Melo Júnior. (2019). Silicon as resistance inducer in to control black aphid Aphis craccivora Koch, 1854 in Phaseolus lunatus lima beans. Arquivos do Instituto Biológico, 86 https://doi.org/10.1590/1808-1657000512018.
2. José Edmir Girão Filho, Luiz Evaldo de Moura Pádua, Gilson Lages Fortes Portela, Francinalva de Morais Sousa, Jayara Dayany da Costa Silva. (2019). Thermal requirements, life expectancy and fertility tables of Aphis craccivora (Hemiptera: Aphididae) in Vigna unguiculata (Fabales: Fabaceae) under laboratory conditions. Arquivos do Instituto Biológico, 86 https://doi.org/10.1590/1808-1657000142018.
3. Esther Pegalepo, Roland Bocco, Geoffrey Onaga, Francis Nwilene, Manuele Tamò, Abou Togola, Sanjay Kumar Katiyar. (2025). Sustainable Insect Pest Management Options for Rice Production in Sub-Saharan Africa. Insects, 16(11), p.1175. https://doi.org/10.3390/insects16111175.
4. Antonia Débora Camila de Lima Ferreira, Leandro Carvalho da Silva, Daniel Rodrigues Nere, Ervino Bleicher. (2020). Population parameters as a way to evaluate the risk of attack of Aphis craccivora (Hemiptera: Aphididae) on cowpea. Arquivos do Instituto Biológico, 87 https://doi.org/10.1590/1808-1657001102018.
5. Leandro Carvalho da Silva, Daniel Rodrigues Nere, Ervino Bleicher, Antônio Vinícius Correa Barbosa, Eraldo José Madureira Tavares. (2018). Demographic parameters of cowpea aphids on advanced semi-erect cowpea lines. Pesquisa Agropecuária Brasileira, 53(8), p.900. https://doi.org/10.1590/s0100-204x2018000800004.
Dimensions
PlumX
Visitas a la página del resumen del artículo
Descargas
Licencia
Derechos de autor 2015 Acta Biológica Colombiana

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
1. La aceptación de manuscritos por parte de la revista implicará, además de su edición electrónica de acceso abierto bajo licencia Attribution-NonCommercial-ShareAlike 4.0 (CC BY NC SA), la inclusión y difusión del texto completo a través del repositorio institucional de la Universidad Nacional de Colombia y en todas aquellas bases de datos especializadas que el editor considere adecuadas para su indización con miras a incrementar la visibilidad de la revista.
2. Acta Biológica Colombiana permite a los autores archivar, descargar y compartir, la versión final publicada, así como las versiones pre-print y post-print incluyendo un encabezado con la referencia bibliográfica del articulo publicado.
3. Los autores/as podrán adoptar otros acuerdos de licencia no exclusiva de distribución de la versión de la obra publicada (p. ej.: depositarla en un archivo telemático institucional o publicarla en un volumen monográfico) siempre que se indique la publicación inicial en esta revista.
4. Se permite y recomienda a los autores/as difundir su obra a través de Internet (p. ej.: en archivos institucionales, en su página web o en redes sociales cientificas como Academia, Researchgate; Mendelay) lo cual puede producir intercambios interesantes y aumentar las citas de la obra publicada. (Véase El efecto del acceso abierto).