Promoción del crecimiento de Baccharis macrantha (Asteraceae) con bacterias solubilizadoras de fosfatos asociadas a su rizosfera
Growth Promotion of Baccharis macrantha (Asteraceae) by Phosphate Solubilizing Rhizosphere Bacteria
DOI:
https://doi.org/10.15446/abc.v20n3.44742Palabras clave:
Bacillus firmus, Pseudomonas fluorescens, restauración (es)Bacillus firmus, Pseudomonas fluorescens, restoration (en)
El objetivo de esta investigación fue aislar y caracterizar bacterias solubilizadoras de fosfatos (BSF) asociadas a la rizosfera de Baccharis macrantha y Viburnum triphyllum, y evaluar su capacidad para solubilizar fosfatos en condiciones in vitro. Además se determinó el efecto de la inoculaciónde las cepas de BSF más eficientes sobre el crecimiento de B. macrantha. Las muestras de suelo rizosférico de B. macrantha y V. triphyllum fueron colectadas en los meses de mayo-período de lluvia y septiembre-período seco del 2012. Para la cuantificación de bacterias heterótrofas cultivables y BSF se empleó el método de recuento en placa en los medios Agar Tripticasa de Soya y Pikovskaya (PVK) respectivamente. La capacidad de solubilización de fosfatos de las cepas aisladas se estimó a partir del diámetro de los halos formados alrededor de las colonias en el medio de cultivo PVK después de 7 días de incubación a 28 °C. Los ensayos de inoculación en B. macrantha se realizaron con las BSF más eficientes. La inoculación de las BSF B. firmus y P. fluorescens de forma individual y como inoculante combinado mostro un efecto benéfico, incrementando significativamente el porcentaje de germinación de semillas, la altura de la plántula, la longitud de la raíz y el peso seco de B. macrantha. La inoculación de BSF podría ser considerada una estrategia para mejorar el crecimiento y establecimiento de B. macrantha en pastizales abandonados.
The objectives of this research was to isolate and characterize phosphate solubilizing bacteria (BSF) associated to the rhizosphere of Baccharis macrantha and Viburnum triphyllum, and to assess their ability to solubilize phosphate under conditions in vitro. Furthermore to determine the effect of inoculation of the strains BSF more efficient on the growth of B. macrantha. Rhizosphere soil samples of B. macrantha and V. triphyllum were collected in the months of May-rainy season and September-period dry the 2012. Trypticase Soya Agar and Pikovskaya (PVK) were used for quantification of culturable heterotrophic bacteria and BSF, respectively. The phosphate solubilizing capacity of the isolated strains was estimated from the diameter of the halo around the colonies formed in the culture medium PVK after 7 days incubation at 28 °C. Inoculation assays were performed with more efficient BSF in B. macrantha. Inoculation of BSF Bacillus firmus and Pseudomona fluorescens individually and as inoculant combined showed a beneficial effect, significantly increasing the percentage of seed germination, seedling height, root length and dry weight of B . macrantha. Inoculation the BSF could be considered a strategy to improve the growth and development of B. macrantha in abandoned pastures.
Doi: https://doi.org/10.15446/abc.v20n3.44742.
Artículo de investigación/Original research paper
PROMOCIÓN DEL CRECIMIENTO DE Baccharis macrantha (ASTERACEAE) CON BACTERIAS SOLUBILIZADORAS DE FOSFATOS ASOCIADAS A SU RIZOSFERA
Growth Promotion of Baccharis macrantha (Asteraceae) by Phosphate Solubilizing Rhizosphere Bacteria
Elsa Giovanna ÁVILA MARTÍNEZ1, Luz Marina LIZARAZO FORERO1, Francisco CORTÉS PÉREZ2.
1 Grupo de Investigación Biología Ambiental, Escuela de Biología, Universidad Pedagógica y Tecnológica de Colombia. Avenida Central del Norte. Tunja, Colombia.
2 Grupo de Investigación Ecología de Bosques Andinos Colombianos. Universidad Pedagógica y Tecnológica de Colombia. Avenida Central del Norte. Tunja, Colombia.
For correspondence. bio.ambient@uptc.edu.co.
Received: 3rd August 2014, Returned for revision: 1st December 2014, Accepted: 6th January 2015.
Associate Editor: Susana Raquel Feldman.
Citation / Citar este artículo como: Ávila Martínez EG, Lizarazo Forero LM, Cortés Pérez F. Promoción del crecimiento de Baccharis macrantha (Asteraceae) con bacterias solubilizadoras de fosfatos asociadas a su rizosfera. Acta biol. Colomb. 2015;20(3):121-131. doi: https://doi.org/10.15446/abc.v20n3.44742.
RESUMEN
El objetivo de esta investigación fue aislar y caracterizar bacterias solubilizadoras de fosfatos (BSF) asociadas a la rizosfera de Baccharis macrantha y Viburnum triphyllum, y evaluar su capacidad para solubilizar fosfatos en condiciones in vitro. Además se determinó el efecto de la inoculación de las cepas de BSF más eficientes sobre el crecimiento de B. macrantha. Las muestras de suelo rizosférico de B. macrantha y V. triphyllum fueron colectadas en los meses de mayo-período de lluvia y septiembre-período seco del 2012. Para la cuantificación de bacterias heterótrofas cultivables y BSF se empleó el método de recuento en placa en los medios Agar Tripticasa de Soya y Pikovskaya (PVK) respectivamente. La capacidad de solubilización de fosfatos de las cepas aisladas se estimó a partir del diámetro de los halos formados alrededor de las colonias en el medio de cultivo PVK después de 7 días de incubación a 28 °C. Los ensayos de inoculación en B. macrantha se realizaron con las BSF más eficientes. La inoculación de las BSF B. firmusy P. fluorescens de forma individual y como inoculante combinado mostro un efecto benéfico, incrementando significativamente el porcentaje de germinación de semillas, la altura de la plántula, la longitud de la raíz y el peso seco de B. macrantha. La inoculación de BSF podría ser considerada una estrategia para mejorar el crecimiento y establecimiento de B. macrantha en pastizales abandonados.
Palabras clave: Bacillus firmus, Pseudomonas fluorescens, restauración.
ABSTRACT
The objectives of this research was to isolate and characterize phosphate solubilizing bacteria (BSF) associated to the rhizosphere of Baccharis macrantha and Viburnum triphyllum, and to assess their ability to solubilize phosphate under conditions in vitro. Furthermore to determine the effect of inoculation of the strains BSF more efficient on the growth of B. macrantha. Rhizosphere soil samples of B. macrantha and V. triphyllum were collected in the months of May-rainy season and September-period dry the 2012. Trypticase Soya Agar and Pikovskaya (PVK) were used for quantification of culturable heterotrophic bacteria and BSF, respectively. The phosphate solubilizing capacity of the isolated strains was estimated from the diameter of the halo around the colonies formed in the culture medium PVK after 7 days incubation at 28 °C. Inoculation assays were performed with more efficient BSF in B. macrantha. Inoculation of BSF Bacillus firmus and Pseudomona fluorescens individually and as inoculant combined showed a beneficial effect, significantly increasing the percentage of seed germination, seedling height, root length and dry weight of B . macrantha. Inoculation the BSF could be considered a strategy to improve the growth and development of B. macrantha in abandoned pastures.
Keywords: Bacillus firmus, Pseudomonas fluorescens, restoration.
INTRODUCCIÓN
La plantación de arbustos y árboles de especies nativas constituye una de las estrategias más ampliamente utilizadas para la restauración de pastizales abandonados (con dominancia de especies exóticas invasivas) y áreas degradadas (Holl, 2002; Goméz et al., 2004; Vargas, 2011), sin embargo, el éxito del establecimiento de las plantas y la sucesión dependen en gran medida de la disponibilidad de nutrientes en el suelo y por consiguiente de la actividad de las comunidades microbianas que lo habitan.
Uno de los factores limitantes más frecuentes en los procesos de restauración es la baja disponibilidad de nutrientes presentes en el suelo, de esta manera las plantas introducidas no se pueden establecer con facilidad, presentando bajas tasas de crecimiento y altos niveles de mortalidad. Adicionalmente, los suelo donde se llevan a cabo los planes de revegetación se caracterizan por ser suelos degradados donde las poblaciones de microorganismos benéficos que establecen relaciones simbióticas con las plantas están muy disminuidas (Barreto et al., 2007; Franco y García, 2012), como consecuencia al realizar planes de restauración se siembran plantas sin los microorganismos que pueden ayudar a su desarrollo y fácil adaptación al suelo. Por tal razón, una de las alternativas que se puede desarrollar para contribuir en la consolidación de los planes de restauración en suelos deteriorados consiste en incrementar la abundancia de microorganismos que establecen asociaciones benéficas con las especies vegetales introducidas (Matias et al., 2009).
Se realizaron plantaciones experimentales con especies nativas como Baccharis macrantha Kunth y Viburnum tryphyllum Bentham en pastizales abandonados del municipio de Arcabuco, no obstante, el establecimiento de las plantas estuvo limitado en gran medida por la deficiencia de nutrientes principalmente de fósforo (Cortés-Pérez F. Obs. Pers.).
Aunque el P es uno de los macronutrientes esenciales para el crecimiento y desarrollo de las plantas, es el segundo elemento más limitante para el establecimiento y producción de biomasa tanto en ecosistemas naturales como en sistemas bajo manejo antrópico (Hinsinger, 2001; Gyaneshwar et al., 2002; Khan et al., 2007; Richardson y Simpson, 2011). La baja disponibilidad de P en los suelos tropicales se debe a que estos además de ser deficientes en P, son extremadamente ácidos y tienen una fuerte capacidad para fijar P en forma de fosfatos insolubles de hierro y aluminio (Rodríguez y Fraga, 1999; Khan et al., 2007).
Este evento conduce a la necesidad de aplicaciones repetidas y excesivas de fertilizantes fosfatados solubles, que además de las limitaciones económicas debido a sus altos costos, pueden conducir a problemas ambientales tales como la eutrofización del ecosistemas acuáticos, la salinidad del suelo (Correll, 1998; Del Campillo et al., 1999) y a la acumulación en el suelo de elementos tóxicos presentes en los fertilizantes (Yamazaki y Geraldo, 2003).
Las bacterias que se encuentran colonizando las raíces de las plantas son denominadas comúnmente como Rizobacterias Promotoras del Crecimiento Vegetal (PGPRs), definidas por Kloepper (1993). Estas bacterias de vida libre presentes en el suelo, capaces de adaptarse, colonizar y persistir en la rizósfera de las especies de plantas que están presentes en la mayoría de los ambientes (Compant et al., 2005), se encuentran ampliamente representadas en cuanto a géneros microbianos. Las PGPRs estimulan el crecimiento de las plantas a través de una compleja mezcla de diferentes mecanismos, que pueden incluir fijación del nitrógeno, producción de sideróforos, síntesis y liberación de fitohormonas, modulación de los niveles de etileno de las plantas y servir como control biológico de fitopatógenos (Fulchieri et al., 1993; Bashan y Holguin, 1998; Cassán et al., 2001a; Cassán et al., 2001b; Richardson et al., 2009). Otros mecanismos que se han propuesto, es el incremento de la captación del agua y minerales, como convertir formas insolubles de P, a formas solubles que pueden ser fácilmente tomada por la raíces de las plantas (Gray y Smith, 2005; Ivanova et al., 2006; Khan et al., 2007; Richardson y Simpson, 2011). Además muchas de estas bacterias tienen la capacidad de trascender las barreras de la endodermis, atravesar la corteza de la raíz hasta el sistema vascular y, como consecuencia, vivir como endófitos en tallos, hojas, tubérculos y otros órganos (Zinniel et al., 2002; Compant et al., 2005) sin causar daño a la planta.
Uno de los mecanismos más ampliamente estudiados en las PGPRs es la liberación de ácidos orgánicos de bajo peso molecular, estos ácidos a través de sus grupos hidroxilo y carboxilo quelan los cationes ligados a fosfatos, liberando iones de ortofosfato (H2PO4-1 y HPO3-2), los cuales son fácilmente absorbidos por las raíces de las plantas (Chen et al., 2006; Paredes-Mendoza y Espinosa-Victoria, 2010).
Las bacterias solubilizadoras de fosfatos (BSF) son vitales para el ciclo del P en el suelo y algunas de ellas pueden ser empleadas para aumentar la disponibilidad de este elemento (Richardson y Simpson, 2011). Por ejemplo, en varios trabajos se ha reportado que la inoculación de microorganismos solubilizadores de P en diferentes especies forestales, además de estimular el crecimiento de las plantas en términos de altura, longitud de las raíces y biomasa, ayudan al establecimiento de las mismas en suelos deficientes en P (Galindo et al., 2006; Ramos et al., 2007; Matias et al., 2009).
En este contexto, los objetivos del presente trabajo fueron aislar y caracterizar BSF asociadas a la rizosfera de B. macrantha y V. triphyllum y evaluar su capacidad para solubilizar fosfatos en condiciones de invernadero, determinando el efecto de la inoculación de las cepas de BSF más eficientes sobre el crecimiento de B. macrantha.
MATERIALES Y MÉTODOS
Área de estudio y toma de muestras
Se trabajó un lote experimental de Ecología de la Restauración plantado con Baccharis macrantha y Viburnum triphyllum en el año 2008, ubicado en la vereda Peñas Blancas del municipio de Arcabuco-Boyacá. Los suelos del área de estudio se caracterizan por presentar un bajo contenido de P disponible (2,4 ppm), pH fuertemente ácido (4,8) y por contener una alta concentración de aluminio (1,56 cmol kg-1) según un análisis de caracterización físico-química de suelos realizados en el año 2010 (Cortés-Pérez F. Obs. Pers.).
Se tomaron 32 muestras (16 de suelo rizosférico de B. macrantha y 16 de V. triphyllum), en dos diferentes períodos climáticos (ocho muestras por especie en cada período climático) correspondientes a los meses de mayo (período de lluvia con precipitación media mensual de 128,3 mm) y septiembre (período seco con precipitación media mensual de 39,9 mm) del 2012.
Se recogieron muestras de suelo rizosférico, adherido a las raíces de cada una de las plantas, cada una de 50 g, para conformar una muestra integrada de 1 kg, que se depositaron en bolsas plásticas estéril sellopack y se refrigeraron hasta el momento de su análisis.
Cuantificación de bacterias heterótrofas cultivables y bacterias solubilizadoras de fosfatos
A partir de las muestras de suelo se realizaron diluciones seriadas hasta 10-4, y se inoculó 0,1 mL por duplicado en los medios de cultivo Agar Tripticasa de Soya -ATS- y Agar Pikovskaya -PVK- (empleando como fuente de P fosfato tricálcico-Ca3(PO4)2 5g L-1, Pikovskaya, 1948). Los medios de cultivos ATS y PVK se incubaron a 28°C por 24 h y siete días respectivamente.
Posteriormente, se realizó la cuantificación de las colonias, las cuales fueron expresadas en términos de unidades formadoras de colonia/g suelo (UFC/g de suelo). El recuento de BSF, se realizó por conteo de las colonias que formaron halo de solubilización en el medio PVK.
Con el fin de determinar la producción de ácidos orgánicos relacionados con la solubilización de fosfatos, las colonias con halos de solubilización en el medio de cultivo PVK, fueron repicadas al medio Agar Sandar-Rao y Shina -SRSM-1- (este medio contiene la misma composición del medio PVK pero suplementado con 0,1 g/L de purpura de bromocresol, como indicador de pH, Sandar-Rao y Shina, 1963).
Caracterización de las bacterias solubilizadoras de fosfatos
Las colonias que formaron halo de solubilización en el medio de cultivo PVK, fueron aisladas y caracterizadas macroscópicamente con base a la pigmentación, borde y elevación. La identificación microscópica se realizó mediante tinción de Gram; adicionalmente se realizó coloración de verde de malaquita para comprobar presencia de esporas y coloración de rojo congo para determinar bacterias formadoras de cápsula.
Pruebas de identificación a los morfotipos seleccionados
Las colonias seleccionadas según morfología macro y microscópica se cultivaron en los medios selectivos y diferenciales EMB (Pronadisa)®, agar McConkey (Pronadisa)®, King B (Pronadisa)®, Manitol (Pronadisa)®. Para los microorganismos escogidos a partir de los medios selectivos, se realizaron pruebas bioquímicas convencionales, como catalasa y comerciales, para el caso de las formas bacilares Gram negativas se usó oxidasa (BioMérieux®), los kit de identificación API 20E (Enterobacterias-BioMérieux®) y API 20NE (no Enterobacterias-BioMérieux®), por otro lado, las bacterias Gram positivas, se sembraron en las pruebas BBL CrystalTM. Luego de la lectura de las reacciones producidas, espontáneas o reveladas mediante la adición de reactivos, se llevó a cabo el registro manual de los datos para su posterior incorporación al software APIWEB (bioMérieux). Los resultados obtenidos fueron informados de acuerdo a los criterios establecidos por el fabricante, considerando un resultado como válido cuando el porcentaje de identificación fue de al menos 90 %.
Capacidad de solubilización de fosfatos in vitro
La capacidad de solubilización de fosfatos de las cepas aisladas se estimó a partir del diámetro de los halos formados alrededor de las colonias en el medio de cultivo PVK después de siete días de incubación a 28 °C. Se consideró como diámetro total a la distancia de extremo a extremo del halo de solubilización incluida la colonia y como diámetro del halo de solubilización (h) a la diferencia entre el diámetro total y el diámetro de la colonia. Así, las cepas aisladas fueron agrupadas según el h en cuatro categorías, 1: h >0-2 mm, 2: h >2-4, 3: h >4-6, 4: h >6.
El índice de solubilización de fosfatos (IS), se calculó como la relación entre el diámetro total y el diámetro de la colonia (Premono etal., 1996; Ramachandran etal., 2007; Khan et al., 2010). El IS de cada una de las bacterias asociadas a la rizosfera de B. macrantha y V. triphyllum corresponde al promedio de cinco colonias.
Ensayos de inoculación en B. macrantha
El aislamiento de bacterias solubilizadoras de fosfatos (BSF), se realizó a partir de suelo rizosférico de B. macrantha y V. triphyllum, sin embargo, los ensayos de inoculación solamente se llevaron a cabo en semillas de B. macrantha, debido a que no fue posible obtener semillas de V. triphyllum por el estado fenológico en el que se encontraba la planta en el período en el que se realizó el ensayo.
El experimento se estableció en un invernadero ubicado en instalaciones de la Universidad Pedagógica y Tecnológica de Colombia en la ciudad Tunja, a una temperatura promedio de 13,2 °C y 2810 m s. n. m.
Preparación de los inoculantes
Las dos cepas que presentaron mayor IS en condiciones in vitro fueron identificadas mediante pruebas bioquímicas comerciales como Bacillus firmus y Pseudomonas fluorescens. Cultivos de las dos cepas con 24 h de crecimiento en ATS fueron repicados en caldo Luria Bertani (LB), e incubados hasta obtener una densidad de 108 UFC/mL. La suspención B. firmus y P. fluorescens se ajustó una absorbancia de 1,0 a 600 nm y de 0,1 a 600 nm respectivamente.
Para producir un inoculante combinado (B. firmus + P. fluorescens), previamente se realizaron pruebas de compatibilidad, mediante la técnica de enfrentamiento dual que consiste en trazar en una caja de ATS una estría de una de las cepas a enfrentar, mientras que la otra cepa a examinar es sembrada perpendicularmente con respecto al cultivo inicial. A continuación las cajas fueron puestas en incubación a 30 °C por 48 h (Mittal et al., 2008). Al final del período de incubación no se formaron zonas de inhibición de crecimiento entre las dos cepas.
Parámetros de crecimiento
El diseño del experimento correspondió a un diseño completamente al azar con cuatro tratamientos, cada uno con 36 réplicas. Los tratamientos aplicados correspondieron a: (1) suelo estéril + semillas de B. macrantha inoculadas con B. firmus; (2) suelo estéril + semillas de B. macrantha inoculadas con P. fluorescens; (3) suelo estéril + semillas de B. macrantha inoculadas con B. firmus + P. fluorescens (inoculante combinado); (4-Control): suelo no estéril + semillas de B. macrantha sin ningún tipo de tratamiento, y por último (Control-caldo LB): semillas de B. macrantha en caldo Luria Bertani (con el fin de observar posibles efectos del medio de cultivo en las semillas).
Como sustrato para la germinación de las semillas se utilizó suelo estéril (autoclavado durante tres ciclos a 121°C, 15 lb presión durante 15 minutos) proveniente del área de estudio. Los pozos de las bandejas de germinación previamente desinfectados con alcohol al 70 %, fueron rellenados con aproximadamente 35 g de suelo estéril (para los tratamientos 1, 2 y 3) y suelo no estéril (para el tratamiento 4-control).
Semillas de B. macrantha superficialmente higienizadas, se sumergieron en 30 mL de cada uno de los inoculantes bacterianos (B. firmus, P. fluorescens e inoculante combinado) durante 60 minutos a 30 °C (Farina et al., 2012). A continuación, en cada uno de los pozos se sembró un grupo semillas (100) a 5 mm de profundidad. El porcentaje de germinación de las semillas para cada tratamiento se registró semanalmente hasta los 72 días.
Cincuenta días después de realizada la siembra se escogieron seis plántulas por tratamiento, debido a que ese era el número de individuos para el tratamiento control y con el fin de realizar observaciones para igual número de individuos en los otros tratamientos, además de evitar competencia entre las plántulas debido al alto número de individuos por cada pozo (Barreto et al., 2007; Ogata et al., 2008).
Después de dos meses y medio, por cada tratamiento fueron colectadas al azar 72 plántulas (dos plántulas por cada una de las réplicas de cada uno de los tratamientos). La raíz de las plántulas fue lavada con agua de grifo para retirar el suelo, registrándose la altura de las plántulas y la longitud de la raíz principal. Posteriormente, el material fue secado a 60 °C por 24 h e inmediatamente se determinó el peso seco (Mohan y Radhakrishnan, 2012; Yu et al., 2012; Dash et al., 2013).
Análisis estadístico
Todos los datos obtenidos fueron analizados estadísticamente con el software PASW Statistics 18 (SPSS Inc, 2013), empleando análisis de varianza (ANDEVA) para establecer diferencias estadísticamente significativas. La comparación de medias se llevó a cabo mediante la prueba de rango múltiple de Duncan, con un nivel de significancia de 0,05.
RESULTADOS
Cuantificación de bacterias heterótrofas cultivables y bacterias solubilizadoras de fosfatos
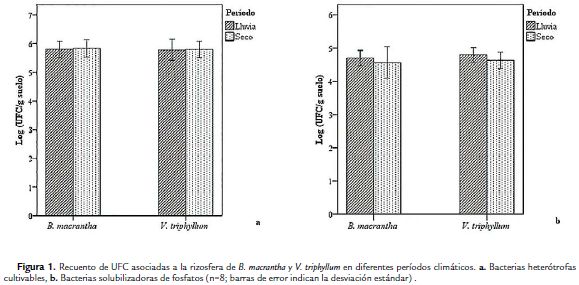
El mayor número de bacterias heterótrofas cultivables (BHC) se presentó en el período seco con un promedio de 7,1 x 105 (±2 x 105) y 6,5 x 105 (±1,8 x 105) UFC/g de suelo para B. macrantha y V. triphyllum respectivamente. No presentándose diferencias estadísticamente significativas entre el número de BHC (UFC/g de suelo) aisladas para B. macrantha y V. triphyllum en los dos períodos climáticos (p = 0,924; Fig. 1a).
Como se indica en la Fig. 1b, el mayor número de bacterias solubilizadoras de fosfatos (BSF) aisladas para B. macrantha y V. triphyllum se presentó en el período de lluvia con un promedio de 5,5 x 104 (±2,3 x 104) y 6,9 x 104 (±3,6 x 104) UFC/g de suelo respectivamente. Sin embargo, no se presentaron diferencias estadísticamente significativas entre el número de BSF (UFC/g de suelo) aisladas de la rizosfera de B. macrantha y V. triphyllum en los dos períodos climáticos (p = 0,595).
El porcentaje de BSF con respecto a las BHC fue del 7,45 % para B. macrantha y de 9,26 % para V. triphyllum.
Caracterización de las bacterias solubilizadoras de fosfatos
La caracterización microscópica de las colonias mostró que la mayoría de las bacterias aisladas correspondieron a bacilos Gram negativos, aislándose en menor proporción bacilos y cocos Gram positivos.
De la totalidad de BSF aisladas para la rizosfera de B. macrantha en el período de lluvia, el 77,53 % de colonias aisladas correspondió a bacilos Gram negativos, el 13,48 % a bacilos Gram positivos no formadores de espora y el 8,99 % restante correspondió a bacilos Gram positivos esporoformadores. En cuanto a las cepas aisladas en período seco, el 71,76 % de estas correspondió a bacilos Gram negativos, el 14,12 % a bacilos Gram positivos no formadores de espora y el 14,12 % restante correspondió a bacilos Gram positivos esporulados.
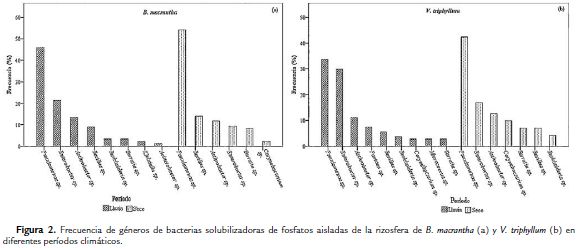
Las BSF aisladas de muestras de rizosfera de B. macrantha, tomadas en período de lluvia se identificaron dentro de ocho géneros, entre los cuales, Pseudomonas fue el más abundante con 46,06 %, seguido por Enterobacter con 21,34 % del total de las cepas bacterianas fosfato-solubilizadoras aisladas. Por otro lado, las BSF aisladas de las muestras de rizosfera tomadas en período seco se identificaron en seis géneros, donde nuevamente Pseudomonas fue uno de los géneros más representativos con un 54,11 %, seguido por Bacillus con 14,11 % del total de las cepas de BSF aisladas. Otros géneros como Acinetobacter, Burkholderia y Klebsiella además de presentar baja frecuencia, se reportaron solamente para la rizosfera de B. macrantha en el período de lluvia (Fig. 2a).
Por otro lado, de la totalidad de BSF aisladas para la rizosfera de V. triphyllum en el período de lluvia, el 77,57 % de las bacterias aisladas correspondió a bacilos Gram negativos, el 14,02 % a bacilos Gram positivos no formadores de espora y el 5,61 % de las bacterias aisladas fueron bacilos Gram positivos esporoformadores, para este caso también se aislaron cocos Gram positivos (2,8 %). En cuanto al período seco, el 70,42 % de las cepas aisladas fueron bacilos Gram negativos, el 22,54 % correspondió a bacilos Gram positivos no formadores de espora y el 7,04 % restante correspondió a bacilos Gram positivos esporulados.
Las BSF aisladas de muestras de rizosfera de V. triphyllum tomadas en período de lluvia se identificaron nueve géneros, entre los cuales, Pseudomonas fue el más abundante con 33,64 %, seguido por Enterobacter con 29,90 % del total de las colonias bacterianas fosfato-solubilizadoras aisladas. De igual manera, para las muestras de rizosfera tomadas en período seco, los géneros bacterianos más abundantes fueron Pseudomonas (42,25 %) y Enterobacter (16,90 %). Otros géneros como Pantoea y Micrococcus, además de presentar baja frecuencia, solamente se registraron para la rizosfera de V. triphyllum en el período de lluvia (Fig. 2b).
Capacidad de solubilización de fosfatos in vitro
Las colonias de BSF que se aislaron en el medio de cultivo PVK, formaron zonas de solubilización. Para la rizosfera de B. macrantha se clasificaron 174 cepas bacterianas de acuerdo al diámetro de su halo de solubilización. La mayoría de las bacterias aisladas (114) formaron halos de solubilización con diámetro entre >0-2 mm, mientras solo seis de las cepas aisladas se clasificaron en el categoría cuatro (halos con diámetro >6 mm); 43 cepas aisladas formaron halos de solubilización con diámetro entre >2-4 mm y las 11 cepas restantes formaron halos de solubilización entre los >4-6 mm.
Por otro lado, para la rizosfera de V. triphyllum se clasificaron en total 178 cepas bacterianas de acuerdo al diámetro del halo de solubilización, de las cuales 124 formaron halos de solubilización con diámetro entre >0-2 mm, 49 de las cepas aisladas formaron halos de solubilización entre >2-4 mm y cinco presentaron halos de solubilización con diámetro entre >4-6 mm. En este caso no se registraron colonias bacterianas con diámetro del halo de solubilización superior a 6 mm.
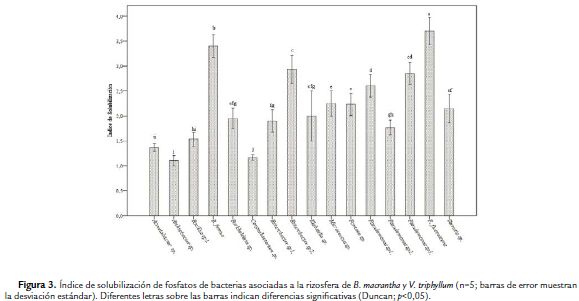
Tal como se muestra en la Fig. 3, las bacterias aisladas presentaron IS que variaron entre 1,1 (±0,1) y 3,7 (±0,27). Los bacterias que presentaron mayor IS se identificaron como B. firmus (IS: 3,4) y P. fluorescens (IS: 3,7; Fig. 3). Estas dos bacterias se subcultivaron y posteriormente se emplearon en el ensayo de inoculación en B. macrantha. En general, se observó que los IS más grandes se produjeron por bacterias Gram negativas.
En relación con las bacterias inoculadas en el medio SRSM-1, todas produjeron acidificación, lo que indica que las bacterias aisladas tienen la capacidad de producir ácidos orgánicos.
Ensayos de inoculación en B. macrantha
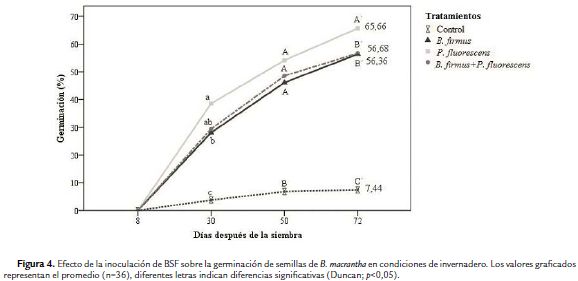
Los porcentajes de germinación de semillas de B. macrantha fueron mayores cuando estas fueron inoculadas con los tratamientos bacterianos, alcanzado valores superiores al 50 % de germinación (65, 56 y 56 % para P. fluorescens, B. firmus + P. fluorescens y B. firmus respectivamente), en tanto que el control tan solo alcanzó el 7 % de germinación (Fig. 4).
Después de 72 días de haberse inoculado y sembrado semillas de B. macrantha, se observaron diferencias estadisticamente significativas en la altura promedio de las plántulas germinadas de semillas inoculadas con B. firmus, P. fluorescens y B. firmus + P. fluorescens, en comparación con la altura promedio de las plántulas obtenidas en el tratamiento control (p = 0,0001).
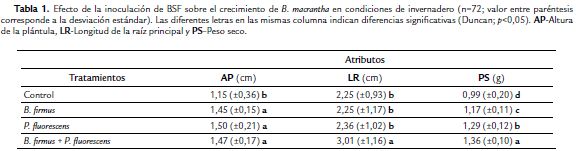
Los valores máximos de altura de las plántulas de B. macrantha se obtuvieron con inoculación de P. fluorescens, seguido por B. firmus y B. firmus + P. fluorescens. No encontrándose diferencias estadísticamente significativas entre la atura promedio de las plántulas para los tres tratamientos (Tabla 1).
La longitud de la raíz principal fue afectada en gran medida por la inoculación de B. firmus + P. fluorescens, donde se registró la máxima longitud.
Para el peso seco el valor más sobresaliente se reportó con la inoculación de B. firmus + P. fluorescens el cual fue estadísticamente superior a los tratamientos donde hubo inoculación de las dos BSF (B. firmus y P. fluorescens) de forma individual (p = 0,0001; Tabla 1).
En el control de semillas de B. macrantha en caldo LB no se observó germinación.
DISCUSIÓN
Cuantificación de bacterias heterótrofas cultivables y bacterias solubilizadoras de fosfatos
Las bacterias solubilizadoras de fosfatos (BSF) asociadas a la rizosfera de B. macrantha y V. triphyllum estuvieron representadas por menos del 10 % en relación a las bacterias heterótrofas cultivables. Al respecto Santa-Regina et al.(2007), Lara et al. (2011) y Azziz et al. (2012), registraron porcentajes de aislamiento entre el 8 y 15 % en cultivos de avena, sorgo y terrenos colonizados por especies nativas y pastizales de carretón y raigrás. En contraste, Martínez-Nieto y García-González (2010), Farina et al. (2012) y Muleta et al. (2013), encontraron que las poblaciones de BSF estuvieron representadas por el 30 % del total de las bacterias asociadas a la rizosfera de plantas de canola (Brasica napus Linneo), encenillo (Weinmannia tomentosa Linneo f) y café (Coffea arabica Linneo).
Caracterización de las bacterias solubilizadoras de fosfatosz
La mayoría de las BSF asociadas a la rizosfera de B. macrantha y V. triphyllum correspondieron a bacilos Gram negativos. Esto es coherente con lo reportado por Martínez-Nieto y García-González (2010) y Lara et al. (2011), quienes señalaron que las poblaciones de BSF relacionadas a la rizosfera de guayaba agria (Psidium araca Swartz) y encenillo, eran predominantemente bacilos Gram negativos.
Otros morfotipos aislados en menor proporción de la rizosfera de B. macrantha y V. triphyllum correspondieron a bacilos y cocos Gram positivos. Lara et al. (2011), reportaron bacilos y cocos Gram positivos en un 5 % y 2 % respectivamente, del total de las BSF asociadas a la rizosfera de árboles de guayaba agria.
Los géneros fosfatosolubilizadores más frecuentes en los dos períodos climáticos para las dos especies de plantas, correspondieron a Pseudomonas sp., Enterobacter sp. y Bacillus sp. Resultados similares son reportados por Muleta et al. (2013), quienes encontraron que Pseudomonas y Bacillus, fueron las BSF más abundantes en la rizosfera de plantas de café que crecían en bosques naturales.
Las BSF de los géneros Acinetobacter sp., y Klebsiella sp., solo se aislaron de la rizosfera de B. macrantha. Por su parte, Pantoea sp. y Micrococcus sp., se aislaron exclusivamente de la rizosfera de V. triphyllum. Autores como Houlden et al. (2008), Dunfield y Germida (2003), Santa-Regina et al. (2007), Farina et al. (2012), reportan que la composición, incidencia y distribución de la comunidad microbiana en la rizosfera es influenciada por muchos factores. Así, patrones de exudación de la raíz que varía durante el ciclo de vida de las plantas y cambios en variables ambientales como la precipitación y la temperatura cambian la composición de la comunidad microbiana.
Adicionalmente, la rizodeposición de nutrientes por parte de las raíces de las plantas es otro de los aspectos determinantes de la diversidad bacteriana, debido a que diferentes especies de plantas crean condiciones desiguales principalmente a través de sus exudados (Smalla et al., 2001; Houlden et al., 2008).
Capacidad de solubilización de fosfatos in vitro
La mayoría de bacterias aisladas formaron halos de solubilización con diámetro inferior a 2 mm. Resultados similares son reportados por Azziz et al. (2012). Contrario a lo reportado por Gupta et al. (2010), et al. (2012), Yu et al. (2012) y Muleta et al. (2013), quienes encontraron que la mayoría de las BSF asociadas a la rizosfera de plantas café y stevia (Stevia rebaudiana Bertoni) formaron halos de solubilización de fosfatos con diámetro superior a los 5 mm después de cinco días de incubación en medio PVK.
El índice de solubilización de fosfatos (IS) de las bacterias asociadas a la rizosfera de B. macrantha y V. triphyllum osciló entre 1,1 a 3,7. Las dos cepas bacterianas que presentaron mayor IS de fosfatos correspondieron a P. fluorescens y B. firmus. Estos resultados concuerdan con los mostrados por Lara et al. (2011), Yu et al. (2012) y Muleta et al. (2013) quienes reportan rizobacterias solubilizadoras de fosfatos con IS entre un rango de 1,25 a 5,82, e indican que en general las cepas Gram negativas presentaron los IS más altos, siendo Pseudomonas el de mayor tamaño halos de solubilización. Adicionalmente, Muleta et al. (2013), reportan que todos las bacterias Gram negativas que aisló tienen la capacidad de producir ácidos orgánicos, principalmente los ácido 2-cetoglucónico y glucónico, lo que explica la mayor capacidad de solubilización de P de las bacterias Gram negativas en comparación con las bacterias Gram positivas.
Las BSF crearon zonas de acidificación en el medio SRSM-1, lo que indica la producción de ácidos orgánicos por parte de los aislamientos. Varios autores señalan que la secreción de ácidos orgánicos es uno de los mecanismos esenciales para la solubilización de fosfatos minerales insolubles (Ca3 (PO4)2, roca fosfórica, entre otros compuestos) por parte de las bacterias. Sin embargo, aclaran que no es el único mecanismo involucrado en este proceso (Illmer y Schinner, 1995; Chen et al., 2006; Muleta et al., 2013). Entre los ácidos orgánicos, la producción de los ácidos 2-cetoglucónico y glucónico por los géneros bacterianos Bacillus y Pseudomonas, es el mecanismo más frecuentemente descrito en la literatura como responsable de la solubilización de fosfatos (Chen et al., 2006; Paredes-Mendoza y Espinosa-Victoria, 2010; Muleta et al., 2013).
Ensayos de inoculación en B. macrantha
El incremento más significativo en los parámetros de crecimiento evaluados para B. macrantha se presentó con la aplicación del inoculante combinado de las BSF en comparación con los resultados obtenidos en los tratamientos donde se inocularon BSF de forma individual. La estimulación de la germinación de semillas, el incremento de la altura de las plántulas y el mayor desarrollo de las raíces de B. macrantha por la inoculación de B. firmus y P. fluorescens, puede ser explicado por la capacidad de estas bacterias para producir sustancias promotoras del crecimiento de las plantas como el ácido indolacético (AIA), cuya principal función es la de estimular la germinación de las semillas, acelerar el crecimiento de las plantas especialmente en sus primeros estadios, inducir la iniciación radicular e incrementar la formación de raíces y pelos radicales (Khalid et al., 2003; Khalid et al., 2004).
Es importante resaltar que el buen desarrollo del sistema radical de plántulas de B. macrantha obtenidas de semillas inoculadas con BSF, podría indicar una mayor probabilidad del establecimiento de las plántulas en condiciones de campo (suelos deficientes en P y otros nutrientes), debido a la mayor área de contacto para la absorción de los nutrientes. Con respecto a esto, Galindo et al. (2006), Ramos et al. (2007) y Matias et al. (2009), Gupta et al. (2010), Gupta et al. (2012) y Muleta et al. (2013), señalan que la inoculación de microorganismos solubilizadores de P en plantas y semillas de especies forestales, además de incrementar significativamente el crecimiento de la planta en términos de altura, peso seco y contenido de P en las diferentes estructuras de la planta, también reduce el índice de mortalidad de las mismas cuando son trasplantadas a campo.
Adicionalmente, Barreto et al. (2007), Farina et al. (2012), Yu et al. (2012) y Dash et al. (2013), señalan que los resultados positivos sobre el crecimiento de las raíces y el aumento del peso seco de tallos y raíces de las plántulas, pueden ser debidos a la habilidad de las cepas bacterianas para solubilizar fosfatos, aunque no afirman que este haya sido el único o principal mecanismo responsable de una respuesta positiva en el crecimiento.
Otras características de las PGPRs, como la producción de sideróforos, la fijación biológica del nitrógeno y la presencia de actividad ACC deaminasa, para reducir la producción de etileno, que aunque no fueron evaluadas para las cepas aisladas en este trabajo, podrían explicar parte de los resultados obtenidos. El género Pseudomonas, ha sido ampliamente estudiado por su capacidad para fijar nitrógeno, sintetizar componentes indólicos y producir sideróforos (Jha et al., 2009; Farina et al., 2012; Mohan y Radhakrishnan, 2012). Otro género bacteriano reconocido por su actividad PGPR es Bacillus, además de su capacidad para solubilizar P, algunas cepas son comúnmente productoras de sideróforos (Ribeiro y Nogueira, 2012).
CONCLUSIONES
La inoculación de las cepas de BSF B. firmus y P. fluorescens de forma individual y como inoculante combinado mostró un efecto benéfico, incrementando significativamente el porcentaje de germinación de semillas, la altura de plántulas, la longitud de las raíces y el peso seco total de B. macrantha. La inoculación de estas BSF puede ser una opción alternativa para la movilización de compuestos fosfatados insolubles que se encuentran presentes en el suelo. Sin embargo, es necesario realizar estudios posteriores para evaluar los efectos de estas cepas bacterianas en condiciones de campo.
AGRADECIMIENTOS
Los autores del trabajo expresan un agradecimiento muy especial a la Dirección de Investigaciones de la Universidad Pedagógica y Tecnológica de Colombia, por el aporte de los recursos con los cuales se financiaron las diferentes actividades experimentales del trabajo y al biólogo Daniel Galindo por su accesoria en el manejo estadístico de los datos.
REFERENCIAS
Azziz G, Bajsa N, Haghjou T, Taulé C, Valverde A, Igual JM, et al. Abundance, diversity and prospecting of culturable phosphate solubilizing bacteria on soils under crop-pasture rotations in a no-tillage regime in Uruguay. Appl Soil Ecol. 2012;61:320-326. Doi: 10.1016/j. apsoil.2011.10.004.
Barreto D, Valero N, Muñoz A, Peralta A. Efecto de microorganismos rizosféricos sobre germinación y crecimiento temprano de Anacardium excelsum. Zonas Áridas. 2007;11(1):240-250.
Bashan Y, Holguin G. Proposal for the division of Plant Growth-Promoting Rhizobacteria into two classification: biocontrol-PGPB (Plant Growth-Promoting Bacteria) and PGPB. Soil Biol Biochem. 1998;30(8):1225-1228. Doi: 10.1016/S0038-0717(97)00187-9.
Cassán F, Bottini R, Schneider G, Piccoli P. Azospirillum brasilense and Azospirillum lipoferum hydrolyze conjugates of GA20 and metabolize the resultant aglycone to GA1 in seedlings of rice dwarf mutants. Plant Physiol. 2001a;125(4):2053-2058. Doi: 10.1104/pp.125.4.2053.
Cassán F, Lucangeli C, Bottini R, Piccoli P. Azospirillum sp. metabolize [17, 17-2H2] gibberellin A20 to [17,17-2H2] Gibberellin A1 in vivo in dy rice mutant seedlings. Plant Cell Physiol. 2001b;42(7):763-767.
Chen YP, Rekha PD, Arun AB, Shen FT, Lai WA, Young CC. Phosphate solubilizing bacteria from subtropical soil and their tricalcium phosphate solubilizing abilities. Appl Soil Ecol. 2006;34(1):33-41. Doi: 10.1016/j.apsoil.2005.12.002.
Compant S, Reiter B, Sessitsch A, Nowak J, Clément C, Barka A. Endophytic colonization of Vitis vinifera L. by a plant groth-promoting bacterium, Burkholderia sp. Strain PsJN. Appl Environ Microbiol. 2005;71(4):1685-1693. Doi: 10.1128/AEM.71.4.1685-1693.2005.
Correll DL. The role of phosphorus in the eutrophication of receiving waters: a review.J Environ Qual. 1998;27(2):261-266. Doi: 10.2134/jeq1998.00472425002700020004x.
Dash S, Kumar A, Gupta N. Growth response of Dalbergia sissoo Roxb. to mineral solubilizing bacteria and fungi in nursery conditions. Trop Ecol. 2013;54(1):109-115.
Del Campillo SE, Van Der Zee S, Torrent J. Modelling long term phosphorus leaching and changes in phosphorus fertility in excessively fertilized acid sandy soils. Eur J Soil Sci. 1999;50(3):391-399. Doi: 10.1046/j.1365-2389.1999.00244.x.
Dunfield KE, Germida JJ. Seasonal changes in the rhizosphere microbial communities associated with field grown genetically modified canola (Brassica napus). Appl Environ Microbiol. 2003;69(12):7310-7318. Doi: 10.1128/ AEM.69.12.7310-7318.2003.
Farina R, Beneduzi A, Ambrosini A, Campos SB, Brito B, Wendisch V, et al. Diversity of plant growth-promoting rhizobacteria communities associated with the stages of canola growth. Appl Soil Ecol. 2012;55:44-52. Doi: 10.1016/j.apsoil.2011.12.011.
Franco LA, García MR. Caracterización de las endomicorrizas y siete grupos de microorganismos en agrosistemas del Piedemonte Amazónico, Colombia. Acta Biol Colomb. 2012;17(2):349-362.
Fulchieri M, Lucangeli C, Bottini R. Inoculation with Azospirillum lipoferum affects growth and gibberellin status of corn seedling roots. Plant Cell Physiol. 1993;34(8):1305-1309.
Galindo T, Polanía J, Sánchez J, Moreno N, Vanegas J, Holguín G. Efecto de inoculantes microbianos sobre la promoción de crecimiento de plántulas de mangle y plantas de Citrullus vulgaris San Andrés Isla, Colombia. Acta biol Colomb. 2006;11(1):83-97.
Gómez L, Zamora R, Gómez J, Hodar J, Castro J, Baraza E. Applying plant facilitation to forest restoration: A meta-análisis of the use of shrubs as nurse plants. Ecol Appl. 2004;14(4):1128-1138. Doi: 10.1890/03-5084.
Gray EJ, Smith DL. Intracellular and extracellular PGPR: commonalities and distinctions in the plant-bacterium signaling processes. Soil Biol Biochem. 2005;37(3):395-412. Doi: 10.1016/j.soilbio.2004.08.030.
Gupta M, Rahi P, Phatania V, Gulati A, Singh B, Kumar-Bhanwra R, et al. Stimulatory effect of phosphate-solubilizing bacteria on plant growth, stevioside and rebaudioside-A contents of Stevia rebaudiana Bertoni. Appl Soil Ecol. 2010;46(2):222-229. Doi: 10.1016/j.apsoil.2010.08.008.
Gupta M, Kiran S, Gulati A, Singh B, Tewari R. Isolation and identification of phosphate solubilizing bacteria able to enhance the growth and aloin-A biosynthesis of Aloebarbadensis Miller. Microbiol Res. 2012;167(6):358-363. Doi: 10.1016/j.micres.2012.02.004.
Gyaneshwar P, Naresh-Kumar GN, Parekh LJ, Poole PS. Role of microorganisms in improving P nutrient of plants. Plant Soil. 2002;245(1):83-93. Doi: 10.1007/978-94-017-1570-6_15.
Hinsinger P. Bioavailability of soil inorganic P in the rhizosphere as affected by root-induced chemical changes: a review. Plant Soil. 2001;237(2):173-195. Doi: 10.1023/A:1013351617532.
Holl KD. Effect of shrubs on tree seedling establishment in an abandoned tropical pasture. J Ecol. 2002;90(1):179-187. Doi: 10.1046/j.0022-0477.2001.00637.x.
Houlden A, Timms-Wilson TM, Day MJ, Bailey MJ. Influence of plant developmental stage on microbial community structure and activity in the rhizosphere of three field crops. FEMS Microbiol Ecol. 2008;65(2):193-201. Doi: 10.1111/j.1574-6941.2008.00535.x.
Illmer P, Schinner F. Solubilization of inorganic calcium phosphates-solubilization mechanisms. Soil Biol Biochem. 1995;27(3):257-263. Doi: 10.1016/0038-0717(94)00190-C.
Ivanova R, Bojinova D, Nedialkova K. Rock phosphate solubilization by soil bacteria. J Chem Technol Metall. 2006;41(3):297-302.
Jha B, Pragash M, Cletus J, Raman G, Sakthivel N. Simultaneous phosphate solubilization potential and antifungal activity of new fluorescent pseudomonad strains, P. aeruginosa, P. plecoglossicida and P. mosselii. World J Microbiol Biotechnol. 2009;25(4):573-581. Doi: 10.1007/s11274-008-9925-x.
Khalid A, Arshad M, Zahir A. Growth and yield response of wheat to inoculation with auxin producing plant growth promoting rhizobacteria. Pak J Bot. 2003;35(4):483-498.
Khalid A, Tahir S, Arshad M, Zahir Z. Relative efficiency of rhizobacteria for auxin biosynthesis in rhizosphere vs. non-rhizosphere soil. Aust J Soil Res. 2004;42(8):921-926. Doi: 10.1071/SR04019.
Khan MS, Zaidi A, Wani P. Role of phosphate solubilizing microorganisms in sustainable agriculture-a review. Agron Sustain Dev. 2007;27(1):29-43. Doi: 10.1051/agro:2006011.
Khan MS, Zaidi A, Ahemad M, Oves M, Wani PA. Plant growth promotion by phosphate solubilizing fungi -current perspective. Arch Agron Soil Sci. 2010;56(1):73-98. Doi: 10.1080/03650340902806469.
Kloepper JW. Plant growth promoting rhizobacteria as biological control agents. In: Metting FB, editor. Soil Microbial Ecology: Applications in Agricultural and Environmental Management. New York: Marcel Dekker; 1993. p. 255-274.
Lara C, Esquivel LM, Negrete-Peñata JL. Bacterias nativas solubilizadores de fosfatos para incrementar los cultivos en el departamento de Córdoba-Colombia. Biotecnología en el Sector Agropecuario y Agroindustrial. 2011;9(2):114-120.
Martínez-Nieto P, García-González DG. Bacterias diazotroficas y solubilizadoras de fósforo aisladas de las especies forestales altoandinas colombianas Weinmannia tomentosa y Escalonia myrtilloides. Rev Intropica. 2010;5(1):63-76.
Matias SR, Pagano MC, Carvalho-Muzzi F, Oliveira CA, Carneiro AA, Horta SN, et al. Effect of rhizobia, mycorrhizal fungi and phosphate-solubilizing microorganisms in the rhizosphere of native plants used to recover an iron ore area in Brazil. Eur J Soil Biol. 2009;45(3):259-266. Doi: 10.1016/j.ejsobi.2009.02.00.
Mittal V, Singh O, Nayyar H, Kaur J, Tewari R. Stimulatory effect of phosphate-solubilizing fungal strains ( Aspergillus awamori and Penicillium citrinum) on the yield of chickpea (Cicerarie tinum L. cv. GPF2). Soil Biol Biochem. 2008;40(3):718-727. Doi: 10.1016/j. soilbio.2007.10.008.
Mohan V, Radhakrishnan A. Screening of phosphate solubilizing bacterial isolates for the growth improvement of Tectonia grandis Linn. Res J Microbiol. 2012;7(2):101-113. Doi: 103923/jm.2012.101.113.
Muleta D, Assefa F, Bõrjesson E, Granhall U. Phosphate-solubilising bacteria associated with Coffea arabica L. in natural coffee forests of southwestern Ethiopia. Journal of the Saudi Society of Agricultural Sciences. 2013;12(1):73-84. Doi: 10.1016/j.jssas.2012.07.002.
Ogata K, Arellano C, Zúñiga D. Efecto de diferentes bacterias aisladas de rizosfera de Caesalpina spinosa en la germinación de algunas especies vegetales. Zonas Áridas. 2008;12(1):137-153.
Paredes-Mendoza M, Espinosa Victoria D. Ácidos orgánicos producidos por rizobacterias que solubilizan fosfato: una revisión crítica. Terra Latinoamericana. 2010;28(1):61-70.
Pikovskaya RI. Mobilization of phosphorus in soil in connection with vitalactivity of some microbial species. Mikrobiologiya. 1948;17:362-370.
Premono M, Moawad MA, Vleck PL. Effect of phosphate solubilizing Pseudomonas putida on the growth of maize and its survival in the rhizosphere. Indones J Crop Sci. 1996;11:13-23.
Ramos-Solano B, Pereyra De La Iglesia MT, Probanza A, Lucas-García JA, Megías M, Gutiérrez-Manero FJ. Screening for PGPR to improve growth of Cistus ladanifer seedlings for reforestation of degraded mediterranean ecosystems. In: Velázquez E, Rodríguez-Barrueco C, editors. First International Meeting on Microbial Phosphate Solubilization. Salamanca, España: Springer; 2007. p. 59-68. Doi: 10.1007/978-1-4020-5765-6_7.
Ramachandran K, Srinivasan V, Hamza S, Anandaraj M. Phosphate solubilizing bacteria isolated from the rhizosphere soil and its growth promotion on black pepper (Pipernigrum L.) cuttings. In: Velázquez E Rodríguez C, editors. First International Meeting on Microbial Phosphate Solubilization. Salamanca, España: Springer; 2007. p. 325-331. Doi: 10.1007/978-1-4020-5765-6_51.
Ribeiro CM, Nogueira-Cardoso EJB. Isolation, selection and characterization of root-associated growth promoting bacteria in Brazil Pine (Araucaria angustifolia). Microbiol Res. 2012;167(2):69-78. Doi: 10.1016/j.micres.2011.03.003.
Richardson AE, Barea JM, McNeill AM, Pringet-Combaret C. Acquisition of phosphorus and nitrogen in the rhizosphere and plant growth promotion by microorganisms. Plant Soil. 2009;321(1-2):305-339. Doi: 10.1007/s11104-009-9895-2.
Richardson AE, Simpson RJ. Soil microorganisms mediating phosphorus availability. Plant Physiol. 2011;156(3):989-996. Doi: 10.1104/PP.111.175448.
Rodríguez H, Fraga R. Phosphate solubilizing bacteria and their role in plant growth promotion. Biotechnol Adv. 1999;17(4-5):319-339. Doi: 10.1016/S0734-9750(99)00014-2.
Sandar R, Shina W. Phosphate dissolving microorganism in the soil and rhizosphere. Indian J Agr Sci. 1963;33:272-278.
Santa-Regina I, Peix A, Díaz T, Rodríguez-Barrueco C, Velázquez E. Effects of plant community composition on total soil microbiota and on phosphate solubilizing bacteria of ex-arable lands. In: Velázquez E, Rodríguez C, editors. First International Meeting on Microbial Phosphate Solubilization. Salamanca, España: Springer; 2007. p. 277-280. Doi: 10.1007/978-1-4020-5765-6_44.
Smalla K, Wieland G, Buchner A, Zock A, Parzy J, Kaiser S, et al. Bulk and rhizosphere soil bacterial communities studied by denaturing gradient gel electrophoresis: plant-dependent enrichment and seasonal shifts revealed. Appl Environ Microbiol. 2001;67(10):4742-4751. Doi: 10.1128/AEM.67.10.4742-4751.2001.
SPSS Inc. PASW Statistics for Windows, Version 18.0. Chicago: IL, USA SPSS Inc. http://www.spss.com [consultado el 14 de septiembre, 2013].
Vargas RO. Restauración Ecológica: biodiversidad y conservación. Acta Biol Colomb. 2011;16(2):221-246.
Yamazaki I, Geraldo L. Uranium content in phosphate fertilizers commercially produced in Brazil. Appl Radiat Isot. 2003;59(2-3):133-136. Doi: 10.1016/S0969-8043(03)00159-3.
Yu X, Liu X, Zhu TH, Liu GH, Mao C. Co-inoculation with phosphate-solubilzing and nitrogen-fixing bacteria on solubilization ofrock phosphate and their effect on growth promotion and nutrient uptake by walnut. Eur J Soil Biol. 2012;50:112-117. Doi: 10.1016/j.ejsobi.2012.01.004.
Zinniel DK, Lambrecht P, Harris NB, Feng Z; Kuczmarski D, Higley P, et al. Isolation and Characterization of Endophytic Colonizing Bacteria from Agronomic Crops and Prairie Plants. Appl Environ Microbiol. 2002;68(5):2198-2208. Doi: 10.1128/AEM.68.5.2198-2208.2002.
Referencias
Azziz G, Bajsa N, Haghjou T, Taulé C, Valverde A, Igual JM, et al. Abundance, diversity and prospecting of culturable phosphate solubilizing bacteria on soils under crop-pasture rotations in a no-tillage regime in Uruguay. Appl Soil Ecol. 2012;61:320-326. Doi: 10.1016/j. apsoil.2011.10.004.
Barreto D, Valero N, Muñoz A, Peralta A. Efecto de microorganismos rizosféricos sobre germinación y crecimiento temprano de Anacardium excelsum. Zonas Áridas. 2007;11(1):240-250.
Bashan Y, Holguin G. Proposal for the division of Plant Growth-Promoting Rhizobacteria into two classification: biocontrol-PGPB (Plant Growth-Promoting Bacteria) and PGPB. Soil Biol Biochem. 1998;30(8):1225-1228. Doi: 10.1016/S0038-0717(97)00187-9.
Cassán F, Bottini R, Schneider G, Piccoli P. Azospirillum brasilense and Azospirillum lipoferum hydrolyze conjugates of GA20 and metabolize the resultant aglycone to GA1 in seedlings of rice dwarf mutants. Plant Physiol. 2001a;125(4):2053-2058. Doi: 10.1104/pp.125.4.2053.
Cassán F, Lucangeli C, Bottini R, Piccoli P. Azospirillum sp. metabolize [17, 17-2H2] gibberellin A20 to [17,17-2H2] Gibberellin A1 in vivo in dy rice mutant seedlings. Plant Cell Physiol. 2001b;42(7):763-767.
Chen YP, Rekha PD, Arun AB, Shen FT, Lai WA, Young CC. Phosphate solubilizing bacteria from subtropical soil and their tricalcium phosphate solubilizing abilities. Appl Soil Ecol. 2006;34(1):33-41. Doi: 10.1016/j.apsoil.2005.12.002.
Compant S, Reiter B, Sessitsch A, Nowak J, Clément C, Barka A. Endophytic colonization of Vitis vinifera L. by a plant groth-promoting bacterium, Burkholderia sp. Strain PsJN. Appl Environ Microbiol. 2005;71(4):1685-1693. Doi: 10.1128/AEM.71.4.1685-1693.2005.
Correll DL. The role of phosphorus in the eutrophication of receiving waters: a review.J Environ Qual. 1998;27(2):261-266. Doi: 10.2134/jeq1998.00472425002700020004x.
Dash S, Kumar A, Gupta N. Growth response of Dalbergia sissoo Roxb. to mineral solubilizing bacteria and fungi in nursery conditions. Trop Ecol. 2013;54(1):109-115.
Del Campillo SE, Van Der Zee S, Torrent J. Modelling long term phosphorus leaching and changes in phosphorus fertility in excessively fertilized acid sandy soils. Eur J Soil Sci. 1999;50(3):391-399. Doi: 10.1046/j.1365-2389.1999.00244.x.
Dunfield KE, Germida JJ. Seasonal changes in the rhizosphere microbial communities associated with field grown genetically modified canola (Brassica napus). Appl Environ Microbiol. 2003;69(12):7310-7318. Doi: 10.1128/ AEM.69.12.7310-7318.2003.
Farina R, Beneduzi A, Ambrosini A, Campos SB, Brito B, Wendisch V, et al. Diversity of plant growth-promoting rhizobacteria communities associated with the stages of canola growth. Appl Soil Ecol. 2012;55:44-52. Doi: 10.1016/j.apsoil.2011.12.011.
Franco LA, García MR. Caracterización de las endomicorrizas y siete grupos de microorganismos en agrosistemas del Piedemonte Amazónico, Colombia. Acta Biol Colomb. 2012;17(2):349-362.
Fulchieri M, Lucangeli C, Bottini R. Inoculation with Azospirillum lipoferum affects growth and gibberellin status of corn seedling roots. Plant Cell Physiol. 1993;34(8):1305-1309.
Galindo T, Polanía J, Sánchez J, Moreno N, Vanegas J, Holguín G. Efecto de inoculantes microbianos sobre la promoción de crecimiento de plántulas de mangle y plantas de Citrullus vulgaris San Andrés Isla, Colombia. Acta biol Colomb. 2006;11(1):83-97.
Gómez L, Zamora R, Gómez J, Hodar J, Castro J, Baraza E. Applying plant facilitation to forest restoration: A meta-análisis of the use of shrubs as nurse plants. Ecol Appl. 2004;14(4):1128-1138. Doi: 10.1890/03-5084.
Gray EJ, Smith DL. Intracellular and extracellular PGPR: commonalities and distinctions in the plant-bacterium signaling processes. Soil Biol Biochem. 2005;37(3):395-412. Doi: 10.1016/j.soilbio.2004.08.030.
Gupta M, Rahi P, Phatania V, Gulati A, Singh B, Kumar-Bhanwra R, et al. Stimulatory effect of phosphate-solubilizing bacteria on plant growth, stevioside and rebaudioside-A contents of Stevia rebaudiana Bertoni. Appl Soil Ecol. 2010;46(2):222-229. Doi: 10.1016/j.apsoil.2010.08.008.
Gupta M, Kiran S, Gulati A, Singh B, Tewari R. Isolation and identification of phosphate solubilizing bacteria able to enhance the growth and aloin-A biosynthesis of Aloebarbadensis Miller. Microbiol Res. 2012;167(6):358-363. Doi: 10.1016/j.micres.2012.02.004.
Gyaneshwar P, Naresh-Kumar GN, Parekh LJ, Poole PS. Role of microorganisms in improving P nutrient of plants. Plant Soil. 2002;245(1):83-93. Doi: 10.1007/978-94-017-1570-6_15.
Hinsinger P. Bioavailability of soil inorganic P in the rhizosphere as affected by root-induced chemical changes: a review. Plant Soil. 2001;237(2):173-195. Doi: 10.1023/A:1013351617532.
Holl KD. Effect of shrubs on tree seedling establishment in an abandoned tropical pasture. J Ecol. 2002;90(1):179-187. Doi: 10.1046/j.0022-0477.2001.00637.x.
Houlden A, Timms-Wilson TM, Day MJ, Bailey MJ. Influence of plant developmental stage on microbial community structure and activity in the rhizosphere of three field crops. FEMS Microbiol Ecol. 2008;65(2):193-201. Doi: 10.1111/j.1574-6941.2008.00535.x.
Illmer P, Schinner F. Solubilization of inorganic calcium phosphates-solubilization mechanisms. Soil Biol Biochem. 1995;27(3):257-263. Doi: 10.1016/0038-0717(94)00190-C.
Ivanova R, Bojinova D, Nedialkova K. Rock phosphate solubilization by soil bacteria. J Chem Technol Metall. 2006;41(3):297-302.
Jha B, Pragash M, Cletus J, Raman G, Sakthivel N. Simultaneous phosphate solubilization potential and antifungal activity of new fluorescent pseudomonad strains, P. aeruginosa, P. plecoglossicida and P. mosselii. World J Microbiol Biotechnol. 2009;25(4):573-581. Doi: 10.1007/s11274-008-9925-x.
Khalid A, Arshad M, Zahir A. Growth and yield response of wheat to inoculation with auxin producing plant growth promoting rhizobacteria. Pak J Bot. 2003;35(4):483-498.
Khalid A, Tahir S, Arshad M, Zahir Z. Relative efficiency of rhizobacteria for auxin biosynthesis in rhizosphere vs. non-rhizosphere soil. Aust J Soil Res. 2004;42(8):921-926. Doi: 10.1071/SR04019.
Khan MS, Zaidi A, Wani P. Role of phosphate solubilizing microorganisms in sustainable agriculture-a review. Agron Sustain Dev. 2007;27(1):29-43. Doi: 10.1051/agro:2006011.
Khan MS, Zaidi A, Ahemad M, Oves M, Wani PA. Plant growth promotion by phosphate solubilizing fungi -current perspective. Arch Agron Soil Sci. 2010;56(1):73-98. Doi: 10.1080/03650340902806469.
Kloepper JW. Plant growth promoting rhizobacteria as biological control agents. In: Metting FB, editor. Soil Microbial Ecology: Applications in Agricultural and Environmental Management. New York: Marcel Dekker; 1993. p. 255-274.
Lara C, Esquivel LM, Negrete-Peñata JL. Bacterias nativas solubilizadores de fosfatos para incrementar los cultivos en el departamento de Córdoba-Colombia. Biotecnología en el Sector Agropecuario y Agroindustrial. 2011;9(2):114-120.
Martínez-Nieto P, García-González DG. Bacterias diazotroficas y solubilizadoras de fósforo aisladas de las especies forestales altoandinas colombianas Weinmannia tomentosa y Escalonia myrtilloides. Rev Intropica. 2010;5(1):63-76.
Matias SR, Pagano MC, Carvalho-Muzzi F, Oliveira CA, Carneiro AA, Horta SN, et al. Effect of rhizobia, mycorrhizal fungi and phosphate-solubilizing microorganisms in the rhizosphere of native plants used to recover an iron ore area in Brazil. Eur J Soil Biol. 2009;45(3):259-266. Doi: 10.1016/j.ejsobi.2009.02.00.
Mittal V, Singh O, Nayyar H, Kaur J, Tewari R. Stimulatory effect of phosphate-solubilizing fungal strains ( Aspergillus awamori and Penicillium citrinum) on the yield of chickpea (Cicerarie tinum L. cv. GPF2). Soil Biol Biochem. 2008;40(3):718-727. Doi: 10.1016/j. soilbio.2007.10.008.
Mohan V, Radhakrishnan A. Screening of phosphate solubilizing bacterial isolates for the growth improvement of Tectonia grandis Linn. Res J Microbiol. 2012;7(2):101-113. Doi: 103923/jm.2012.101.113.
Muleta D, Assefa F, Bõrjesson E, Granhall U. Phosphate-solubilising bacteria associated with Coffea arabica L. in natural coffee forests of southwestern Ethiopia. Journal of the Saudi Society of Agricultural Sciences. 2013;12(1):73-84. Doi: 10.1016/j.jssas.2012.07.002.
Ogata K, Arellano C, Zúñiga D. Efecto de diferentes bacterias aisladas de rizosfera de Caesalpina spinosa en la germinación de algunas especies vegetales. Zonas Áridas. 2008;12(1):137-153.
Paredes-Mendoza M, Espinosa Victoria D. Ácidos orgánicos producidos por rizobacterias que solubilizan fosfato: una revisión crítica. Terra Latinoamericana. 2010;28(1):61-70.
Pikovskaya RI. Mobilization of phosphorus in soil in connection with vitalactivity of some microbial species. Mikrobiologiya. 1948;17:362-370.
Premono M, Moawad MA, Vleck PL. Effect of phosphate solubilizing Pseudomonas putida on the growth of maize and its survival in the rhizosphere. Indones J Crop Sci. 1996;11:13-23.
Ramos-Solano B, Pereyra De La Iglesia MT, Probanza A, Lucas-García JA, Megías M, Gutiérrez-Manero FJ. Screening for PGPR to improve growth of Cistus ladanifer seedlings for reforestation of degraded mediterranean ecosystems. In: Velázquez E, Rodríguez-Barrueco C, editors. First International Meeting on Microbial Phosphate Solubilization. Salamanca, España: Springer; 2007. p. 59-68. Doi: 10.1007/978-1-4020-5765-6_7.
Ramachandran K, Srinivasan V, Hamza S, Anandaraj M. Phosphate solubilizing bacteria isolated from the rhizosphere soil and its growth promotion on black pepper (Pipernigrum L.) cuttings. In: Velázquez E Rodríguez C, editors. First International Meeting on Microbial Phosphate Solubilization. Salamanca, España: Springer; 2007. p. 325-331. Doi: 10.1007/978-1-4020-5765-6_51.
Ribeiro CM, Nogueira-Cardoso EJB. Isolation, selection and characterization of root-associated growth promoting bacteria in Brazil Pine (Araucaria angustifolia). Microbiol Res. 2012;167(2):69-78. Doi: 10.1016/j.micres.2011.03.003.
Richardson AE, Barea JM, McNeill AM, Pringet-Combaret C. Acquisition of phosphorus and nitrogen in the rhizosphere and plant growth promotion by microorganisms. Plant Soil. 2009;321(1-2):305-339. Doi: 10.1007/s11104-009-9895-2.
Richardson AE, Simpson RJ. Soil microorganisms mediating phosphorus availability. Plant Physiol. 2011;156(3):989-996. Doi: 10.1104/PP.111.175448.
Rodríguez H, Fraga R. Phosphate solubilizing bacteria and their role in plant growth promotion. Biotechnol Adv. 1999;17(4-5):319-339. Doi: 10.1016/S0734-9750(99)00014-2.
Sandar R, Shina W. Phosphate dissolving microorganism in the soil and rhizosphere. Indian J Agr Sci. 1963;33:272-278.
Santa-Regina I, Peix A, Díaz T, Rodríguez-Barrueco C, Velázquez E. Effects of plant community composition on total soil microbiota and on phosphate solubilizing bacteria of ex-arable lands. In: Velázquez E, Rodríguez C, editors. First International Meeting on Microbial Phosphate Solubilization. Salamanca, España: Springer; 2007. p. 277-280. Doi: 10.1007/978-1-4020-5765-6_44.
Smalla K, Wieland G, Buchner A, Zock A, Parzy J, Kaiser S, et al. Bulk and rhizosphere soil bacterial communities studied by denaturing gradient gel electrophoresis: plant-dependent enrichment and seasonal shifts revealed. Appl Environ Microbiol. 2001;67(10):4742-4751. Doi: 10.1128/AEM.67.10.4742-4751.2001.
SPSS Inc. PASW Statistics for Windows, Version 18.0. Chicago: IL, USA SPSS Inc. http://www.spss.com[consultado el 14 de septiembre, 2013].
Vargas RO. Restauración Ecológica: biodiversidad y conservación. Acta Biol Colomb. 2011;16(2):221-246.
Yamazaki I, Geraldo L. Uranium content in phosphate fertilizers commercially produced in Brazil. Appl Radiat Isot. 2003;59(2-3):133-136. Doi: 10.1016/S0969-8043(03)00159-3.
Yu X, Liu X, Zhu TH, Liu GH, Mao C. Co-inoculation with phosphate-solubilzing and nitrogen-fixing bacteria on solubilization ofrock phosphate and their effect on growth promotion and nutrient uptake by walnut. Eur J Soil Biol. 2012;50:112-117. Doi: 10.1016/j.ejsobi.2012.01.004.
Zinniel DK, Lambrecht P, Harris NB, Feng Z; Kuczmarski D, Higley P, et al. Isolation and Characterization of Endophytic Colonizing Bacteria from Agronomic Crops and Prairie Plants. Appl Environ Microbiol. 2002;68(5):2198-2208. Doi: 10.1128/AEM.68.5.2198-2208.2002.
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
CrossRef Cited-by
1. Tanya Ascencio-Lino, Esther Matamoros-Alcívar, Verónica Sandoya-Sánchez, Milton Barcos-Arias, Jaime Naranjo-Morán. (2021). Estudio exploratorio de bacterias solubilizadoras de fósforo en dos hábitats asociados con Cedrela montana Moritz ex Turcz. Bionatura, 6(1), p.1575. https://doi.org/10.21931/RB/2021.06.01.20.
2. Mariana Bonifácio Amancio, Yumi Oki, G. Wilson Fernandes, Carla Rago, Aristóteles Góes-Neto, Vasco Ariston de Carvalho Azevedo. (2021). Baccharis. , p.475. https://doi.org/10.1007/978-3-030-83511-8_19.
3. Jeimmi Liliana Amado-Rodríguez, Narda Paola Humeje-Pan, Jorge Orlando Blanco-Valvuena, Nidia Yaneth Torres-Merchán, Miguel Angel García-Parra. (2022). Effect of plant growth promoting bacteria on the phenology of the Amarilla maranganí quinoa cultivar. Revista Colombiana de Ciencias Hortícolas, 16(1) https://doi.org/10.17584/rcch.2022v16i1.13440.
4. Paulina Vega-Celedón, Guillermo Bravo, Alexis Velásquez, Fernanda P. Cid, Miryam Valenzuela, Ingrid Ramírez, Ingrid-Nicole Vasconez, Inaudis Álvarez, Milko A. Jorquera, Michael Seeger. (2021). Microbial Diversity of Psychrotolerant Bacteria Isolated from Wild Flora of Andes Mountains and Patagonia of Chile towards the Selection of Plant Growth-Promoting Bacterial Consortia to Alleviate Cold Stress in Plants. Microorganisms, 9(3), p.538. https://doi.org/10.3390/microorganisms9030538.
Dimensions
PlumX
Visitas a la página del resumen del artículo
Descargas
Licencia
Derechos de autor 2015 Acta Biológica Colombiana

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
1. La aceptación de manuscritos por parte de la revista implicará, además de su edición electrónica de acceso abierto bajo licencia Attribution-NonCommercial-ShareAlike 4.0 (CC BY NC SA), la inclusión y difusión del texto completo a través del repositorio institucional de la Universidad Nacional de Colombia y en todas aquellas bases de datos especializadas que el editor considere adecuadas para su indización con miras a incrementar la visibilidad de la revista.
2. Acta Biológica Colombiana permite a los autores archivar, descargar y compartir, la versión final publicada, así como las versiones pre-print y post-print incluyendo un encabezado con la referencia bibliográfica del articulo publicado.
3. Los autores/as podrán adoptar otros acuerdos de licencia no exclusiva de distribución de la versión de la obra publicada (p. ej.: depositarla en un archivo telemático institucional o publicarla en un volumen monográfico) siempre que se indique la publicación inicial en esta revista.
4. Se permite y recomienda a los autores/as difundir su obra a través de Internet (p. ej.: en archivos institucionales, en su página web o en redes sociales cientificas como Academia, Researchgate; Mendelay) lo cual puede producir intercambios interesantes y aumentar las citas de la obra publicada. (Véase El efecto del acceso abierto).