Genome characterization of a Potato virus S (PVS) variant from tuber sprouts of Solanum phureja Juz. et Buk
Caracterización del genoma de una variante de Potato virus S (PVS) obtenida en brotes de tubérculos de Solanum phureja Juz. et Buk
DOI:
https://doi.org/10.15446/agron.colomb.v34n1.53161Keywords:
plant viruses, carlaviruses, diagnostic techniques, ELISA, PCR, potatoes. (en)virus de plantas, carlavirus, técnicas de diagnóstico, ELISA, PCR, papas (es)
Downloads
Doi: 10.15446/agron.colomb.v34n1.53161
Daniela Vallejo C.1, Pablo Andrés Gutiérrez S.1, and Mauricio Marín M.2
1Laboratory of Industrial Microbiology, Faculty of Sciences, Universidad Nacional de Colombia. Medellin (Colombia)
2 Laboratory of Cellular and Molecular Biology, Faculty of Sciences, Universidad Nacional de Colombia. Medellin (Colombia). mamarinm@unal.edu.co
Received for publication: 21 September, 2015. Accepted for publication: 28 March, 2016.
ABSTRACT
Potato virus S (PVS) is a prevalent virus in potato fields in Colombia and the rest of the world. PVS has been classified into two separate lineages, PVSO (Ordinary) and PVSA (An- dean), which are genetically distinct. In this study, the com- plete genome sequence of a new PVS isolate (PVS_Antioquia) was obtained using High-throughput sequencing (Illumina HiSeq-2000) from tuber sprouts of Solanum phureja (var. Criolla Colombia). The PVS_Antioquia genome comprises 8,483 nt that code for six ORFs: RdRp (223 kDa), TGBp1-3 (25kDa, 12kDa, 7kDa) CP (32.3 kDa) and NABP (11 kDa) and share a high sequence identity with respect to the PVS_RVC (>95%) from Colombia, in contrast to 81 to 82% identity with respect to the PVSA and PVSO isolates from around the world. This genome information was used to design RT-qPCR primers that are specific for the Colombian PVS strains (RVC and Antioquia) which were validated in S. phureja leaf and tuber samples. These primers detected PVS in 80 and 60% of a set of fifteen leaf and tuber samples, respectively, suggesting a high incidence of this virus in the potato crops of Antioquia.
Key words: plant viruses, carlaviruses, diagnostic techniques, ELISA, PCR, potatoes.
RESUMEN
El Potato virus S (PVS) es un virus prevalente en los cultivos de papa de Colombia y otros lugares del mundo. Ha sido dividido en dos razas principales denominadas PVSO (Ordinaria) y PVSA (Andina), que representan a su vez dos linajes genéticos divergentes. En este trabajo se obtuvo la secuencia del genoma completo de un aislamiento de PVS denominado PVS_Antio- quia, por secuenciación masiva de nueva generación (Illumina HiSeq-2000) realizada sobre extractos de transcriptoma de tubérculos de Solanum phureja (var. Criolla Colombia). A partir de este genoma se diseñaron primers específicos para la detección por RT-qPCR de variantes colombianas de PVS (RVC y Antioquia), validándose su utilidad en pruebas de detección en tejido foliar y de tubérculos de S. phureja. El genoma de PVS_Antioquia tiene un tamaño de 8.483 nt que codifica para seis ORFs: RdRp (223 kDa), TGBp1-3 (25kDa, 12kDa, 7kDa) CP (32,3 kDa) y NABP (11 kDa), y comparte altos niveles de identidad con el aislamiento PVS_RVC (>95%) de Colombia y tan solo de 81 a 82% con representantes de PVSA y PVSO de diferentes países del mundo. Los primeros diseñados permitieron detectar el virus en 80 y 60% de 15 muestras foliares y 15 de tubérculos, respectivamente, lo que puede indicar la ocurrencia de altos niveles de incidencia de PVS y sus variantes en los cultivos de papa de Antioquia.
Palabras clave: virus de plantas, carlavirus, técnicas de diagnóstico, ELISA, PCR, papas.
Introduction
Potato virus S (PVS), a virus first described in the Netherlands in 1952 (de BruynOuboter, 1952), is a member of the Carlavirus genus (Betaflexiviridae family) with high incidence in potato fields around the world (Cox and Jones, 2010). PVS virions consist of flexuous rods that are 610-710 to 12-15 nm in size with a positive-sense RNA genome of approximately 8,500 nt in length and six open reading frames (ORFs) encoding an RNA-dependent RNA-polymerase (RdRp, 223 kDa), the triple gene-block proteins (TGBp1-3, 25kDa, 12kDa, 7kDa) involved in virus cell-to-cell movement, a viral coat protein (CP, 32.3 kDa) and a NABP (cysteine-rich nucleic-acid-binding protein) (11 kDa) (Martelli et al., 2007). PVS can be transmitted in a non-persistent manner by aphids, such as Aphis fabae, A. nasturtii, Myzus persicae and Rhopalosiphum padi; mechanical means and/or infected seed tubers (Wardrop et al., 1989; Lambert et al., 2012). Depending on the ability to cause systemic infection or not in the experimental host Chenopodium sp., PVS has been classified into two strains: PVSA (Andean) and PVSO (Ordinary), respectively (Hinostroza-Orihuela, 1973; Lin et al., 2009). More recently, Cox and Jones (2010) proposed the acronyms PVSOCS for isolates that invade Chenopodium sp. systemically, but are not within clade PVSA and PVSA-CL to divergent PVSA isolates that cannot infect Chenopodium sp. systemically and suggested that the term PVSA should be applied strictly to members of the genetically distinct clade. The natural host range of PVS seems to be limited because it has only been reported to infect the sweet cucumber (Solanum muricatum Ait.) (Dolby and Jones, 1988) and different potato species, such as Solanum tuberosum L. (Cox and Jones, 2010) and S. phureja Juz. & Buk (Guzmánet al., 2010; Gutiérrez et al., 2013).
Tipically, PVS strains do not induce visible symptoms in the majority of potato varieties, but, when they do, consist of mild leaf symptoms such as mosaics, leaf rugosity, vein deepening and leaf bronzing (Salari et al., 2011). Although the disease caused by PVSO may be symptomless in the leaves and tubers of infected potatoes, the incidence may reach 100% with yield losses of 15% (Matoueket al., 2005). Additionally, PVS co-infection enhances the severity of other viruses, such as Potato virus A (PVA), Potato virus Y (PVY) and Potato virus X (PVX) (Salari et al., 2011; Ny- alugwe et al., 2012).
S. phureja, locally known as papa criolla, is a potato species widely grown in the South American Andes from western Venezuela to the center of Bolivia (Ghislain et al., 2006) and it has as a main center of diversity in the mountains in the province of Nariño (South of Colombia) (Rodríguez et al., 2009). This crop has received increasing attention in South America as a potential exotic export product due to its excellent organoleptic properties; tubers with yellow skin and medullary tissue; high levels of vitamins B and C, niacine and thiamine; short production cycles and reduced tuber dormancy (Rodríguez et al., 2013). Colombia is the country with the highest commercial explotation of potato varieties derived from S. phureja, which currently represents 8,500 ha and a yearly production of about 100 thousand t (Rodríguez et al., 2013).
Viral diseases are one of the most limiting factors in the production of S. phureja in Colombia, of which PVS has been shown to have a very high incidence (up to 40%) in the main potato producing provinces of Colombia: Antio- quia, Boyaca, Cundinamarca and Nariño (Gil et al., 2013, Gutiérrez et al., 2012, 2013; Gutiérrez-Sánchez, 2014). The coat sequence analysis suggested the existence of at least two PVS variants in Colombia, related to PVSO and PVSA (Gil et al., 2013). A third strain was found by high-trough put sequencing of the foliar transcriptome of S. phureja var. Criolla Colombia (Gutiérrez et al., 2013). The high incidence of PVS in potato crops in Colombia, as well as the presence of new variants never detected elsewhere, highlights the need to better study this genetically distinct clade of PVS that infect S. phureja. In this study, we performed a high-throughput transcriptome sequencing analysis of S. phureja tuber sprouts infected by PVS in the province of Antioquia (Colombia), in order to characterize its sequence properties and to design a set of primers that would be useful in Real-time reverse transcription-PCR (RT-qPCR) for PVS detection.
Materials and methods
Plant samples and DAS-ELISA tests
For this study, fifteen S. phureja tuber samples from different storage cellars in the municipalities of La Union (six samples) and Yarumal (nine samples) and an equal number of leaf samples from S. phureja plots at the flowering stage in the municipalities of Entrerrios (fourth samples from one plot) and Marinilla (11 samples from three plots) were used (Tab. 1). Each tuber and leaf sample consisted of three tubers and six to eight leaflets, respectively. The samples were initially tested for PVS infection by DAS-ELISA using the PSA 40000 kit from Agdia (Elkhart, IN), which uses polyclonal antibodies and alkaline phosphatase enzyme conjugates as capture and detection reagents, respectively.
Results and discussion
Genome features of PVS_Antioquia
The analysis of High-throughput sequencing results con- firmed the presence of a PVS strain, with a genome of 8,483 nt (excluding the 3' poly-A tail), closely related to strain PVS_RVC (95% nucleotide identity), that shares 81 to 82% nucleotide identity with respect to PVSA and PVSO isolates. The assembled sequence was deposited in GenBank under accession KR152654 with PVS_Antioquia as the strain name. No evidence of recombination was found with the program RDP3 (not shown). PVS_Antioquia has 5' and 3' untranslated regions (UTR) of 58 and 104 nt, respectively, and contains six ORFs, as expected. ORF1 (59-5986) codes for the RNA-dependent RNA polymerase (RdRp, 223 kDa) that contains the following functional domains: methyl- transferase (Pfam:PF01660, residues 43-352), Carlavirus endopeptidase (Pfam:PF05379, 1000-1087), RNA helicase (Pfam:PF01443, 1175-1432) and RdRp (Pfam:PF00978, 1553-1967). ORF2 (5973-6704), ORF3 (6682-7008) and ORF4 (6972-7172) comprise the triple gene block (TGB): TGBp1 is predicted to be a 243 residue protein (26.9 kDa) with viral RNA helicase domain (Pfam:PF01443, 40-235), TGBp2 is composed of 108 residues (Pfam:PF01307, 11.7 kDa) and contains a plant viral movement motif (4-104) while TGBp3 comprises 66 residues (7.2 kDa) and contains a 7kDa viral protein motif (Pfam:PF02495, 6-65). The viral coat protein is predicted to be a 294 residues protein (32.3 kDa) encoded by ORF5 at positions 7214-8098 and contain Pfam domains PF08358 (48-99) and PF00286 (108-247), typical of Carlavirus CPs. ORF6 (8095-8379) codes for
Solanum phureja transcriptome sequencing
High-throughput sequencing of the S. phureja transcriptome was performed on a bulk of the tuber-seed sprouts. The bulk sample was ground using liquid nitrogen followed by RNA extraction with the GeneJET Plant RNA Purification mini kit (Thermo Fisher Scientific, Waltham, MA). The library was constructed with the TruSeq RNA Sample Preparation kit (Illumina, San Diego, CA) and rRNA was depleted with the TruSeq Stranded Total RNA with Ribo- Zero Plant kit (Illumina, San Diego, CA). Sequencing was performed with the Illumina HiSeq 2000 System Provided by Macrogen (Seoul, South Korea), which resulted in a pair- end library of 24,817,068 reads for a total of 4,963,413,600 bp. Adapter sequences and low quality bases were removed with SeqTK (https://github.com/lh3/seqtk). The PVS genome was assembled with de novo reconstruction of the S. phureja transcriptome with Trinity (Grabherr et al., 2011) and confirmed by mapping with Bowtie2 (Langmead and Salzberg, 2012). The final contig was assembled from a total of 40,451 paired-end reads with an average depth of 949X. ORFs codifying for viral proteins were identified with BLASTX (Gish and States, 1993). Sequence alignments were performed with MUSCLE (Edgar, 2004). Phylogenetic trees were calculated in MEGA6 (Tamura et al., 2013) using the Maximum Likelihood method based on the General Time Reversible model with a Gamma distribution (+G parameter = 0.4964). Nonsynonymous (Ka) and synonymous (Ks) substitution rates (denoted as Ka and Ks, respectively) were estimated using the software KaKsCalculator (Zhang et al., 2006) with the LPB method (Pamilo and Bianchi, 1993). Recombination analysis was done with the program RDP3 (Martin et al., 2010).
Primer design and RT-qPCR detection of PVS
Alignment of Colombian CP sequences, obtained in this and previous studies (Gil et al., 2013; Gutiérrez et al., 2012, 2013; Gutiérrez-Sánchez, 2014), allowed for the identification of sequences that are useful for designing RT-qPCR primers that are specific for the PVS variants found in Colombia with the aid of the program Primer3Plus (Un- tergasser et al., 2012). Validation of the RT-qPCR primers PVS_gen_F and qPVS_gen_R was performed on the fifteen tuber samples and fifteen leaf samples collected in the different municipalities of Antioquia. RNA was extracted from 100 mg of ground tissue using the GeneJET Plant RNA Purification kit (Thermo, Fisher Scientific, Waltham, MA) and eluted in 40 μL of DEPC treated water; the purity and concentration were determined by absorbance readings at 260 and 280 nm using a Nanodrop 2000C (Thermo Fisher Scientific, Waltham, MA). Retrotranscription was performed for 30 min at 50°C in 20 μL containing 200 U of Maxima Reverse Transcriptase (Thermo Fisher Scientific, Waltham, MA), 1X RT Buffer, 0.5 mM dNTP Mix, 100 pmol Oligo(dT)18, 20 U de RiboLock RNase Inhibitor and 100-500 ng of total RNA. For the qPCR, the Maxima SYBR Green/ROX qPCR Master Mix (2X) kit (Thermo Fisher Scientific, Waltham, MA) was used in 25 μL of reaction containing 12.5 μLmix, 10 μL DEPC water, specific primers PVS_gen_F (5'ATG CCG CCY AAA CCA GAT CC 3') and qPVS_gen_R (5'AGC ATK GCT TCY TCA TTT TGC CCT G 3') at 0.3 μM and 50-100 ngc DNA. The amplification cycles consisted of 10 min at 95°C to activate the polymerase, followed by 35 cycles at 95°C for 15 s and 53°C for 45 s, using a Rotor-Gene Q-5plex Platform (Qiagen, Hilden, Germany); fluorescense was measured after each amplification cycle. The PVS positive control was obtained from a PVS infected potato leaf-tissue and a virus-free sample was used as the negative. The samples were considered positive if they exhibited fluorescence values higher than the threshold before cycle 35 (Schena et al., 2004). Primer specificity was verified by High Resolution Melting in the 50 and 99°C range; the identity of the amplicons was con- firmed by Sanger sequencing of five amplification products (including the positive control), previously purified with the QIAquick Gel Extraction (Qiagen, Valencia, CA) kit. Sequences were edited manually with MEGA6 (Tamura et al., 2013) and compared against the NCBI database using BLASTN (www.ncbi.nlm.nih.gov/BLAST).
Results and discussion
Genome features of PVS_Antioquia
The analysis of High-throughput sequencing results confirmed the presence of a PVS strain, with a genome of 8,483 nt (excluding the 3' poly-A tail), closely related to strain PVS_RVC (95% nucleotide identity), that shares 81 to 82% nucleotide identity with respect to PVSA and PVSO isolates. The assembled sequence was deposited in GenBank under accession KR152654 with PVS_Antioquia as the strain name. No evidence of recombination was found with the program RDP3 (not shown). PVS_Antioquia has 5' and 3' untranslated regions (UTR) of 58 and 104 nt, respectively, and contains six ORFs, as expected. ORF1 (59-5986) codes for the RNA-dependent RNA polymerase (RdRp, 223 kDa) that contains the following functional domains: methyl- transferase (Pfam:PF01660, residues 43-352), Carlavirus endopeptidase (Pfam:PF05379, 1000-1087), RNA helicase (Pfam:PF01443, 1175-1432) and RdRp (Pfam:PF00978, 1553-1967). ORF2 (5973-6704), ORF3 (6682-7008) and ORF4 (6972-7172) comprise the triple gene block (TGB): TGBp1 is predicted to be a 243 residue protein (26.9 kDa) with viral RNA helicase domain (Pfam:PF01443, 40-235), TGBp2 is composed of 108 residues (Pfam:PF01307, 11.7 kDa) and contains a plant viral movement motif (4-104) while TGBp3 comprises 66 residues (7.2 kDa) and contains a 7kDa viral protein motif (Pfam:PF02495, 6-65). The viral coat protein is predicted to be a 294 residues protein (32.3 kDa) encoded by ORF5 at positions 7214-8098 and contain Pfam domains PF08358 (48-99) and PF00286 (108-247), typical of Carlavirus CPs. ORF6 (8095-8379) codes for a 94 a.a. protein (10.6 kDa) and contains a cysteine-rich nucleic-acid-binding protein motif (Pfam:PF01623, 1-89). Ten polymorphic sites were detected in the PVS_Antioquia assembly: A1657G, A1933T, G3169A, T3817C, A3821G, A4828C, G4837A, A6050G, C6131T, C7600T; substitution A3821G results in amino acid change I1255V within RdRp (Fig. 1).
The sequence comparison between the PVS_Antioquia and PVS_RVC revealed a total of 310 transitions and 68 transversions for a global transition/transversion ratio of 4.56. With 60 amino acid substitutions, RdRp is the most divergent protein (96.96% aa identity); the most variable region corresponded to the one connecting the peptidase and methyl transferase domains (Fig. 2). The overall Ka/ Ks ratio for the RdRp ORF was 0.12, suggesting a strong negative selection for the whole protein; however, a sliding window analysis revealed three regions undergoing neutral selection: 640-670, 739-778, 1196-1226 (Ka/Ks of 0.97, 1.00 and 0.84, respectively) and a segment within the helicase domain under positive selection (1263-1277, Ka/Ks of 3.22) (Fig. 2). The triple gene block proteins TGBp1-3 showed a high degree of conservation among the PVS lineages (Fig. 2), with measured Ka/Ks ratios of 0.08, 0.05 and 0.0 that suggested a strong negative selection. TGBp1 shares 98.3% identity at the amino acid level with respect to PVS_RVC and contains four aminoacid substitutions: Y123H, C138S, E140G and T228S. TGBp2 has only one aminoacid substitution E69G while TGBp3 is 100% identical to its homo- log in PVS_RVC. The CP had a total of four amino acid substitutions (V31A, Q35E, P37S and E54G) with respect to PVS_RVC and a sliding window analysis revealed a N-terminal region to be under neutral selection (Ka/Ks=1.08, 23-41). The 11K protein had the highest global Ka/ Ks ratio with a value of 0.8, suggesting a mutation rate close to neutrality; however, residues 7-32 had a local Ka/Ks ratio of 1.23, indicating a slighty positive selection; the following substitutions were observed for this protein: G7S, Y14N, I28V, H40R and P81S. Recombination analyses performed on the PVC_Antioquia genome discarded recombination with other PVS strains as the mechanism of emergence for this new lineage. Failure to detect this PVS variant in previous studies was probably due to the lack of sequence information on Andean PVS strains; future studies would probably confirm the presence of this PVS lineage in other regions of Colombia and South America.
The phylogenetic analysis of the complete PVS genomes showed that isolate PVS_Antioquia clustered with PVS_RVC in an independent clade with a bootstrap of 100%. This clade is a sister group to Andean strains composed of BB-AND from Brazil (Geraldino et al., 2012) and RL5 from Colombia (Gutiérrez et al., 2012) (Fig. 3A). Using a partial segment of the CP sequence, the cluster analysis suggested the existence of four distinct groups (Fig. 3B). The first group comprised PVSO strains and included three Colombian strains isolated in Colombia (Quincha- Cundinamarca, Valle de María-Antioquia and Chasques- Cundinamarca). The second group corresponded to isolates Peruvian and Vltava, of which the latter has been shown to be a recombinant strain between PVSO and PVSA (Geraldino et al., 2012). Group three comprised PVSA isolates BB-AND from Brazil, Q5 from Chile, Guizhou CP01 from China and four Colombian isolates (Suras-Nariño, and El Roble2, RL5, Aldana Bajo from Antioquia). The fourth clade seemed to be a lineage derived from the PVSA group and comprised PVS strains infecting S. phureja such as PVS_Antioquia as well as nine other Colombian isolates from Nariño, Antioquia and Cundinamarca, reported by Gil et al. (2103) and including PVS_RVC (Gutiérrez et al., 2013). CP sequences isolated from S. tuberosum (Gil et al., 2013) clustered in the same clade as PVS_Antioquia, suggesting that this PVS lineage does not have S. phureja as its unique host; however, we propose to name this derived lineage as PVSP in reference to the first known host (S. phureja). Future studies on local S. tuberosum and S. phureja varieties from the South-American Andes will demonstrate whether PVSP has a generalized distribution in countries that are part of the center of origin of the Potato or not. Additionally, it will be of great interest to determine the pathogenic characteristics of members of the PVSP lineage (i.e local or systemic lesions) on Chenopodium sp., which will allow a biological comparison with respect to PVSO and PVSA.
Primer design and RT-qPCR detection of PVS
During the initial stages of this study, it was noticed that previously published primer sets designed to detect PVS failed to amplify some ELISA-positive samples even after exhaustive modifications of both RT-PCR and RT-qPCR protocols (data not shown). A similar situation was observed in a study by Gil et al. (2013) using RT-PCR where the authors where obliged to combine primers PVSCPF and PVSR reported in different papers (Nie and Singh, 2001; Ali et al., 2008) due to amplification problems using the original published sets. Sequence alignment of these primers with respect to the genomes of PVS_Antioquia, RVC and RL5 confirmed the presence of several mismatches at the annealing sites that could affect PCR efficiency (Fig. 4A, B). As these amplification problems could be detrimental to any PCR-based diagnostic tool aimed at detecting Colombian PVS isolates, a new primer set (PVS_gen_F and qPVS_gen_R) was designed for specific detection by RT-qPCR of PVS variants from Colombia. Primers PVS_gen_F and and qPVS_gen_R were tested by RT-qPCR using fifteen tuber and leaf samples obtained at different locations in Antioquia. This trial resulted in positive amplification curves for 80 and 60% of the leaf and tuber samples analysed. The Ct values suggested a higher viral titer in the leaf tissues (Ct in the 7.12-30.08 range) than in the tubers (Ct 28.76-33.94). The specifity of the reaction was confirmed by the melting curve analysis, which resulted in Tm values in good agreement with the positive control (86.96±1°C) (Fig. 4C, D). Sanger sequencing of four randomly chosen samples and for the positive control confirmed amplification of the PVS coat region. Two sequences showed higher identity with regions at positions 7218-7301 of the coat of PVS-RVC (98% identity) while the remaining two samples did so with positions 7215-7300 of the PVS-RL5 genome (100% identity).
In a previous study, Gil et al. (2013) detected the presence of PVS in 40% of the 320 S. tuberosum and S. phureja leaf samples from the four main potato producing provinces of Colombia: Antioquia, Boyaca, Cundinamarca and Nariño. A separate study on the accessions from the Coleccion Central Colombiana de papa using immunoprinting and DAS-ELISA with polyclonal antibodies revealed infections levels of 61.3 and 85%, respectively (Franco-Lara et al., 2009; Guzmánet al., 2010). These reports underscore the need to use stricter parameters in the tuber seed certification program of Colombia, which tolerates PVS levels of 1, 2 and 5% in basic, registered and certified tuber seeds, respectively (ICA, 2015). Similar studies in the rest of the world have revealed high levels of PVS incidence when tuber-seed certifications programs do not reach all farmers in a region or due to the use of diagnostic tests with low sensitivity. For example, a three year study in seven provinces of Iran using two hundred and forty potato samples with one or more symptoms of leaf mosaic, distortion, mottling and yellowing, detected PVS in 18.2% of the samples with a predominance of the PVSO lineage (Salari et al., 2011). In China, Wang et al. (2011) reported an average PVS infection level of 16.3%, reaching values of 22.6 and 26.7% in the provinces of Heilongjiang and Yunnan, respectively. In Costa Rica, Vásquezet al. (2006) evaluated the incidence of PVS and distribution at different altitudes, finding PVS to be present in 19% of the 600 tested samples. The highest PVS incidence was found at middle altitutes because the virus was detected in 60% of the plots of this region with an average infection of 75%.
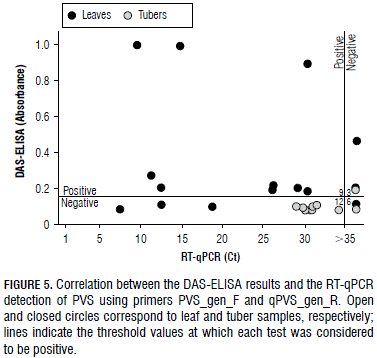
Finally, as expected, the RT-qPCR proved to be of higher sensitivity with respect to ELISA; the latter only detected PVS in one tuber in contrast to RT-qPCR where PVS was found in nine samples (60%); with respect to the leaf samples, ELISA tested positive in eleven cases, while RT-qPCR did so for 12 samples (80%) (Fig. 5). These results suggest a higher PVS titer in leaves than tubers, which supports the notion that RT-qPCR is the method of choice in PVS seed certification programs. The absence of PVS symptoms in most of the potato cultivars and the use of non-certified seeds in different potato-growing regions likely contribute to the prevalence of PVS in many potato-growing areas (Lin et al., 2014a). The ordinary strain of PVS is very widespread in Europe and is considered symptomless for the majority of potato cultivars (Dolby and Jones, 1988). PVSA, on the other hand, can produce much more severe reactions, such as premature senescence and defoliation, and higher losses might result from co-infection by other viruses, such as PVA, PVY and PVX (Salari et al., 2011; Nyalugwe et al., 2012). For this reason, PVSA has been included in the European Union quarantine list for the potato (Jeffries, 1998). A recent study has also shown that PVS may break-down Phytophthora infestans resistance in the potato, making the late blight disease more severe, which may have an important impact in potato breeding programs (Lin et al., 2014b).
Due to the increasing importance of S. phureja for internal use as well as a potential export crop, it is important to establish appropriate certification guidelines using highly sensitive and specific techniques designed to detect local PVS variants. Especially in international trade, tubers and in vitro plants can carry PVS. It would be interesting to further investigate the biological features of isolates belonging to PVSP, including the host range, transmission by aphids and overall agronomical effects as well as the ability of the members of new proposed lineage PVSP to cause systemic and/or non-systemic infections in Chenopodium sp. and its synergistic interaction with other potato viruses.
Conclusions
Complete sequencing of a PVS strain obtained from S. phureja tuber sprouts in Antioquia (Colombia) confirmed the existence of a new lineage of this virus, for which we propose the acronym PVSP. Based on this genome sequence, primers PVS_gen_F and qPVS_gen_R, targeting the CP region, were designed for use in RT-qPCR detection of this virus. The validation of this molecular test on fifteen tuber samples and fifteen leaf samples revealed high levels of incidence of PVS in both tissues (60 and 80%, respectively), suggesting that urgent measures are required to strengthen current S. phureja seed certification programs in Colombia.
Acknowledgment
This work was funded by the Universidad Nacional de Colombia (Grants VRI: 19438 and 26737) and the International Foundation for Science (Sweden, Grant C/4634-2).
Literature cited
Ali, M.C., T. Maoka, and K.T. Natsuaki. 2008. The occurrence of potato viruses in Syria and the molecular detection and characterization of Syrian Potato virus S isolates. Potato Res. 51, 151-161. Doi: 10.1007/s11540-008-9099-9
Cox, B.A. and R.A.C. Jones. 2010. Genetic variability in the coat protein gene of Potato virus S isolates and distinguishing its biologically distinct strains. Arch. Virol. 155, 1163-1169. Doi: 10.1007/s00705-010-0680-6
Crosslin, J.M. and L.L. Hamlin. 2011. Standardized RT-PCR conditions for detection and identification of eleven viruses of potato and Potato spindle tuber viroid. Am. J. Potato Res. 88, 333-338. Doi: 10.1007/s12230-011-9198-z
De BruynOuboter, M.P. 1952. A new potato virus. pp. 83-84. In: Proceedings of the Conference on Potato Virus Diseases. Wageningen-Lisse, The Netherland.
Dolby, C.A. and R.A.C. Jones. 1988. The relationship between the Andean strain of Potato virus S and Pepino latent virus. Ann. Appl. Biol. 112, 231-234. Doi: 10.1111/j.1744-7348.1988.tb02058.x
Edgar, R.C. 2004. MUSCLE: multiple sequence alignment with high accuracy and high throughput. Nucleic Acids Res. 32, 1792-1797. Doi: 10.1093/nar/gkh340
Franco-Lara, L., C.A. Soto A., and M. Guzmán B. 2009. Detección de los virus PVX, PVS, PVY y PLRV en la Colección Central Colombiana de papa por medio de la técnica de inmunoimpresión (IMI). Rev. Fac.Cienc. Básicas. 5, 130-139.
Geraldino, P.S., S.B.F. Galvino-Costa, S.R.R.P. Ribeiro, and A.R. Figueira. 2012. Complete genome sequence of the first Andean strain of Potato virus S from Brazil and evidence of recombination between PVS strains. Arch. Virol. 157, 1357-1364. Doi: 10.1007/s00705-012-1289-8
Ghislain, M., D. Andrade, F. Rodríguez, R.J. Hijmans, and D.M. Spooner. 2006. Genetic analysis of the cultivated potato Solanum tuberosum L. Phureja Group using RAPDs and nuclear SSRs. Theor. Appl. Genet. 113, 1515-1527. Doi: 10.1007/s00122-006-0399-7
Gil, J.F., J.M. Cotes and M. Marín. 2013. Detección serológica y caracterización molecular de Potato virus S (PVS, Carlavirus) en cultivos de papa de Colombia. Rev. Biol. Trop. 61, 565-575. Doi: 10.15517/rbt.v61i2.11149
Gish, W. and D.J. States. 1993. Identification of protein coding regions by database similarity search. Nature Genet. 3, 266-272. Doi: 10.1038/ng0393-266
Grabherr, M.G., B.J. Haas, M. Yassour, J.Z. Levin, D.A. Thompson, I. Amit, X. Adiconis, L. Fan, R. Raychowdhury, Q. Zeng, Z. Chen, E. Mauceli, N. Hacohen, A. Gnirke, N. Rhind, F. di Palma, BW. Birren, C. Nusbaum, K. Lindblad-Toh, N. Friedman and A. Regev. 2011. Full-length transcriptome assembly from RNA-seq data without a reference genome. Nat. Biotechnol. 29, 644-652. Doi: 10.1038/nbt.1883
Gutiérrez S., P.A., J.F. Alzate, and M. Marín-M. 2012. Pirosecuenciación del genoma de una cepa andina de Potato virus S (PVS, Carlavirus) infectando Solanum phureja (Solanaceae) en Colombia. Rev. Fac. Cienc. Básicas 8, 84-93.
Gutiérrez, P.A., J.F. Alzate, and M.A. Marín-Montoya. 2013. Complete genome sequence of a novel potato virus S strain infecting Solanum phureja in Colombia. Arch. Virol. 158, 2205-2208. Doi: 10.1007/s00705-013-1730-7
Gutiérrez-Sánchez, P., J. Alzate-Restrepo, and M. Marín-Montoya. 2014. Caracterización del viroma de ARN en tejido radical de Solanum phureja mediante pirosecuenciación 454 GS-FLX. Bioagro 26, 89-98.
Guzmán, M., V. Román, L. Franco, and P. Rodríguez. 2010. Presencia de cuatro virus en algunas accesiones de la Colección Central Colombiana de papa mantenida en campo. Agron. Colomb. 28, 225-233.
Hinostroza-Orihuela, A.M. 1973. Some properties of potato virus S isolated from Peruvian potato varieties. Potato Res. 16, 244-250. Doi: 10.1007/BF02356057
ICA, Instituto Colombiano Agropecuario. 2015. Resolución 3168 de 2015, por medio de la cual se reglamenta y controla la producción, importación y exportación de semillas producto del mejoramiento genético para la comercialización y siembra en el país, así como el registro de las unidades de evaluación agronómica y/o unidades de investigación en fitomejoramiento y se dictan otras disposiciones. Diario Oficial No. 49.632. Bogota.
Jeffries, C.J. 1998. FAO/IPGRI technical guidelines for the safe movement of germplasm. Potato. No. 19. FAO; IPGRI, Rome.
Lambert, S.J., J.B. Scott, S.J. Pethybridge, and F.S. Hay. 2012. Strain characterization of Potato virus S isolates from Tasmania, Australia. Plant Dis. 96, 813-819. Doi: 10.1094/PDIS-07-11-0573
Langmead, B. and S.L. Salzberg. 2012. Fast gapped-read alignment with Bowtie 2. Nat. Methods 9, 357-359. Doi: 10.1038/nmeth.1923
Lin, Y.H., K.L. Druffel, J. Whitworth, M.J. Pavek, and H.R. Pappu. 2009. Molecular characterization of two potato virus S isolates from late-blight-resistant genotypes of potato (Solanum tuberosum). Arch. Virol. 154, 1861-1863. Doi: 10.1007/s00705-009-0486-6
Lin, Y.H., J.A. Abad, C.J. Maroon-Lango, K.L. Perry, and H.R. Pappu. 2014a. Molecular characterization of domestic and exotic potato virus S isolates and a global analysis of genomic sequences. Arch.Virol. 159, 2115- 2122. Doi: 10.1007/s00705-014-2022-6
Lin, Y.H., D.A. Johnson, and H.R. Pappu. 2014b. Effect of Potato virus S infection on late blight resistance in potato. Am. J. Potato Res. 91, 642-648. Doi: 10.1007/s12230-014-9394-8
Martelli, G.P., M.J. Adams, J.F. Kreuze, and V.V. Dolja. 2007. Family Flexiviridae: a case study in virion and genome plasticity. Annu. Rev. Phytopathol. 45, 73-100. Doi: 10.1146/annurev.phyto.45.062806.094401
Martin, D.P., P. Lemey, M. Lott, V. Moulton, D. Posada, and P. Lefeuvre. 2010. RDP3: a flexible and fast computer program for analyzing recombination. Bioinformatics 26, 2462-2463. Doi: 10.1093/bioinformatics/btq467
Matoušek, J., J.I. Schubert, J. Ptáček, P. Kozlová, and P. Dĕdič. 2005. Complete nucleotide sequence and molecular probing of Potato virus S genome. ActaVirol. 49, 195-205.
Nie, X. and R.P. Singh. 2001. A novel usage of random primers for multiplex RT-PCR detection of virus and viroid in aphids, leaves and tubers. J. Virol. Methods 91, 37-49. Doi: 10.1016/S0166-0934(00)00242-1
Nyalugwe, E.P., C.R. Wilson, B.A. Coutts, and R.A.C. Jones. 2012. Biological properties of Potato virus X in potato: effects of mixed infection with Potato virus S and resistance phenotypes in cultivars from three continents. Plant Dis. 96, 43-54. Doi: 10.1094/PDIS-04-11-0305
Pamilo, P. and N.O. Bianchi. 1993. Evolution of the Zfx and Zfy genes: rates and interdependence between the genes. Mol. Biol. Evol. 10, 271-281.
Rodríguez, L.E., C.E. Ñustez, and N. Estrada. 2009. Criolla Latina, Criolla Paisa y Criolla Colombia, nuevos cultivares de papa criolla para el departamento de Antioquia (Colombia). Agron. Colomb. 27, 289-303.
Rodríguez R., O.J., L.E. Rodríguez M., and J.M. Cotes T. 2013. Caracterización morfo agronómica de híbridos provenientes del cruzamiento entre especies diploides de papa. Rev. Fac. Cienc. Básicas 9, 54-67.
Salari, K., H. Massumi, J. Heydarnejad, A. Hosseini Pour, and A. Varsani. 2011. Analysis of Iranian Potato virus S isolates. Virus Genes 43, 281-288. Doi: 10.1007/s11262-011-0619-3
Schena, L., F. Nigro, A. Ippolito, and D. Gallitelli. 2004. Real-time quantitative PCR: a new technology to detect and study phytopathogenic and antagonistic fungi. Eur. J. Plant Pathol. 110, 893-908. Doi: 10.1007/s10658-004-4842-9
Tamura, K., G. Stecher, D. Peterson, A. Filipski, and S. Kumar. 2013. MEGA6: Molecular evolutionary genetics analysis version 6.0. Mol. Biol. Evol. 30, 2725-2729. Doi: 10.1093/molbev/mst197
Untergasser, A., I. Cutcutache, T. Koressaar, J. Ye, B.C. Faircloth, M. Remm, and S.G. Rozen. 2012. Primer3-new capabilities and interfaces. Nucleic Acids Res. 40, e115. Doi: 10.1093/nar/gks596
Vásquez, V., M. Montero-Astúa, and C. Rivera. 2006. Incidencia y distribución altitudinal de 13 virus en cultivos de Solanum tuberosum (Solanaceae) en Costa Rica. Rev. Biol. Trop. 54, 1135-1141. Doi: 10.15517/rbt.v54i4.3090; 10.15517/rbt.v54i4.14088
Wang, B., Y. Ma, Z. Zhang, Z. Wu, Y. Wu, Q. Wang, and M. Li. 2011. Potato viruses in China. Crop Prot. 30, 1117-1123. Doi: 10.1016/j.cropro.2011.04.001
Wardrop, E.A., A.B. Gray, R.P. Singh, and J.F. Peterson. 1989. Aphid transmission of potato virus S. Am. Pototato J. 66, 449-459. Doi: 10.1007/BF02855437
Yang, L., B. Nie, J. Liu, and B. Song. 2014. A Reexamination of the effectiveness of Ribavirin on eradication of viruses in potato plantlets in vitro using ELISA and quantitative RT-PCR. Am. J. Potato Res. 91, 304-311. Doi: 10.1007/s12230-013-9350-z
Zhang, Z., J. Li, X.-Q. Zhao, J. Wang, G.K.-S. Wong, and J. Yu. 2006. KaKs_Calculator: calculating Ka and Ks through model selection and model averaging. Genomics Proteomics Bioinformatics 4, 259-263. Doi: 10.1016/S1672-0229(07)60007-2
References
Ali, M.C., T. Maoka, and K.T. Natsuaki. 2008. The occurrence of potato viruses in Syria and the molecular detection and characterization of Syrian Potato virus S isolates. Potato Res. 51, 151-161. Doi: 10.1007/s11540-008-9099-9
Cox, B.A. and R.A.C. Jones. 2010. Genetic variability in the coat protein gene of Potato virus S isolates and distinguishing its biologically distinct strains. Arch. Virol. 155, 1163-1169. Doi: 10.1007/s00705-010-0680-6
Crosslin, J.M. and L.L. Hamlin. 2011. Standardized RT-PCR conditions for detection and identification of eleven viruses of potato and Potato spindle tuber viroid. Am. J. Potato Res. 88, 333-338. Doi: 10.1007/s12230-011-9198-z
De BruynOuboter, M.P. 1952. A new potato virus. pp. 83-84. In: Proceedings of the Conference on Potato Virus Diseases. Wageningen-Lisse, The Netherland.
Dolby, C.A. and R.A.C. Jones. 1988. The relationship between the Andean strain of Potato virus S and Pepino latent virus. Ann. Appl. Biol. 112, 231-234. Doi: 10.1111/j.1744-7348.1988.tb02058.x
Edgar, R.C. 2004. MUSCLE: multiple sequence alignment with high accuracy and high throughput. Nucleic Acids Res. 32, 1792-1797. Doi: 10.1093/nar/gkh340
Franco-Lara, L., C.A. Soto A., and M. Guzmán B. 2009. Detección de los virus PVX, PVS, PVY y PLRV en la Colección Central Colombiana de papa por medio de la técnica de inmunoimpresión (IMI). Rev. Fac.Cienc. Básicas. 5, 130-139.
Geraldino, P.S., S.B.F. Galvino-Costa, S.R.R.P. Ribeiro, and A.R. Figueira. 2012. Complete genome sequence of the first Andean strain of Potato virus S from Brazil and evidence of recombination between PVS strains. Arch. Virol. 157, 1357-1364. Doi: 10.1007/s00705-012-1289-8
Ghislain, M., D. Andrade, F. Rodríguez, R.J. Hijmans, and D.M. Spooner. 2006. Genetic analysis of the cultivated potato Solanum tuberosum L. Phureja Group using RAPDs and nuclear SSRs. Theor. Appl. Genet. 113, 1515-1527. Doi: 10.1007/s00122-006-0399-7
Gil, J.F., J.M. Cotes and M. Marín. 2013. Detección serológica y caracterización molecular de Potato virus S (PVS, Carlavirus) en cultivos de papa de Colombia. Rev. Biol. Trop. 61, 565-575. Doi: 10.15517/rbt.v61i2.11149
Gish, W. and D.J. States. 1993. Identification of protein coding regions by database similarity search. Nature Genet. 3, 266-272. Doi: 10.1038/ng0393-266
Grabherr, M.G., B.J. Haas, M. Yassour, J.Z. Levin, D.A. Thompson, I. Amit, X. Adiconis, L. Fan, R. Raychowdhury, Q. Zeng, Z. Chen, E. Mauceli, N. Hacohen, A. Gnirke, N. Rhind, F. di Palma, BW. Birren, C. Nusbaum, K. Lindblad-Toh, N. Friedman and A. Regev. 2011. Full-length transcriptome assembly from RNA-seq data without a reference genome. Nat. Biotechnol. 29, 644-652. Doi: 10.1038/nbt.1883
Gutiérrez S., P.A., J.F. Alzate, and M. Marín-M. 2012. Pirosecuenciación del genoma de una cepa andina de Potato virus S (PVS, Carlavirus) infectando Solanum phureja (Solanaceae) en Colombia. Rev. Fac. Cienc. Básicas 8, 84-93.
Gutiérrez, P.A., J.F. Alzate, and M.A. Marín-Montoya. 2013. Complete genome sequence of a novel potato virus S strain infecting Solanum phureja in Colombia. Arch. Virol. 158, 2205-2208. Doi: 10.1007/s00705-013-1730-7
Gutiérrez-Sánchez, P., J. Alzate-Restrepo, and M. Marín-Montoya. 2014. Caracterización del viroma de ARN en tejido radical de Solanum phureja mediante pirosecuenciación 454 GS-FLX. Bioagro 26, 89-98.
Guzmán, M., V. Román, L. Franco, and P. Rodríguez. 2010. Presencia de cuatro virus en algunas accesiones de la Colección Central Colombiana de papa mantenida en campo. Agron. Colomb. 28, 225-233.
Hinostroza-Orihuela, A.M. 1973. Some properties of potato virus S isolated from Peruvian potato varieties. Potato Res. 16, 244-250. Doi: 10.1007/BF02356057
ICA, Instituto Colombiano Agropecuario. 2015. Resolución 3168 de 2015, por medio de la cual se reglamenta y controla la producción, importación y exportación de semillas producto del mejoramiento genético para la comercialización y siembra en el país, así como el registro de las unidades de evaluación agronómica y/o unidades de investigación en fitomejoramiento y se dictan otras disposiciones. Diario Oficial No. 49.632. Bogota.
Jeffries, C.J. 1998. FAO/IPGRI technical guidelines for the safe movement of germplasm. Potato. No. 19. FAO; IPGRI, Rome.
Lambert, S.J., J.B. Scott, S.J. Pethybridge, and F.S. Hay. 2012. Strain characterization of Potato virus S isolates from Tasmania, Australia. Plant Dis. 96, 813-819. Doi: 10.1094/PDIS-07-11-0573
Langmead, B. and S.L. Salzberg. 2012. Fast gapped-read alignment with Bowtie 2. Nat. Methods 9, 357-359. Doi: 10.1038/nmeth.1923
Lin, Y.H., K.L. Druffel, J. Whitworth, M.J. Pavek, and H.R. Pappu. 2009. Molecular characterization of two potato virus S isolates from late-blight-resistant genotypes of potato (Solanum tuberosum). Arch. Virol. 154, 1861-1863. Doi: 10.1007/s00705-009-0486-6
Lin, Y.H., J.A. Abad, C.J. Maroon-Lango, K.L. Perry, and H.R. Pappu. 2014a. Molecular characterization of domestic and exotic potato virus S isolates and a global analysis of genomic sequences. Arch.Virol. 159, 2115- 2122. Doi: 10.1007/s00705-014-2022-6
Lin, Y.H., D.A. Johnson, and H.R. Pappu. 2014b. Effect of Potato virus S infection on late blight resistance in potato. Am. J. Potato Res. 91, 642-648. Doi: 10.1007/s12230-014-9394-8
Martelli, G.P., M.J. Adams, J.F. Kreuze, and V.V. Dolja. 2007. Family Flexiviridae: a case study in virion and genome plasticity. Annu. Rev. Phytopathol. 45, 73-100. Doi: 10.1146/annurev.phyto.45.062806.094401
Martin, D.P., P. Lemey, M. Lott, V. Moulton, D. Posada, and P. Lefeuvre. 2010. RDP3: a flexible and fast computer program for analyzing recombination. Bioinformatics 26, 2462-2463. Doi: 10.1093/bioinformatics/btq467
Matoušek, J., J.I. Schubert, J. Ptáček, P. Kozlová, and P. Dĕdič. 2005. Complete nucleotide sequence and molecular probing of Potato virus S genome. ActaVirol. 49, 195-205.
Nie, X. and R.P. Singh. 2001. A novel usage of random primers for multiplex RT-PCR detection of virus and viroid in aphids, leaves and tubers. J. Virol. Methods 91, 37-49. Doi: 10.1016/S0166-0934(00)00242-1
Nyalugwe, E.P., C.R. Wilson, B.A. Coutts, and R.A.C. Jones. 2012. Biological properties of Potato virus X in potato: effects of mixed infection with Potato virus S and resistance phenotypes in cultivars from three continents. Plant Dis. 96, 43-54. Doi: 10.1094/PDIS-04-11-0305
Pamilo, P. and N.O. Bianchi. 1993. Evolution of the Zfx and Zfy genes: rates and interdependence between the genes. Mol. Biol. Evol. 10, 271-281.
Rodríguez, L.E., C.E. Ñustez, and N. Estrada. 2009. Criolla Latina, Criolla Paisa y Criolla Colombia, nuevos cultivares de papa criolla para el departamento de Antioquia (Colombia). Agron. Colomb. 27, 289-303.
Rodríguez R., O.J., L.E. Rodríguez M., and J.M. Cotes T. 2013. Caracterización morfo agronómica de híbridos provenientes del cruzamiento entre especies diploides de papa. Rev. Fac. Cienc. Básicas 9, 54-67.
Salari, K., H. Massumi, J. Heydarnejad, A. Hosseini Pour, and A. Varsani. 2011. Analysis of Iranian Potato virus S isolates. Virus Genes 43, 281-288. Doi: 10.1007/s11262-011-0619-3
Schena, L., F. Nigro, A. Ippolito, and D. Gallitelli. 2004. Real-time quantitative PCR: a new technology to detect and study phytopathogenic and antagonistic fungi. Eur. J. Plant Pathol. 110, 893-908. Doi: 10.1007/s10658-004-4842-9
Tamura, K., G. Stecher, D. Peterson, A. Filipski, and S. Kumar. 2013. MEGA6: Molecular evolutionary genetics analysis version 6.0. Mol. Biol. Evol. 30, 2725-2729. Doi: 10.1093/molbev/mst197
Untergasser, A., I. Cutcutache, T. Koressaar, J. Ye, B.C. Faircloth, M. Remm, and S.G. Rozen. 2012. Primer3-new capabilities and interfaces. Nucleic Acids Res. 40, e115. Doi: 10.1093/nar/gks596
Vásquez, V., M. Montero-Astúa, and C. Rivera. 2006. Incidencia y distribución altitudinal de 13 virus en cultivos de Solanum tuberosum (Solanaceae) en Costa Rica. Rev. Biol. Trop. 54, 1135-1141. Doi: 10.15517/rbt.v54i4.3090; 10.15517/rbt.v54i4.14088
Wang, B., Y. Ma, Z. Zhang, Z. Wu, Y. Wu, Q. Wang, and M. Li. 2011. Potato viruses in China. Crop Prot. 30, 1117-1123. Doi: 10.1016/j.cropro.2011.04.001
Wardrop, E.A., A.B. Gray, R.P. Singh, and J.F. Peterson. 1989. Aphid transmission of potato virus S. Am. Pototato J. 66, 449-459. Doi: 10.1007/BF02855437
Yang, L., B. Nie, J. Liu, and B. Song. 2014. A Reexamination of the effectiveness of Ribavirin on eradication of viruses in potato plantlets in vitro using ELISA and quantitative RT-PCR. Am. J. Potato Res. 91, 304-311. Doi: 10.1007/s12230-013-9350-z
Zhang, Z., J. Li, X.-Q. Zhao, J. Wang, G.K.-S. Wong, and J. Yu. 2006. KaKs_Calculator: calculating Ka and Ks through model selection and model averaging. Genomics Proteomics Bioinformatics 4, 259-263. Doi: 10.1016/S1672-0229(07)60007-2
How to Cite
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Download Citation
CrossRef Cited-by
1. H. Yanagisawa, Y. Matsushita, A. Khiutti, N. Mironenko, Y. Ohto, O. Afanasenko. (2021). Occurrence and distribution of viruses infecting potato in Russia. Letters in Applied Microbiology, 73(1), p.64. https://doi.org/10.1111/lam.13476.
2. Andrea García, Mónica Higuita, Rodrigo Hoyos, Yuliana Gallo, Mauricio Marín, Pablo Gutiérrez. (2023). Prevalence of RNA viruses in certified, and informal potato seed tubers in the province of Antioquia (Colombia). Archives of Phytopathology and Plant Protection, 56(1), p.29. https://doi.org/10.1080/03235408.2023.2170208.
3. Pablo Gutiérrez, Ary Rivillas, Daniel Tejada, Susana Giraldo, Andrea Restrepo, María Ospina, Susana Cadavid, Yuliana Gallo, Mauricio Marín. (2021). PVDP: A portable open source pipeline for detection of plant viruses in RNAseq data. A case study on potato viruses in Antioquia (Colombia). Physiological and Molecular Plant Pathology, 113, p.101604. https://doi.org/10.1016/j.pmpp.2021.101604.
4. SUSANA GIRALDO RAMÍREZ, ANDREA SIERRA MEJÍA, MARIA ISABELLA OSPINA ORTIZ, MÓNICA HIGUITA VALENCIA, YULIANA GALLO GARCÍA, PABLO ANDRÉS GUTIÉRREZ SÁNCHEZ, Mauricio Alejandro Marín Montoya. (2022). DETECCIÓN Y CARACTERIZACIÓN MOLECULAR DEL POTATO VIRUS B (PVB) EN CULTIVOS DE PAPA CRIOLLA (Solanum phureja) EN ANTIOQUIA. Acta Biológica Colombiana, 27(2) https://doi.org/10.15446/abc.v27n2.89422.
5. Michelle Bacca, Mónica Higuita, Andrea Restrepo, Yuliana Gallo, Mauricio Marín, Pablo Gutiérrez. (2023). Analysis of viruses infecting Cape gooseberry (Physalis peruviana) in southwestern Antioquia (Colombia) suggests a new member of the genus Trichovirus. Archives of Phytopathology and Plant Protection, 56(8), p.647. https://doi.org/10.1080/03235408.2023.2216342.
6. Yuliana Marcela Gallo García, Andrea Sierra Mejia, Pablo Andrés Gutiérrez Sánchez, Mauricio Alejandro Marín Montoya. (2020). Prevalencia de cinco virus de ARN en tubérculos-semilla de papa cultivados en Antioquia (Colombia). Biotecnología en el Sector Agropecuario y Agroindustrial, 19(1), p.66. https://doi.org/10.18684/bsaa.v19.n1.2021.1343.
7. Yuliana Marcela Gallo García, Andrea Sierra Mejía, Livia Donaire Segarra, Miguel Aranda, Pablo Andres Gutiérrez Sánchez, Mauricio Marín Montoya. (2019). Coinfección natural de virus de ARN en cultivos de papa (Solanum tuberosum subsp. Andigena) en Antioquia (Colombia). Acta Biológica Colombiana, 24(3), p.546. https://doi.org/10.15446/abc.v24n3.79277.
8. Andrea García, Mónica Higuita, Rodrigo Hoyos, Yuliana Gallo, Mauricio Marín, Pablo Gutiérrez. (2022). Indexing of RNA viruses in certified and uncertified potato seed-tubers from Solanum tuberosum cv. Diacol Capiro, and S. phureja cv. Criolla Colombia: a pilot study. Archives of Phytopathology and Plant Protection, 55(9), p.1082. https://doi.org/10.1080/03235408.2022.2081760.
9. Erika Corrales-Cabra, Mónica Higuita, Andrea Restrepo, Yuliana Gallo, Pablo Gutiérrez, Mauricio Alejandro Marín Montoya. (2023). Detección molecular de virus en cultivos de uchuva (Physalis peruviana) del suroeste de Antioquia (Colombia). Acta Agronómica, 71(1), p.88. https://doi.org/10.15446/acag.v71n1.99453.
10. Muhammad Shafiq, Sadia Ahmad, Muhammad Taqqi Abbas, Aymen Ahsan, Mahrukh Asif, Muhammad Saleem Haider. (2024). Viral Diseases of Field and Horticultural Crops. , p.353. https://doi.org/10.1016/B978-0-323-90899-3.00085-9.
11. Nobuya Onozuka, Takehiro Ohki, Norikuni Oka, Tetsuo Maoka. (2020). Detection of four major potato viruses in Japan using a simple RNA preparation and one-step multiplex RT-PCR. Journal of General Plant Pathology, 86(4), p.290. https://doi.org/10.1007/s10327-020-00923-5.
12. O. Karpova, A. Alexandrova, E. Yeriskina, R. Kryldakov, D. Gritsenko, N. Galiakparov, B. Iskakov. (2020). Andean and Ordinary Strains of Potato Virus S Infecting Potatoes in Southern Kazakhstan. Plant Disease, 104(2), p.599. https://doi.org/10.1094/PDIS-09-19-1822-PDN.
13. Johana Madroñero, Zayda Lorena Corredor Rozo, Javier Antonio Escobar Pérez, Myriam Lucia Velandia Romero. (2019). Next generation sequencing and proteomics in plant virology: how is Colombia doing?. Acta Biológica Colombiana, 24(3), p.423. https://doi.org/10.15446/abc.v24n3.79486.
14. V. O. Samarskaya, F. A. Butyrin, T. P. Suprunova, N. A. Spechenkova, M. E. Taliansky, N. O. Kalinina. (2026). The distribution and genetic variability of potato viruses in Russian regions. Acta Naturae, 18(1), p.91. https://doi.org/10.32607/actanaturae.27830.
15. Nobuya Onozuka, Takehiro Ohki, Norikuni Oka, Tetsuo Maoka. (2021). One-step real-time multiplex reverse transcription-polymerase chain reaction assay with melt curve analysis for detection of potato leafroll virus, potato virus S, potato virus X, and potato virus Y. Virology Journal, 18(1) https://doi.org/10.1186/s12985-021-01591-3.
16. Andrea García, Susana Giraldo, Mónica Higuita, Rodrigo Hoyos, Mauricio Marín, Pablo Gutiérrez. (2023). Detection of RNA viruses in potato seed-tubers from northern Antioquia (Colombia). Revista Ceres, 70(5) https://doi.org/10.1590/0034-737x202370050013.
17. Claude Bragard, Katharina Dehnen‐Schmutz, Paolo Gonthier, Marie‐Agnès Jacques, Josep Anton Jaques Miret, Annemarie Fejer Justesen, Alan MacLeod, Christer Sven Magnusson, Panagiotis Milonas, Juan A Navas‐Cortes, Stephen Parnell, Roel Potting, Philippe Lucien Reignault, Hans‐Hermann Thulke, Wopke van der Werf, Antonio Vicent Civera, Jonathan Yuen, Lucia Zappalà, Thierry Candresse, Christophe Lacomme, Bernard Bottex, Carla Oplaat, Annelien Roenhorst, Martijn Schenk, Francesco Di Serio. (2020). Pest categorisation of potato virus S (non‐EU isolates). EFSA Journal, 18(1) https://doi.org/10.2903/j.efsa.2020.5855.
18. Andrea Sierra, Yuliana Gallo, Meike Estrada, Pablo Gutiérrez, Mauricio Marín. (2021). Detection of four RNA viruses in commercial and informal potato seed tubers in Antioquia (Colombia). Archives of Phytopathology and Plant Protection, 54(5-6), p.273. https://doi.org/10.1080/03235408.2020.1829424.
19. Yuliana Gallo, Mauricio Marín, Pablo Gutiérrez. (2021). Detection of RNA viruses in Solanum quitoense by high-throughput sequencing (HTS) using total and double stranded RNA inputs. Physiological and Molecular Plant Pathology, 113, p.101570. https://doi.org/10.1016/j.pmpp.2020.101570.
20. Erika Corrales-Cabra, Mónica Higuita, Rodrigo Hoyos, Yuliana Gallo, Mauricio Marín, Pablo Gutiérrez. (2021). Prevalence of RNA viruses in seeds, plantlets, and adult plants of cape gooseberry (Physalis peruviana) in Antioquia (Colombia). Physiological and Molecular Plant Pathology, 116, p.101715. https://doi.org/10.1016/j.pmpp.2021.101715.
21. Héctor Camilo Medina Cárdenas, Pablo Andrés Gutiérrez Sánchez, Mauricio Alejandro Marín Montoya. (2017). Detection and sequencing of Potato virus Y (PVY) and Potato leafroll virus (PLRV) in a volunteer plant of Solanum tuberosum L. cv. Diacol-Capiro. Acta Agronómica, 66(4), p.625. https://doi.org/10.15446/acag.v66n4.59753.
22. Johanna Stammler, Anita Oberneder, Adolf Kellermann, Johannes Hadersdorfer. (2018). Detecting potato viruses using direct reverse transcription quantitative PCR (DiRT-qPCR) without RNA purification: an alternative to DAS-ELISA. European Journal of Plant Pathology, 152(1), p.237. https://doi.org/10.1007/s10658-018-1468-x.
23. Franklin W. Santillan, Cesar E. Fribourg, Ian P. Adams, Adrian J. Gibbs, Neil Boonham, Monica A. Kehoe, Solomon Maina, Roger A. C. Jones. (2018). The Biology and Phylogenetics of Potato virus S Isolates from the Andean Region of South America. Plant Disease, 102(5), p.869. https://doi.org/10.1094/PDIS-09-17-1414-RE.
Dimensions
PlumX
Article abstract page views
Downloads
License
Copyright (c) 2016 Agronomía Colombiana

This work is licensed under a Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.
© Centro Editorial de la Facultad de Ciencias Agrarias, Universidad Nacional de Colombia
Reproduction and quotation of material appearing in the journal is authorized provided the following are explicitly indicated: journal name, author(s) name, year, volume, issue and pages of the source. The ideas and observations recorded by the authors are their own and do not necessarily represent the views and policies of the Universidad Nacional de Colombia. Mention of products or commercial firms in the journal does not constitute a recommendation or endorsement on the part of the Universidad Nacional de Colombia; furthermore, the use of such products should comply with the product label recommendations.
The Creative Commons license used by Agronomia Colombiana journal is: Attribution - NonCommercial - ShareAlike (by-nc-sa)

Agronomia Colombiana by Centro Editorial of Facultad de Ciencias Agrarias, Universidad Nacional de Colombia is licensed under a Creative Commons Reconocimiento-NoComercial-CompartirIgual 4.0 Internacional License.
Creado a partir de la obra en http://revistas.unal.edu.co/index.php/agrocol/.




















