Semiconductor magnéticamente diluido de SnO2- Fe obtenido por precipitación controlada
(Diluted) Magnetic semiconductor of SnO2- Fe obtained by controlled precipitation
DOI:
https://doi.org/10.15446/dyna.v84n201.55690Palabras clave:
Semiconductor magnéticamente diluido, SnO2, Síntesis, Microestructura, Comportamiento magnético (es)Oxygen Diluid Magnetic Semiconductor, SnO2, Synthesis, Microstructure, Magnetic behavior (en)
Recibido: 11 de febrero de 2016; Revisión recibida: 12 de diciembre de 2016; Aceptado: 25 de febrero de 2017
Resumen
Fueron obtenidas soluciones solidas de SnO2 dopadas con 5% y 8% mol de Fe usando el método de precipitación controlada. Después del proceso de síntesis las muestras en polvo fueron tratadas térmicamente a 350, 500 e 900°C durante una hora. Mediante DRX se observó la casiterita como única fase, y analizando los datos con refinamiento Rietveld se determinó una estimativa de tamaño de cristalito. Usando espectroscopia Raman se estudió la presencia de hierro en las muestras, observando su banda característica en 727cm-1. Microscopia electrónica de transición permitió conocer el tamaño de partícula. Comparando los tamaños de cristalito y de partícula fue posible concluir que las nanopartículas obtenidas son monocristales. Los polvos fueron caracterizados magnéticamente, encontrando comportamiento ferromagnético a 5K en la muestra dopada con 8% y comportamiento paramagnético con tendencia superparamagnetica a 300K.
Palabras clave :
Semiconductor magnéticamente diluido, SnO2, Síntesis, Microestructura, Comportamiento magnético.Abstract
Solid solutions were synthesized SnO2 doped with 5% and 8 mol% Fe by the controlled precipitation method. The particles size was obtained of (12 nm with heath treatment 450 °C. The presence of iron in the structure is evidenced by Raman spectroscopy The crystallite size we obtained with the results of XRD, and particle size by MET, it was concluded that the nanoparticles obtained were monocrystalline. The particles were characterized magnetically, for the powders doped to 8% Fe was determined ferromagnetic behavior at 5K, with a tendency superparamagnetic and paramagnetic at a temperatue of 300K.
Keywords :
Oxygen Diluid Magnetic Semiconductor, SnO2, Synthesis, Microstructure, Magnetic behavior.1. Introducción
El óxido de estaño es un semiconductor tipo n con un valor de banda prohibida de 3.7 eV [1], con estructura cristalina tipo rutilo. En su fase casiterita, como se conoce al SnO2, es un polvo blanco, insoluble en ácidos y álcalis. Es un excelente opacador de brillo y se utiliza en los colorantes cerámicos. Se utiliza en la fabricación de electrodos [2], sensores de gases [3] y varistores [4]; tiene como grupo espacial p/42 mnm y en su celda unitaria se encuentran dos átomos de estaño y cuatro de oxígeno. Es estable a elevadas temperaturas y resiste al ataque químico producido por los ácidos y bases comunes. Presenta una estructura cristalina tetragonal, tipo rutilo, con parámetros de red a = 4.737Å y c=3.186Å [5]. Por otro lado, los semiconductores magnéticamente diluidos son materiales en los cuales una fracción de los cationes que componen su estructura son reemplazados por cationes de metales de transición que poseen electrones desapareados en sus orbitales, dando origen a propiedades magnéticas, magneto-ópticas y magneto electrónicas muy interesantes. Sus aplicaciones más importantes están en la fabricación de dispositivos electrónicos en la “spintronic”, como sensores de gases, memorias de almacenamiento, entre otros. Concretamente, el óxido de estaño, en su fase casiterita, ha sido dopado con varios metales de transición, vanadio [6], níquel [7], cobalto [8] y manganeso [9] para obtener semiconductores magnéticamente diluidos.
En este trabajo se sintetizaron nanopartículas de óxido de estaño, SnO2 dopadas con 5 y 8% en moles de Fe, utilizando el método de precipitación controlada. Su comportamiento magnético se estudió utilizando medidas de susceptibilidad magnética en función de la temperatura, curvas de magnetización y curvas de histéresis a diferentes temperaturas. Los resultados indican que el Fe se incorporó en la estructura de los óxidos conformándose soluciones sólidas y las curvas de histéresis obtenidas muestran el comportamiento ferromagnético del sistema a una temperatura de 5K.
2. Materiales y métodos
2.1. Materiales
Para obtener las muestras de interés fueron utilizados los precursores, cloruro estañoso y sulfato ferroso.
2.2. Síntesis: Precipitación controlada
Este método se empleó con el fin de obtener nanopartículas con diseño morfológico adecuado, además de garantizar su reproducibilidad y poder controlar las características de las partículas a través de los procesos de nucleación y crecimiento; como solvente se utilizó una solución de agua y etanol, en proporciones volumétricas iguales. Por otro lado, la precipitación se realizó a condiciones de agitación constante (100 rpm) y a un pH adecuado, valor que se determinó monitoreando la variación de este parámetro en el sistema. Inicialmente se obtuvo la curva de valoración potenciométrica del sistema, y de allí el valor de pH de trabajo, pH 6.5. Para obtener la suspensión de hierro, el precursor se disolvió en agua destilada-desionizada y se ajustó su pH a un valor de 8 para favorecer el estado de oxidación del hierro +2, seguidamente se mezclaron las dos soluciones y se dejó envejecer la mezcla obtenida durante 24 horas. Finalmente se realizó una serie de 8 lavados con dietilamina (0,1 M), en una solución de agua y etanol cada 24 horas, con el objetivo de eliminar los cloros y los sulfatos del sistema. El polvo resultante se secó en la estufa a 100°C durante 24 horas. El polvo seco se utilizó para realizar las respectivas caracterizaciones del sólido.
2.3. Caracterización
Las propiedades magnéticas de las soluciones solidas de SnO2-Fe, sintetizadas en este trabajo, se determinaron utilizando medidas de magnetización DC. Las medidas fueron realizadas en colaboración del grupo experimental de materia condensada (CIFMC-UNB), utilizando para ello un sistema PPMS (physical property measurement system), con un módulo VMS para concentraciones menores a 10%, y variando la temperatura entre 5 y 300K, aplicándose campos magnéticos hasta de 90 KOe.
Figura 1: Difractogramas de rayos X correspondientes a la casiterita, dopada con 8% en moles de hierro y sintetizada a un pH 8, sin tratamiento térmico y tratadas a 350°C y 900°C durante una hora.
3. Resultados y discusión
3.1. Difracción de rayos X
En la Fig. 1 se muestran los difractogramas de rayos X de los polvos de SnO2, dopados con 8% de hierro y sintetizados a pH 8, tratadas térmicamente a diferentes temperaturas. Para la muestra sin tratamiento térmico se observa que su difractograma presenta los picos característicos de la casiterita (PDF41-1445), anchos y poco definidos indicando que la estructura no está completamente cristalizada.
Tratando el sólido a las temperaturas de 350 °C y 900°C, por 1 hora, se favoreció el ordenamiento de la estructura, condición que se evidencia porque los picos de difracción son más agudos, lo que indica una mayor cristalización en las muestras analizadas. Todos los patrones de la Fig. 1 muestran las reflexiones de Bragg consistentes con una estructura tipo rutilo de grupo espacial, P/42mmm. La ausencia de reflexiones adicionales indica que los iones Fe se incorporaron en la estructura cristalina sustituyendo a los iones Sn, conformándose así una solución sólida SnO2-Fe. En la Fig. 2 se muestran los resultados de refinamiento Rietveld correspondientes a los difractogramas de la muestra dopada con Fe-8 mol% y sintetizada a pH 8, después de tratarla térmicamente a diferentes temperaturas.
Mediante el análisis de refinamiento Rietveld (Fig. 2) se confirmó que la casiterita es la única fase cristalina y se observó una disminución del ancho de los picos a medida que se incrementó la temperatura de tratamiento térmico; el tamaño de cristalito, calculado utilizando los resultados del refinamiento Rietveld, fue de 3nm para la muestra sin tratamiento térmico, y de 4nm y 52nm para las tratadas a 400°C y 900°C, respectivamente.
En la Tabla 1 se muestran los valores de tamaño de cristalito (<D>), la micro-deformación reticular (<ε>) y los parámetros de calidad determinados para algunas temperaturas de tratamiento térmico. La Fig. 3 muestra la influencia del porcentaje de dopado sobre la naturaleza de las fases cristalinas presentes en las muestras sintetizadas a pH 8, tratadas térmicamente a 500°C. Se observó que para los dos porcentajes de dopado, 5% y 8% en moles de hierro, la casiterita es la única fase cristalina y no está muy cristalizada; no se observan diferencias apreciables en la estructura cristalina de los sólidos por los diferentes porcentajes de Fe que ellos tienen.
Figura 2: Refinamiento Rietveld correspondientes a muestras sintetizadas utilizando como solvente una mezcla de agua y etanol a un pH de 8 y dopada a 8% en moles de hierro obtenidos antes y después de tratarlas térmicamente a 350°C, 500°C y 900°C
Fuente: AutorTabla 1: Parámetros obtenidos del refinamiento Rietveld realizados a los difractogramas de las muestras dopados con 8% de Fe, sintetizadas a pH 8.

Figura 3: Difractogramas de rayos X correspondientes a la casiterita, a un pH de 8, dopadas con diferentes porcentajes de Fe (5% y 8%), y tratadas térmicamente a 500°C durante una hora.
3.2. Espectroscopia infrarroja con transformada de Fourier (FTIR)
En la Fig. 4 se observa las deconvoluciones correspondientes a los espectros IR, en el intervalo entre 400 y 900 cm-1 para las muestras tratadas térmicamente a 500°C, siendo la Fig. 4.a para la muestra dopada con 5% en moles de Fe, sintetizada a pH 8, En ella se pueden observar las bandas asociadas a grupos funcionales correspondientes a modos vibracionales del óxido de estaño tal como se indica en la Tabla 2. En la Fig. 4.b se encuentra la deconvolución de la muestra dopada con 8% de Fe, sintetizada a pH 8. Comparando las figuras 4.a e 4.b se observa que las bandas ubicadas a 625 cm-1 y a 550 cm-1, correspondientes a los enlaces Sn-O, presentan diferente intensidad relativa y desplazamiento.
Figura 4: Deconvolución entre 400 y 900 cm-1 de los espectros IR de las muestras sintetizadas a pH 8 y tratadas térmicamente a 500°C (a) muestra dopada con 5% en moles de Fe (b) muestra dopada con 8% de Fe.
Fuente: AutorTabla 2: Grupos funcionales asociados a las bandas presentes en los espectros correspondientes a muestras de SnO2 dopadas al 5% y 8% a pH 8.

Figura 5: Deconvolución espectro Raman, entre 400 y 800 cm-1, de una muestra cerámica de óxido de estaño sintetizada a pH 8, utilizando como solvente una mezcla de agua -etanol, y dopada con 8% de hierro.
3.3. Espectroscopia Raman
En la Fig. 5 se muestra la deconvolución del espectro Raman obtenido para la muestra de SnO2-Fe sintetizada a pH 8, en una mezcla de agua etanol, y dopada con 8% en moles de Fe. En ella se observan bandas a 420, 630 y 765 cm-1 que corresponden a las vibraciones características del SnO2, [15] Eg, A1g y B2g respectivamente; adicionalmente se evidencia claramente las bandas S1, S2 y S3 ubicadas a 500, 550 y 710cm-1, respectivamente. Además, se puede observar una pequeña banda en 727cm-1, que se puede asociar a las vibraciones del hierro [16]
3.4. Microscopia electrónica de transmisión (MET)
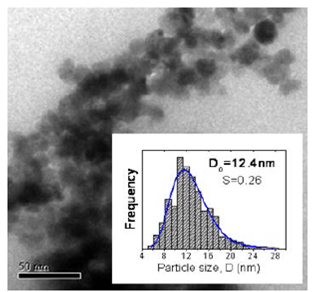
El estudio de la distribución de tamaño de partícula se hizo con ayuda de imágenes obtenidas por MET y el programa imageJ de libre acceso. En la Fig. 6 podemos observar que los tamaños de partícula obtenidos con esta técnica son del mismo orden de magnitud a los valores de tamaño de cristalito obtenidos por refinamiento Rietveld dispuestos en la tabla 1, de aproximadamente 12 nm, como puede ser observado para la muestra dopada con 8% en moles de Fe. De forma similar, fue estudiado el tamaño de partícula para la muestra compuesta por 5% en moles de dopado obteniendo un tamaño de aproximadamente 10 nm. Podemos inferir de este estudio que las muestras en estudio están compuestas por partículas monocristalinas.
Figura 6: Fotografías obtenidas con MET de la muestras sintetizadas a pH 8, y tratada térmicamente a 500°C, dopada con 8% de Fe.
Figura 7: Curvas de susceptibilidad magnética correspondientes SnO2 dopada con 8% y 5% en moles de Fe sintetizadas a pH 8.
3.5. Susceptibilidad magnética
En la Fig. 7 se observan las curvas de susceptibilidad magnética correspondientes al SnO2 dopado con 8% y 5% en moles de Fe sintetizadas pH 8. Las muestras presentan, principalmente, un comportamiento paramagnético ya que no existe evidencia de una temperatura de transición (temperatura de Curie).
En las Figs. 8(a) y 8(b) se presentan las curvas de la magnetización en función del campo magnético para muestras de SnO2 dopada con 8% y 5% en moles de Fe a pH 8.
Figura 8: Curvas de la magnetización en función del campo magnético correspondientes a una muestra de SnO2 dopada con 8% y 5% en moles de Fe sintetizadas a pH 8 (a) para 5K. (b) para 300K.
Se puede observar que, para la temperatura de 5K, existen valores de campo coercitivo y de magnetización remanente, presentando la muestra dopada al 8% valores más altos; en la Tabla 3 se indican estos valores.
Para una temperatura de 300K, en la Fig. 8.b. se puede observar que los valores de magnetización remanente y campo coercitivo correspondientes a estas muestras son nulos.
De acuerdo a las Fig. 8 y los datos de la tabla 3, se puede concluir que las muestras de SnO2 dopadas con hierro a 5% y 8% presentan un comportamiento ferromagnético a bajas temperaturas, siendo más evidente para la muestra dopada al 8%; a temperatura ambiente este material pasa a ser paramagnético.
Fuete: AutorTabla 3: Valores de campo coercitivo y magnetización remanente correspondientes a muestras de óxido de estaño dopadas

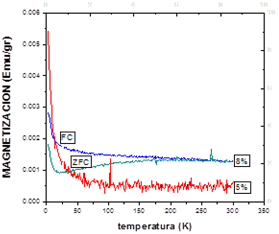
Figura 9: Curvas de magnetización en función de la temperatura a campo cero (ZFC) y a 100 Oe (FC), correspondiente al SnO2 dopado con 5% en moles de Fe sintetizada a pH 10.
De acuerdo a las Fig. 8 y los datos de la Tabla 3, se puede concluir que las muestras de SnO2 dopadas con hierro a 5% y 8% presentan un comportamiento ferromagnético a bajas temperaturas, siendo más evidente para la muestra dopada al 8%; a temperatura ambiente este material pasa a ser paramagnético.
3.6. Curvas de ZFC y FC
En la Fig. 9 se observan las curvas de magnetización en función de la temperatura, en presencia de un campo magnético externo de 100 Oe (FC) y en ausencia de este (ZFC).
Se puede observar que para la muestra dopada al 5% en moles de hierro, las curvas de ZFC y FC no se separan indicando que esta muestra no tiene una temperatura de bloqueo. Mientras que, para la muestra dopada al 8% en moles de hierro, las curvas ZFC y FC presentan una separación y la FC tiene un máximo a ~210 K, temperatura de bloqueo. Considerando la Fig. 9 se puede concluir que la muestra dopada al 8% presenta tendencia al superparamagnetismo, ya que la existencia de una temperatura de bloqueo es propio de este tipo de materiales.
4. Conclusiones
DRX indicó que las muestras dopadas a 5% y 8% en moles de hierro, y sintetizadas a pH 8 solo presentaron los picos de difracción correspondientes al SnO2 indicando que el Fe debió de sustituir al Sn+4 generando soluciones sólidas de SnO2-Fe.
Utilizando espectroscopia Raman se pudo identificar claramente la existencia de la fase casiterita (SnO2) en las muestras, reiterando los resultados de DRX. También se pudo determinar la presencia del hierro adicionado, al sistema de estaño (SnO2), debido a la presencia una banda ubicada a 720 cm-1 asociada a las vibraciones del hierro.
Del análisis con MET, las muestras dopadas con hierro, en porcentajes del 5% y 8%, y tratadas térmicamente a 500°C, se pudo concluir que dado el tamaño de partícula, entre 10 y 12 nm, y el tamaño de cristalito obtenido por refinamiento Rietveld, de 13nm, las partículas son monocristalinas dada la semejanza entre estos.
Las curvas de susceptibilidad, en función de la temperatura, mostraron que los sistemas de SnO2, dopados con 5% y 8% en moles de Fe y sintetizados a pH 8, presentaban comportamiento paramagnético.
De la caracterización magnética se pudo observar que las muestras presentaban un comportamiento ferromagnético a bajas temperaturas y a temperatura ambiente de material paramagnético, más evidente para la muestra dopada con 8% en moles de Fe.
Bibliografía
Referencias
Herrera, F., Estudio de las propiedades estructurales y magnéticas de nanopartículas del SnO2, dopadas con Ni, Co y Cr, MSc Thesis, Instituto de Física, Universidade de Brasilia - Brasil, 2010.
Aquino, G. y, Torres F., Oxidación anódica directa del tolueno sobre los electrodos de SnO2 dopado, Thesis, Universidad Nacional del Centro del Perú, Huancayo, Perú, 2005.
Montenegro, A., Ponce, M., Castro, S. y Rodriguez-Paez, J.E. SnO2-Bi2O3 and SnO2-Sb2O3, gas sensor, obtained by soft chemical method, Journal of the European Ceramic Society, (27) pp 4143-4146, 2007. DOI: 10.1016/j.jeurceramsoc.2007.02.106
Mosquera, A., Rodriguez-Paez, J.E., Varela, J.A. and Bueno, P.R., Syntesis of SnO2 by chemical routes and its use in varistors production. Journal of the European Ceramic Society, (27), pp 3893-3896, 2007. DOI: 10.1016/j.jeurceramsoc.2007.02.056
Ararat-Ibarguen, C.E., Montenegro, A., Rodríguez-Páez, J.E. y Urresta-Aragón, J., Efecto de la naturaleza del precursor sobre las caracteristicas de las nanoparticulas de SnO2 sintetizadas, Quím. Nova 30(7), pp. 1578-1583, 2007. DOI: 10.1590/S0100-40422007000700015
Hong, N.H. and Sakai J., Ferromagnetic V-doped SnO2 thin films, France by School of Materials Science, JAIST, 923-1292, Physica B: Condensade Matter, (358), pp 265-268, 2005. DOI: 10.1016/j.physb.2005.01.456
Sunita, M. and Ravi, S., Magnetic properties of Sn1-x NixO2 based diluted magnetic semiconductors. Solid State Communications, 150(33-34), pp. 1570-1574, 2010. [8] Bouaine, A., Brihi, N., Schmerber, G., Ulhaq-Bouillet, C., Colis, S., and Dinia, A., Structural, optical, and magnetic properties of Co-doped SnO2 powders synthesized by the coprecipitation technique. Phys. Chem. C, (111), pp 2924-2928, 2007. DOI: 10.1021/jp066897p
Tian, Z.M., Yuan, S.L., He, J.H., Li, P., Zhang, S.Q., Wan, C.H., Wang, Y.Q. and Yi, S.Y, Structure and magnetic properties in Mn doped SnO2 nanoparticles synthesized by chemical co-precipitation method. Journal of Alloys and Compounds, 466(20), pp. 26-30, 2008. DOI: 10.1016/j.jallcom.2007.11.054
Nakamoto, K., Infrared and Raman spectra of inorganic and coordination compounds Part B, John Wiley & Sons, fifth edition, Inc. New York, 1997.
Amalric-Popescu, D. and Bozon-Verdulaz, F., Catálysis. Today 70, pp. 139-154, 2001.
Bertoluzza, A., Fagnano, C., Morelli, M.A. and GuglielmiM., Raman and infrared spectra on silica gel evolving toward glass. Journal of Non-Crystalline Solids 48(1), pp. 117-128, 1982. DOI: 10.1016/0022-3093(82)90250-2.
Thornton, E.W. and Harrison, P.G., Tin oxide surfaces. Part 1.—Surface hydroxyl groups and the chemisorption of carbon dioxide and carbon monoxide on tin (IV) oxide. J. Chem. Soc., Faraday Trans. 1, (71), pp 461-472, 1975. DOI: 10.1039/F19757100461
Orel, B., Lavrencic-Stangar, U., Crnajak-Orel, Z., Bukovec, P. and Kosec, J.M., Structural and FTIR spectroscopic studies of gel-xerogel-oxide transitions of SnO2 and SnO2: Sb powders and dip-coated films prepared via inorganic sol-gel route. Non Crystal Solids, 167, pp. 272-288, 1994. DOI: 10.1016/00223093(94)90250-X
Wang, X., Zhang, F.X., Loa, I., Syassen, K., Hanfland, M. and Mathis, Y.-L., Structural properties, infrared reflectivity, and Raman modes of SnO at high pressure. Phys. Stat. Sol. b(241), pp. 3168-3178, 2004. DOI: 10.1002/pssb.200405231
Rumyantseva, M.N., Kovalenko, V.V., Gaskov, A.M., Pagnier, T., Machon, D., Arbiol, J. and Morante, J.R., Nanocomposites SnO2/Fe2O3: Wet chemical synthesis and nanostructure characterization. Sensors and Actuators B: Chemical, 109, pp, 64-74, 2005.
Cómo citar
IEEE
ACM
ACS
APA
ABNT
Chicago
Harvard
MLA
Turabian
Vancouver
Descargar cita
CrossRef Cited-by
1. Ana Karina Pérez‐Guzmán, Anna Ilyina, Alejandro Zugasti‐Cruz, Jose Daniel García‐García, Elda Patricia Segura‐Ceniceros, Jose Luis Martínez‐Hernández, Rodolfo Ramos‐González. (2019). Chitosan–heparin functionalised magnetic nanoparticles for the magnetic recovery of Aspergillus niger lipase enzyme. Micro & Nano Letters, 14(6), p.623. https://doi.org/10.1049/mnl.2018.5490.
Dimensions
PlumX
Visitas a la página del resumen del artículo
Descargas
Licencia
Derechos de autor 2017 DYNA

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial-SinDerivadas 4.0.
El autor o autores de un artículo aceptado para publicación en cualquiera de las revistas editadas por la facultad de Minas cederán la totalidad de los derechos patrimoniales a la Universidad Nacional de Colombia de manera gratuita, dentro de los cuáles se incluyen: el derecho a editar, publicar, reproducir y distribuir tanto en medios impresos como digitales, además de incluir en artículo en índices internacionales y/o bases de datos, de igual manera, se faculta a la editorial para utilizar las imágenes, tablas y/o cualquier material gráfico presentado en el artículo para el diseño de carátulas o posters de la misma revista.