Pre and Postharvest Enzymatic Activity in Gulupa (Passiflora edulis Sims) Fruits from the Colombian Lower Montane Rain Forest
Actividad Enzimática en Precosecha y Poscosecha en Frutos de Gulupa (Passiflora edulis Sims), en Condiciones del Bosque Húmedo Montano Bajo de Colombia
DOI:
https://doi.org/10.15446/rfnam.v67n1.42645Keywords:
Tropical fruit, hydrolytic enzymes, fruit ripening, enzyme changes (en)Frutos tropicales, enzimas hidrolíticas, maduración de la fruta, cambios enzimáticos (es)
Downloads
“High-Andean fruits” are deemed important because of their potential for domestic consumption and exportation. Among them, gulupa (Passiflora edulis Sims) is an exotic fruit of good acceptance in European markets. However, the technological support associated with the crop is incipient and its short shelf life leads to rapid deterioration of the product. This fact makes it necessary to investigate the physical, physiological and biochemical processes that characterize fruit ripening, in order to take actions to ensure that it arrives in its best possible condition to the consumer. In this context, the current study aimed at identifying enzymatic activity in gulupa fruits during pre and postharvest. Plant material from the Colombian Gene Bank (administered by Corpoica) was used. Fruits of known age were periodically harvested to determine the activity of the enzymes α-amylase, polygalacturonase (PG), pectinmethylesterase (PME) and polyphenol oxidase (PPO) through destructive samplings. It was found that α-amylase and PG are linked to the increase of soluble solids, which favors the sweet taste of the fruit. In turn, the low activity of PPO enables agroindustrial processing without severe fruit browning.
Los “frutales alto-andinos”, se consideran importantes por su potencial de consumo nacional y exportación. Entre ellos está la gulupa (Passiflora edulis Sims), reconocida como un frutal exótico de buena aceptación en mercados europeos. Sin embargo, el respaldo tecnológico asociado al cultivo, es incipiente y su corta vida poscosecha conduce al rápido deterioro del producto. Esto hace necesario plantear estudios de los procesos físicos, fisiológicos y bioquímicos que caracterizan la maduración, con el fin de procurar que el fruto llegue en las mejores condiciones de calidad a los consumidores. El estudio tuvo como objetivo conocer la actividad enzimática en los frutos de gulupa en precosecha y en poscosecha, con el fin de contribuir a su manejo en estas etapas del desarrollo. Se utilizó material vegetal proveniente del Banco de Germoplasma de la nación Colombiana administrado por Corpoica, haciendo muestreos destructivos periódicos de frutos con edad conocida, para determinar la actividad de las enzimas α-amilasa, poligalacturonasa (PG), pectinmetilesterasa (PME) y polifenoloxidasa (PFO) en la pulpa del fruto. Se encontró que las enzimas α-amilasa y PG, auspician el incremento en la acumulación de sólidos solubles, favoreciendo el sabor dulce del fruto, en tanto que la baja actividad de la enzima PFO, posibilita la transformación agroindustrial, sin que se presente pardeamiento
Pre and Postharvest Enzymatic Activity in Gulupa (Passiflora edulis Sims) Fruits from the Colombian Lower Montane Rain Forest
Actividad Enzimática en Precosecha y Poscosecha en Frutos de Gulupa (Passiflora edulis Sims), en Condiciones del Bosque Húmedo Montano Bajo de Colombia
Germán Franco1; José Régulo Cartagena Valenzuela2; Guillermo Antonio Correa Londoño3; Benjamín Alberto Rojano4; Ana María Piedrahita Correa5; Albert Ibarz6 and Víctor Falguera7
1 Researcher. Corpoica. C. I. La Selva. A.A. 100. Rionegro, Antioquia, Colombia. <gfranco@corpoica.org.co>
2 Associate Professor. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias Agrarias - Departamento de Ciencias Agronómicas. A.A. 1779. Medellín, Colombia. <jrcartag@unal.edu.co>
3 Associate Professor. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias Agrarias - Departamento de Ciencias Agronómicas. A.A. 1779. Medellín, Colombia. <gcorrea@unal.edu.co>
4 Associate Professor. Universidad Nacional de Colombia - Sede Medellín - Facultad de Ciencias - Escuela de Química. A.A. 3840. Medellín, Colombia. <brojano@unal.edu.co>
5 Colciencias Young Researcher. Universidad Nacional de Colombia - Sede Medellín. Facultad de Ciencias - Escuela de Química. A.A. 3840. Medellín, Colombia <anamarapiedrahita@gmail.com>
6 Associate Professor. Food Technology Department. Universitat de Lleida. Rovira Roure 191. 25198, Lleida, España <aibarz@tecal.udl.cat>
7 Researcher. Efficient Water Management Program. Institut de Recerca i Tecnologia Agroalimentàries (IRTA). Rovira Roure 191. 25198, Lleida, España <victor.falguera@irta.cat>
Received: August 13, 2013; accepted: September 26, 2013.
DOI: https://doi.org/10.15446/rfnam.v67n1.42645
This work is licensed under a Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.

Abstract. "High-Andean fruits" are deemed important because of their potential for domestic consumption and exportation. Among them, gulupa (Passiflora edulis Sims) is an exotic fruit of good acceptance in European markets. However, the technological support associated with the crop is incipient and its short shelf life leads to rapid deterioration of the product. This fact makes it necessary to investigate the physical, physiological and biochemical processes that characterize fruit ripening, in order to take actions to ensure that it arrives in its best possible condition to the consumer. In this context, the current study aimed at identifying enzymatic activity in gulupa fruits during pre and postharvest. Plant material from the Colombian Gene Bank (administered by Corpoica) was used. Fruits of known age were periodically harvested to determine the activity of the enzymes a-amylase, polygalacturonase (PG), pectinmethylesterase (PME) and polyphenol oxidase (PPO) through destructive samplings. It was found that a-amylase and PG are linked to the increase of soluble solids, which favors the sweet taste of the fruit. In turn, the low activity of PPO enables agroindustrial processing without severe fruit browning.
Key words: Tropical fruit, hydrolytic enzymes, fruit ripening, enzyme changes.
Resumen. Los "frutales alto-andinos", se consideran importantes por su potencial de consumo nacional y exportación. Entre ellos está la gulupa (Passiflora edulis Sims), reconocida como un frutal exótico de buena aceptación en mercados europeos. Sin embargo, el respaldo tecnológico asociado al cultivo, es incipiente y su corta vida poscosecha conduce al rápido deterioro del producto. Esto hace necesario plantear estudios de los procesos físicos, fisiológicos y bioquímicos que caracterizan la maduración, con el fin de procurar que el fruto llegue en las mejores condiciones de calidad a los consumidores. El estudio tuvo como objetivo conocer la actividad enzimática en los frutos de gulupa en precosecha y en poscosecha, con el fin de contribuir a su manejo en estas etapas del desarrollo. Se utilizó material vegetal proveniente del Banco de Germoplasma de la nación Colombiana administrado por Corpoica, haciendo muestreos destructivos periódicos de frutos con edad conocida, para determinar la actividad de las enzimas a-amilasa, poligalacturonasa (PG), pectinmetilesterasa (PME) y polifenoloxidasa (PFO) en la pulpa del fruto. Se encontró que las enzimas a-amilasa y PG, auspician el incremento en la acumulación de sólidos solubles, favoreciendo el sabor dulce del fruto, en tanto que la baja actividad de la enzima PFO, posibilita la transformación agroindustrial, sin que se presente pardeamiento.
Palabras clave: Frutos tropicales, enzimas hidrolíticas, maduración de la fruta, cambios enzimáticos.
Generally considered enjoyable and highly-demanded by consumers, High-Andean fruits are commonly marketed fresh in the same region where they are produced. These fruits have a short shelf life with rapid deterioration of their properties in this phase, which affects their quality. Thus, it is necessary to design studies of the physical, physiological and biochemical processes that characterize their ripening. In the Andean region, a wide range of fruit species with good agronomic potential have been identified, including round curuba or gulupa (Passiflora edulis Sims) (Lobo, 2000). Most of the production of this species in Colombia is exported (usually to European markets) reaching 2,250 t in 2012, with a value of US$ 9,750,000 (Agronet, 2012).
Enzymes can be active during postharvest and the changes they determine can positively or negatively influence fruit organoleptic characteristics, so it is important to know the different reactions they catalyze in plant tissues, in order to exploit their advantages and avoid their undesirable effects (Tomás-Barberan and Espin, 2001). A large portion of the fruit protein fraction subjected to changes at different stages of maturation is constituted by enzymes (Belitz and Grosch, 1997; Abu-Goukh and Bashir, 2003), which determine, among other processes, susceptibility to pre and postharvest handling impairment. Inside the fruit, enzymes are involved in catabolic and anabolic reactions, acting only in accordance with cell needs. If the cells are injured, some enzymes are released from their compartments and come into contact with the corresponding substrate, resulting in different reactions that are not always desirable (Brummell and Harpster, 2001). Enzymes perform specific activities at different stages of development. However, when the plant (or fruit) is used as food, all subsequent changes to the optimum consumption point are undesirable and should be prevented during handling and storage (Haard, 1985).
One of the enzymes involved in the reactions of fruit ripening is a-amylase (EC 3.2.1.1), which promotes the hydrolysis of glycosidic bonds a-1-4 and a-1-6 of starch, thus producing oligosaccharides such as maltose and glucose. This process takes place even if the fruit has been separated from the plant at the preclimacteric stage. This allows early (pre-climacteric) harvest, which, when followed by storage under controlled conditions, prevents the fruit from ripening before commercialization (Bowers, 1992; Granados, 1994; García and Peña, 1995; Seymour and Gross, 1996; Willats et al., 2001; Arellano et al., 2005; Menéndez et al., 2006).
Pectinmethylesterase (PME; EC 3.1.1.11) is related to the degradation of pectic substances in the middle lamella of cells. PME hydrolyzes the methoxyl and carboxyl groups of pectin, giving low-methoxyl pectins. This process produces free carboxylic groups (citric acid) involved in pH regulation, cell wall ionic balance and other hydrolytic enzyme activities. PME activity does not affect softening during maturation, but it substantially alters fruit integrity during processing (Hagerman and Austin, 1986; Granados, 1994; Willats et al., 2001; Aponte and Guadarrama 2003, Menéndez et al., 2006). Later on, some other enzymes catalyze the hydrolysis of polygalacturonic acid chains, which results in single units of D-galacturonic acid (Granados, 1994). Genomic data have recently shown that PMEs belong to large multigene families whose primary and quaternary structures are conserved among plant taxa (Pelloux et al., 2007). This enzyme is inhibited by phenolic acids and activated by ethylene, as reported by Arellano et al. (2005) after investigating its activity in black zapote (Diospyros digyna Jacq).
Polygalacturonase (PG; EC 3.2.1.15) hydrolyzes the glycosidic bonds of deesterified polygalacturonides, producing sugars and organic acids. Along with PME, PG constitutes an enzyme system that causes fruit texture degradation and results in suitable consumption hardness. However, excessive activity increases the concentration of galacturonic acid, which causes noticeable softening and makes the fruit more susceptible to the attack of pathogens (Bowers, 1992; García and Peña, 1995; Menéndez et al., 2006).
In the presence of molecular oxygen, polyphenol oxidase (PPO; EC 1.10.3.1) catalyzes the oxidation of phenolic compounds, not only leading to products that are responsible for enzymatic browning during harvest, postharvest, processing and storage, but largely determining the quality and economic value of fruits and vegetables as well. Bruises, cuttings and other mechanical plant damage of cell walls allow oxygen to permeate and come into contact with enzymes and their substrates, which results in darkening or browning processes (García et al., 2006; Ayaz et al., 2008; Guerrero, 2009; Llorente, 2010; Oort, 2010). PPO being a membrane-bound enzyme, the action of ethylene on membrane permeability during maturation can promote the action of the enzyme on phenolic compounds (Arellano et al., 2005; Castro et al., 2006). Llorente (2010) states that this enzyme type has not been assigned a precise location within a metabolic pathway and that its biological function is not clear yet.
Given the importance of the reactions in which these enzymes take place and their effects on fruit quality, the present study aimed at identifying enzymatic activity in gulupa fruits during pre and postharvest, in order to contribute to crop management at these stages.
MATERIALS AND METHODS
Location. The experimental crop was planted in La Selva Research Center (Rionegro, Antioquia, Colombia), which belongs to Corpoica (6º7'49'' N, 75º24'49'' W; 2090 masl; average temperature of 17 °C; annual rainfall of 1917 mm; average relative humidity [RH], 78%; average sunshine, 1,726 hours/year; and average evapotranspiration, 1,202 mm), corresponding to a Lower Montane Rain Forest (LM-rf).
Biological material. The trial was conducted in an experimental area where 10 gulupa accessions were randomly planted. The materials are part of the Colombian Gene Bank (administered by Corpoica), which, after Amplified Fragment Length Polimorphism (AFLP) and Simple Sequence Repeat (SSR) molecular marker analysis, was reported to have low genetic variability (Ortiz, 2010). According to Angel et al. (2011), the fruits were obtained from homogametic flowers with and without herkogamy, which were labeled with colored threads, these stages being taken as day zero of fruit age. Since then on, time records were labeled as days after flowering (DAF). The harvest took place at 91 DAF as established by Franco et al. (2013).
Experimental procedure. For all analyses, destructive samplings were performed every seven days from 49 DAF to 112 DAF, except for PPO, which was determined from 84 DAF onwards. For postharvest analysis, the fruits were collected since 91 DAF and monitored every seven days until 21 days after harvest, coinciding with 98, 105 and 112 DAF. These records were used to compare the enzymatic activity of fruits on and off the vine. The sampling unit consisted of 10 fruits which were randomly gathered from the planted materials, forming independently balanced samples with respect to fruit size. They were transported in styrofoam boxes containing dry ice (internal temperature of 4 °C). Determinations were performed at the laboratory of Food Science of Universidad Nacional de Colombia, Medellin campus. Postharvest variables were assessed at the Postharvest Laboratory of Corpoica.
Raw juice was obtained by cutting the fruits across the equatorial zone and sieving the pulp and seeds. All procedures were performed on a vessel containing ice, in order to obtain a temperature of approximately 4 °C. The resulting juice was placed in an ice-cooled container. For enzymatic activity determination, the juice of 10 fruits was mixed until complete homogeneity, with the subsequent extraction of three samples for analysis.
a-amylase activity. Enzyme extract was obtained by homogenizing 5 g of pulp with 10 mL of a 0.05 M citrate buffer solution (pH 4.5, 13 mM EDTA, 10 mM 2-mercaptoethanol, and 1% polyvinylpyrrolidone [w/v]). For 40 min, the mixture was centrifuged at 4,000 rpm and 4 °C on a LABNET® Hermle Z366 centrifuge. The supernatant was used for enzyme analysis. a-amylase activity was determined by the method described by Bernfelds (1955) with some modifications. 250 µL of enzyme extract were added to a 1% starch solution in 0.02 M phosphate buffer (pH 6.9) and kept at 23 °C for 10 min. The reaction was stopped by adding 500 µL of a 1% DNS solution and the mixture was brought to 90 °C for 5 min, after which it was cooled in ice bath. Absorbance at 540 nm was read by means of an UV-Vis Thermo Scientific Genesis® 20 spectrophotometer. The activity of a-amylase was expressed as µmol min-1 of maltose released per mg of total protein under the conditions of the experiment.
PG activity. Enzyme extract was obtained by homogenizing 5 g of pulp with 10 mL of a 0.05 M citrate buffer solution (pH 4.5, 13 mM EDTA, 10 mM 2-mercaptoethanol and 1% polyvinylpyrrolidone [w/v]). For 40 min, the mixture was centrifuged at 4000 rpm and 4 °C in a LABNET® Hermle Z366 centrifuge. The supernatant was used for enzyme analysis. Following methodology by Nelson (1944), PG activity was determined by spectrophotometric measurement (Miller, 1959) of the reducing sugars generated after the action of the enzyme on polygalacturonic acid. 60 µL of enzyme extract were added to 540 µL of a 0.4% (w/v) polygalacturonic acid solution in 0.05 M acetate buffer, pH 4.0. This mixture was incubated at 37 °C for 10 min and the reaction was stopped by adding 600 µL of a 1% DNS solution. The mixture was brought to 90 °C for 5 min, after which it was cooled in ice bath. Absorbance at 540 nm was read by means of an UV-Vis Thermo Scientific Genesis® 20 spectrophotometer. PG activity was expressed as µmol min-1 of galacturonic acid released per mg of total protein, under the conditions of the experiment.
PME activity. Enzyme extract was obtained by homogenizing 4.5 g of pulp with 15 mL of an 8.8% (w/v) NaCl solution. The mixture was stirred vigorously for 30 s and then centrifuged at 4000 rpm and 4 °C on a LABNET® Hermle Z366 centrifuge for 40 min. The supernatant constituted the enzyme extract, which was adjusted to pH 7.5 with 0.1 N NaOH. PME activity was determined by monitoring the pH change produced by the hydrolysis of the ester bond in the polygalacturonic acid molecule through bromothymol blue (which absorbs at a wavelength of 620 nm) color change. For proper enzymatic activity determination, 100 µL of enzyme extract were added to 200 µL of a 0.15 M NaCl solution, 100 µL of 0.5% (w/v) bromothymol blue and 1 mL of a solution of citrus pectin 0.25% (w/v) adjusted to pH 7.5 with 0.1 N NaOH. After three minutes, the difference in absorbance at 620 nm, which was read by means of a Multiskan V1.2 Spectrum Thermo Scientific® spectrophotometer, expresses the enzymatic activity as DAbs min-1 per mg of total protein, under the conditions of the experiment (Hagerman and Austin, 1986).
PPO activity. Enzyme extract was obtained by homogenizing 4 g of pulp with 20 mL of a 0.2 M phosphate buffer solution (pH 7.0) containing 0.4 g of polyvinylpyrrolidone (PVP). The mixture was stirred vigorously for 30 s and then centrifuged at 400 rpm and 4 °C in a LABNET® Hermle Z366 centrifuge for 40 min. The supernatant constituted the enzymatic extract. PPO activity was determined based on the method described by García (2006), wherein a unit of activity is defined as the amount of enzyme that causes an absorbance increase of 0.001 units min-1 at 30 °C. One thousand µL of enzyme extract were added to 1,480 µL of a 100 mM catechol solution and 500 µL of 0.2 M phosphate buffer, pH 7.0. The mixture was brought to 30 °C for 3 min, after which absorbance at 420 nm was read by means of an UV-Vis Thermo Scientific Genesis® 20 spectrophotometer for 5 min. The activity of PPO was expressed as UA min-1 per mg of total protein, under the conditions of the experiment.
Total protein. Total protein was measured by the Bradford method (1976), which quantifies the binding of Coomassie Blue dye to an unknown protein and compares it to a standard curve prepared with different concentrations of serum albumin protein (BSA).
Total soluble solids. Total soluble solids were determined according to Colombian Technical Standard (Norma Técnica Colombiana - NTC) 4624 by Icontec (1999), using a Milton Roy Company® refractometer at a temperature of 20 ºC. Quantification was performed on each of the 10 fruits gathered at every sampling period.
RESULTS AND DISCUSSION
a-amylase specific activity. An activity increase started 63 DAF and reached the highest record at 70 DAF (Figure 1). Similar results were reported by Menéndez et al. (2006), who established that yellow passion fruit (P. edulis var. flavicarpa Degener) a-amylase activity was more intense in the ninth week and then decreased.
The greatest activity of this enzyme was found to be associated to soluble solids concentration increase (Figure 2), because the substrate of this enzyme is starch (Shiomi et al., 1996; Menéndez et al., 2006). Upon hydrolyzed, starch contributes to glucose increase, giving the gulupa fruit a sweet taste. Postharvest values showed the same tendency of the fruits on the vine, thus ensuring the processing of starch by this enzyme and, consequently, an optimum fruit quality.
PME specific activity. Increase and maximum peak of this activity (Figure 3) coincided with that observed for a-amylase, agreeing with a previous report by Aponte and Guadarrama (2005) and Menéndez et al. (2006). These authors determined that the activity of this enzyme increases towards physiological maturity and then decreases at harvest (Figure 3). In the maturation process of passion fruit, Aponte and Guadarrama (2003) and Menéndez et al. (2006) also observed that the activity of this enzyme is higher at the commercial maturity stage, with decreased activity during over ripening stages.
PME activity does not affect softening during ripening, but it significantly alters the integrity of the fruit during its processing (Granados, 1994; Hagerman and Austin, 1986; Willats et al. 2001; Aponte and Guadarrama 2003). PME prepares the fruit for the action of other enzymes that catalyze the hydrolysis of polygalacturonic acid chains, producing single units of D-galacturonic acid (Granados, 1994). During postharvest, PME activity showed a tendency to decrease, which contrasts with that of other climacteric fruits such as black zapote (Diospyros digyna Jacq), where this parameter showed an increase that matched other metabolic events such as the production of ethylene (Arellano et al., 2005).
PG specific activity. Like PME, this enzyme is associated to fruit ripening. PG showed low activity at 84 DAF, with a peak at 91 DAF (Figure 4), similar to a previous report in yellow passion fruit by Menéndez et al. (2006), which these authors observed at a different age, though. This was probably due to the different geographic location and altitude of the areas where the experiments were conducted. The coincidence between maximum PG activity peak and soluble solids content increase was very clear in this study. During postharvest, PG activity followed an increasing trend until seven days after harvest, as indicated by Aponte and Guadarrama (2005).
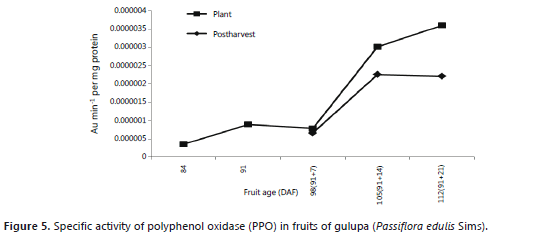
PPO specific activity. The values found in this study for the specific activity of PPO in gulupa were small (Figure 5), coinciding with those observed by Falguera et al. (2011) in yellow passion fruit. These records showed an increasing pattern during ripening and postharvest, consistent with the observations of Lobo (1995) in papaya (Carica papaya L.) and Dueñas et al. (2008) in pitahaya (Acanthocereus pitajaya sensu Croizat). In some cases this enzyme shows an intense activity after the climacteric peak, producing browning problems in fruits like apple (Malus domestica Borkh), for which the application of treatments such as ultraviolet radiation has been suggested to inactivate the negative effect on the juice (Falguera et al., 2011). Also during postharvest, PPO showed an increasing trend, different from that observed in other fruits such as Gros Michel bananas, where Garcia et al. (2006) found the lowest activity of this enzyme at advanced stages of maturation, suggesting its degradation with ripening. The observed values indicate that PPO action on polyphenolic compounds is reduced, which favors the processing of gulupa (Ayaz et al., 2008; Guerrero, 2009; Llorente, 2010, Oort, 2010).
CONCLUSIONS
From the point of view of the quality of the fruit, the activity of the enzymes a-amylase and PG in gulupa (Passiflora edulis Sims) is important because they enhance soluble solids increase. The low activity of PPO guarantees the industrial processing of gulupa juice, probably with only smooth enzymatic browning.
BIBLIOGRAPHY
Abu-Goukh, A.A. and H.A. Bashir. 2003. Changes in pectic enzymes and cellulase activity during guava fruit ripening. Food Chemistry 83(2): 213-218.
Agronet. 2012. Comercio exterior de Colombia. Exportaciones del sector agropecuario. www.agronet.gov.co; consulta: noviembre 2012.
Ángel, C., G. Nates, R. Ospina, C. Melo y M. Amaya. 2011. Biología floral y reproductiva de la gulupa Passiflora edulis sims f. edulis. Caldasia 33(2): 433-451.
Aponte, L. y A. Guadarrama. 2003. Actividad de las enzimas pectinmetilesterasa, poligalacturonasa y celulasa durante la maduración de frutos de parchita maracuyá (Passiflora edulis f. flavicarpa Degener). Revista de la Facultad de Agronomía. (Maracay) 29(2): 145-160.
Arellano, L.A., C. Saucedo y L. Arévalo. 2005. Cambios bioquímicos y fisiológicos durante la maduración de frutos de zapote negro (Diospyros digyna Jacq.). Agrociencia 39(2): 173-181.
Ayaz, F.A., O. Demir, H. Torun, Y. Kolcuoglu and A. Colak. 2008. Caharacterizacion of polyphenoloxidase (PPO) and total phenolic contens in medlar (Mespilus germanica L.) fruit during ripening and over ripening. Food Chemistry 106(1): 291-298.
Belitz, H.D. y W. Grosch. 1997. Química de los alimentos. Segunda edición. Editorial Acribia. Zaragoza, España. 1.087 p.
Bernfelds, P. 1955. Amylase a y b. pp. 149-159 In: Colowick S.P., N.O. Kaplan (eds.). Methods in enzymology. Volume 1. Academic Press, Nueva York, USA. 835 p.
Bowers, J. 1992. Food theory and applications. Macmillan Publishing Company, New York, USA. 952 p.
Bradford, M. 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry (1-2)72: 248-254.
Brummell, D.A. and M.H. Harpster. 2001. Cell wall metabolism in fruit softening and quality and its manipulation in transgenic plants. Plant Molecular Biology 47(1-2): 311-340.
Castro, J.A., L.E. Baquero y C.E. Narváez. 2006. Catalasa, peroxidasa y polifenolxidasa de pitahaya amarilla (Acanthocereus pitajaya). Revista Colombiana de Química 35(1): 91-100.
Dueñas, Y., C. Narváez y L. Restrepo. 2008. Inhibición de lesiones por frío de pitaya amarilla (Acanthocereus pitajaya) a través del choque térmico: catalasa, peroxidasa y polifenoloxidasa. Acta Biológica Colombiana 13(1): 95-106.
Falguera, V., J. Pagán and A. Ibarz. 2011. Effect of UV irradiation on enzymatic activities and physicochemical properties of apple juices from different varieties. LWT - Food Science and Technology 44(1): 115-119.
Franco, G., J.R. Cartagena y G.A. Correa. 2013. Informe. Análisis de crecimiento del fruto de gulupa (Passiflora edulis Sims), en las condiciones ecológicas del bosque húmedo montano bajo de Colombia. Facultad de Ciencias Agrarias. Universidad Nacional de Colombia, Medellín. 12 p.
García, H.E. y V.C. Peña. 1995. La pared celular: componente fundamental de las células vegetales. Universidad Autónoma de Chapingo, México. 75 p.
García, C., G. Giraldo, H. Hurtado y C. Mendivil. 2006. Cinética enzimática de la polifenol oxidasa del banano (Gros Michel) en diferentes estados de maduración. Vitae 13(2): 13-19.
Guerrero, C.A. 2009. Inhibición de la actividad enzimática de la polifenol oxidasa extraída del banano (Cavendish Valery) mediante sistemas bifásicos acuosos con isoespintanol y ácido ascórbico. Tesis Magíster en Ciencia y Tecnología de Alimentos. Facultad de Ciencias Agropecuarias. Universidad Nacional de Colombia, Sede Medellín. 91 p.
Granados, J.R. 1994. Química avanzada Nuffield, ciencia de la alimentación. Editorial Reverté S.A. Barcelona. 172 p.
Haard, N.F. 1985. Características de los tejidos de plantas comestibles. pp. 861-867. En: Fennema, O.R. (ed.). Introducción a la Ciencia de los Alimentos. Editorial Reverté S.A. Barcelona.
Hagerman, A.E. and P.J. Austin. 1986. Continuous spectrophotometric assay for plant pectin methyl esterase. Journal of Agriculture and Food Chemistry 34(3): 440-444.
Instituto Colombiano de Normas Técnicas y Certificación. (Icontec). 1999. NTC 4624. Jugos de frutas y hortalizas. Determinación del contenido de sólidos solubles. Método refractométrico. Icontec, Bogotá. 9 p.
Menéndez, O., S.E. Lozano, M. Arenas, K.A. Bermúdez, A. Martínez y A. Jiménez. 2006. Cambios en la actividad de a-amilasa, pectinmetilestrasa y poligalacturonasa durante la maduración del maracuyá amarillo (Passiflora edulis var. flavicarpa Degener. Interciencia 31(10): 728-733.
Miller, G. 1959. Use of dinitrosalicylic acid reagent for determination of reducing sugar. Analytical Chemistry 31(3): 26-31.
Nelson, N. 1944. A photometric adaptation of the Somogyi method for determination of glucose. The Journal of Biological Chemistry 153: 378-380.
Lobo, M.G. 1995. Caracterización bioquímica de frutos de papaya (Carica papaya cv. Sunrise), hembra y hermafrodita, en relación con su aptitud al procesado por congelación. Tesis doctoral. Facultad de Farmacia. Universidad Complutense de Madrid. Madrid. 326 p.
Lobo, M. 2000. Papel de la variabilidad genética en el desarrollo de los frutales andinos como alternativa productiva. pp. 27-36. En: Memorias III Seminario de Frutales de Clima Frío Moderado. Centro de Desarrollo Tecnológico de Frutales - CDTF, Manizales.
Llorente, B.E. 2010. Un rol biológico propuesto para las misteriosas polifenol oxidasas vegetales. Tesis Doctor en Química Biológica. Facultad de Ciencias Exactas y Naturales. Departamento de Química Biológica. Universidad de Buenos Aires, Argentina. 88 p.
Oort, van M. 2010. Enzymes in bread making. pp. 103-143. In: Whitehurst, R.J. and Oort, van M. (ed.) Enzymes in Food Technology. Second edition. Wiley Blackwell Publishing, New Delhi, India. 360 p.
Ortiz, D.C. 2010. Estudio de la variabilidad genética en materiales comerciales de gulupa (Passiflora edulis f. edulis Sims) en Colombia. Tesis Magíster en Ciencias Agrarias. Facultad de Agronomía. Universidad Nacional de Colombia, Bogotá. 127 p.
Pelloux, J., C. Rustérucci and E.J. Mellerowicz. 2007. New insights into pectin methylesterase structure and function. Trends in Plant Science 12(6): 267-277.
Seymour; G. B. and K. C. Gross. 1966. Cell wall disassembly and fruit softening. Postharvest News Information. 7: 45N-52N.
Shiomi, S., L.S. Wamocho and S.G. Agong. 1996. Ripening characteristics of purple passion fruit on and off the vine. Postharvest Biology and Technology 7(1-2): 161- 170.
Tomás-Barberan, F.A. and J.C. Espin. 2001. Phenolic compounds and related enzymes as determinants of quality in fruits and vegetables. Journal of the Science of Food and Agriculture 81(9): 853-876.
Willats, W.G., L. McCartney, W. Mackie and J.P. Knox. 2001. Pectin: cell biology and prospects for functional analysis. Plant Molecular Biology 47(1-2):9-27.
References
Abu-Goukh, A.A. and H.A. Bashir. 2003. Changes in pectic enzymes and cellulase activity during guava fruit ripening. Food Chemistry 83(2): 213-218.
Agronet. 2012. Comercio exterior de Colombia. Exportaciones del sector agropecuario. www.agronet.gov.co; consulta: noviembre 2012.
Ángel, C., G. Nates, R. Ospina, C. Melo y M. Amaya. 2011. Biología floral y reproductiva de la gulupa Passiflora edulis sims f. edulis. Caldasia 33(2): 433-451.
Aponte, L. y A. Guadarrama. 2003. Actividad de las enzimas pectinmetilesterasa, poligalacturonasa y celulasa durante la maduración de frutos de parchita maracuyá (Passiflora edulis f. flavicarpa Degener). Revista de la Facultad de Agronomía. (Maracay) 29(2): 145-160.
Arellano, L.A., C. Saucedo y L. Arévalo. 2005. Cambios bioquímicos y fisiológicos durante la maduración de frutos de zapote negro (Diospyros digyna Jacq.). Agrociencia 39(2): 173-181.
Ayaz, F.A., O. Demir, H. Torun, Y. Kolcuoglu and A. Colak. 2008. Caharacterizacion of polyphenoloxidase (PPO) and total phenolic contens in medlar (Mespilus germanica L.) fruit during ripening and over ripening. Food Chemistry 106(1): 291-298.
Belitz, H.D. y W. Grosch. 1997. Química de los alimentos. Segunda edición. Editorial Acribia. Zaragoza, España. 1.087 p.
Bernfelds, P. 1955. Amylase a y b. pp. 149-159 In: Colowick S.P., N.O. Kaplan (eds.). Methods in enzymology. Volume 1. Academic Press, Nueva York, USA. 835 p.
Bowers, J. 1992. Food theory and applications. Macmillan Publishing Company, New York, USA. 952 p.
Bradford, M. 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry (1-2)72: 248-254.
Brummell, D.A. and M.H. Harpster. 2001. Cell wall metabolism in fruit softening and quality and its manipulation in transgenic plants. Plant Molecular Biology 47(1-2): 311-340.
Castro, J.A., L.E. Baquero y C.E. Narváez. 2006. Catalasa, peroxidasa y polifenolxidasa de pitahaya amarilla (Acanthocereus pitajaya). Revista Colombiana de Química 35(1): 91-100.
Dueñas, Y., C. Narváez y L. Restrepo. 2008. Inhibición de lesiones por frío de pitaya amarilla (Acanthocereus pitajaya) a través del choque térmico: catalasa, peroxidasa y polifenoloxidasa. Acta Biológica Colombiana 13(1): 95-106.
Falguera, V., J. Pagán and A. Ibarz. 2011. Effect of UV irradiation on enzymatic activities and physicochemical properties of apple juices from different varieties. LWT - Food Science and Technology 44(1): 115-119.
Franco, G., J.R. Cartagena y G.A. Correa. 2013. Informe. Análisis de crecimiento del fruto de gulupa (Passiflora edulis Sims), en las condiciones ecológicas del bosque húmedo montano bajo de Colombia. Facultad de Ciencias Agrarias. Universidad Nacional de Colombia, Medellín. 12 p.
García, H.E. y V.C. Peña. 1995. La pared celular: componente fundamental de las células vegetales. Universidad Autónoma de Chapingo, México. 75 p.
García, C., G. Giraldo, H. Hurtado y C. Mendivil. 2006. Cinética enzimática de la polifenol oxidasa del banano (Gros Michel) en diferentes estados de maduración. Vitae 13(2): 13-19.
Guerrero, C.A. 2009. Inhibición de la actividad enzimática de la polifenol oxidasa extraída del banano (Cavendish Valery) mediante sistemas bifásicos acuosos con isoespintanol y ácido ascórbico. Tesis Magíster en Ciencia y Tecnología de Alimentos. Facultad de Ciencias Agropecuarias. Universidad Nacional de Colombia, Sede Medellín. 91 p.
Granados, J.R. 1994. Química avanzada Nuffield, ciencia de la alimentación. Editorial Reverté S.A. Barcelona. 172 p.
Haard, N.F. 1985. Características de los tejidos de plantas comestibles. pp. 861-867. En: Fennema, O.R. (ed.). Introducción a la Ciencia de los Alimentos. Editorial Reverté S.A. Barcelona.
Hagerman, A.E. and P.J. Austin. 1986. Continuous spectrophotometric assay for plant pectin methyl esterase. Journal of Agriculture and Food Chemistry 34(3): 440-444.
Instituto Colombiano de Normas Técnicas y Certificación. (Icontec). 1999. NTC 4624. Jugos de frutas y hortalizas. Determinación del contenido de sólidos solubles. Método refractométrico. Icontec, Bogotá. 9 p.
Menéndez, O., S.E. Lozano, M. Arenas, K.A. Bermúdez, A. Martínez y A. Jiménez. 2006. Cambios en la actividad de a-amilasa, pectinmetilestrasa y poligalacturonasa durante la maduración del maracuyá amarillo (Passiflora edulis var. flavicarpa Degener. Interciencia 31(10): 728-733.
Miller, G. 1959. Use of dinitrosalicylic acid reagent for determination of reducing sugar. Analytical Chemistry 31(3): 26-31.
Nelson, N. 1944. A photometric adaptation of the Somogyi method for determination of glucose. The Journal of Biological Chemistry 153: 378-380.
Lobo, M.G. 1995. Caracterización bioquímica de frutos de papaya (Carica papaya cv. Sunrise), hembra y hermafrodita, en relación con su aptitud al procesado por congelación. Tesis doctoral. Facultad de Farmacia. Universidad Complutense de Madrid. Madrid. 326 p.
Lobo, M. 2000. Papel de la variabilidad genética en el desarrollo de los frutales andinos como alternativa productiva. pp. 27-36. En: Memorias III Seminario de Frutales de Clima Frío Moderado. Centro de Desarrollo Tecnológico de Frutales - CDTF, Manizales.
Llorente, B.E. 2010. Un rol biológico propuesto para las misteriosas polifenol oxidasas vegetales. Tesis Doctor en Química Biológica. Facultad de Ciencias Exactas y Naturales. Departamento de Química Biológica. Universidad de Buenos Aires, Argentina. 88 p.
Oort, van M. 2010. Enzymes in bread making. pp. 103-143. In: Whitehurst, R.J. and Oort, van M. (ed.) Enzymes in Food Technology. Second edition. Wiley Blackwell Publishing, New Delhi, India. 360 p.
Ortiz, D.C. 2010. Estudio de la variabilidad genética en materiales comerciales de gulupa (Passiflora edulis f. edulis Sims) en Colombia. Tesis Magíster en Ciencias Agrarias. Facultad de Agronomía. Universidad Nacional de Colombia, Bogotá. 127 p.
Pelloux, J., C. Rustérucci and E.J. Mellerowicz. 2007. New insights into pectin methylesterase structure and function. Trends in Plant Science 12(6): 267-277.
Seymour; G. B. and K. C. Gross. 1966. Cell wall disassembly and fruit softening. Postharvest News Information. 7: 45N-52N.
Shiomi, S., L.S. Wamocho and S.G. Agong. 1996. Ripening characteristics of purple passion fruit on and off the vine. Postharvest Biology and Technology 7(1-2): 161- 170.
Tomás-Barberan, F.A. and J.C. Espin. 2001. Phenolic compounds and related enzymes as determinants of quality in fruits and vegetables. Journal of the Science of Food and Agriculture 81(9): 853-876.
Willats, W.G., L. McCartney, W. Mackie and J.P. Knox. 2001. Pectin: cell biology and prospects for functional analysis. Plant Molecular Biology 47(1-2):9-27.
How to Cite
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Download Citation
CrossRef Cited-by
1. Nunes de Jesus Onildo, Leila Soares Taliane, Augusto Girardi Eduardo, Castro Carriello Rosa Raul, Jorge de Oliveira Eder, Jos eacute da Cruz Neto Al iacute rio, Tebinka dos Santos Valeria, Roberto Pereira Oliveira Jo atilde o. (2016). Evaluation of intraspecific hybrids of yellow passion fruit in organic farming. African Journal of Agricultural Research, 11(24), p.2129. https://doi.org/10.5897/AJAR2016.10819.
Dimensions
PlumX
Article abstract page views
Downloads
License
Copyright (c) 2015 Revista Facultad Nacional de Agronomía Medellín

This work is licensed under a Creative Commons Attribution-NonCommercial 4.0 International License.
The journal allows the author(s) to maintain the exploitation rights (copyright) of their articles without restrictions. The author(s) accept the distribution of their articles on the web and in paper support (25 copies per issue) under open access at local, regional, and international levels. The full paper will be included and disseminated through the Portal of Journals and Institutional Repository of the Universidad Nacional de Colombia, and in all the specialized databases that the journal considers pertinent for its indexation, to provide visibility and positioning to the article. All articles must comply with Colombian and international legislation, related to copyright.
Author Commitments
The author(s) undertake to assign the rights of printing and reprinting of the material published to the journal Revista Facultad Nacional de Agronomía Medellín. Any quotation of the articles published in the journal should be made given the respective credits to the journal and its content. In case content duplication of the journal or its partial or total publication in another language, there must be written permission of the Director.
Content Responsibility
The Faculty of Agricultural Sciences and the journal are not necessarily responsible or in solidarity with the concepts issued in the published articles, whose responsibility will be entirely the author or the authors.