Common bean (Phaseolus vulgaris L.) yield response to chemical and biological fertilization in different localities of Colombia
Respuesta productiva del cultivo del fríjol (Phaseolus vulgaris L.) a la fertilización química y biológica en zonas productoras de Colombia
DOI:
https://doi.org/10.15446/rfnam.v71n3.72392Keywords:
Poultry manure, Mycorrhizae, Rhizobium, Phosphate rock (en)Gallinaza, Micorrizas, Rhizobium, Roca fosfórica (es)
The research was carried out in 2015 in five bean producing locations in Colombia. The objective was to evaluate the effect of different treatments of chemical and biological fertilization on the yield of climbing and bush beans. According to the results obtained, in Antioquia, it is possible to replace the chemical fertilization by biological fertilization in the climbing bean Corpoica LAS-106 and the bush bean Citará. In Cundinamarca, similar situation was presented with “Cargamanto Rojo”. In Santander, it was found that the combination of mycorrhizae (AMF) and Rhizobium improves the performance of the bush bean ICA-Rovirense (2839.5 t ha-1) and ICA-Radical-J1J1 (1955.7 t ha-1), with respect to national average yield (1.2 t ha-1). The use of biofertilizers (mycorrhizal fungi and Rhizobium) improved the yields in the bean crop, with the materials used (climbing and bush) and in the localities studied.
There is an additive effect in the applications of the biofertilizers evaluated, since it is a higher yield in the bean crop when these were applied individually combined.
La investigación se realizó en 2015 en cinco localidades productoras de frijol en Colombia. El objetivo fue evaluar el efecto de diferentes tratamientos de fertilización química y biológica sobre el rendimiento de frijoles volubles y arbustivos. De acuerdo con los resultados obtenidos, en Antioquia, es posible reemplazar la fertilización química por fertilización biológica en el frijol voluble Corpoica LAS-106 y el arbustivo Citará. En Cundinamarca, similar situación se presentó con el frijol “Cargamanto Rojo”. En Santander, se encontró que la combinación de micorrizas (AMF) y Rhizobium mejora el rendimiento de los fríjoles arbustivos ICA-Rovirense (2839,5 t ha-1) e ICA- Radical-J1J1 (1955,7 t ha-1), con respecto al rendimiento promedio nacional (1,2 t ha-1). El uso de biofertilizantes (hongos formadores de micorriza y Rhizobium) mejoró los rendimientos en el cultivo del frijol, con los materiales utilizados (volubles y arbustivos) y en las localidades estudiadas. Existe un efecto aditivo en las aplicaciones de los biofertilizantes evaluados, ya que se observó un mayor rendimiento en el cultivo de frijol cuando estos se aplicaron combinados que individualmente.
Recibido: 24 de mayo de 2018; Aceptado: 17 de julio de 2018
ABSTRACT
The research was carried out in 2015 in five bean producing locations in Colombia. The objective was to evaluate the effect of different treatments of chemical and biological fertilization on the yield of climbing and bush beans. According to the results obtained, in Antioquia, it is possible to replace the chemical fertilization by biological fertilization in the climbing bean Corpoica LAS-106 and the bush bean Citará. In Cundinamarca, similar situation was presented with "Cargamanto Rojo". In Santander, it was found that the combination of mycorrhizae (AMF) and Rhizobium improves the performance of the bush bean ICA-Rovirense (2839.5 t ha-1) and ICA-Radical-J1J1 (1955.7 t ha-1), with respect to national average yield (1.2 t ha-1). The use of biofertilizers (mycorrhizal fungi and Rhizobium) improved the yields in the bean crop, with the materials used (climbing and bush) and in the localities studied. There is an additive effect in the applications of the biofertilizers evaluated, since it is a higher yield in the bean crop when these were applied individually combined.
Keywords:
Poultry manure, Mycorrhizae, Rhizobium, Phosphate rock.RESUMEN
La investigación se realizó en 2015 en cinco localidades productoras de frijol en Colombia. El objetivo fue evaluar el efecto de diferentes tratamientos de fertilización química y biológica sobre el rendimiento de frijoles volubles y arbustivos. De acuerdo con los resultados obtenidos, en Antioquia, es posible reemplazar la fertilización química por fertilización biológica en el frijol voluble Corpoica LAS-106 y el arbustivo Citará. En Cundinamarca, similar situación se presentó con el frijol "Cargamanto Rojo". En Santander, se encontró que la combinación de micorrizas (AMF) y Rhizobium mejora el rendimiento de los fríjoles arbustivos ICA-Rovirense (2839,5 t ha-1) e ICA- Radical-J1J1 (1955,7 t ha-1), con respecto al rendimiento promedio nacional (1,2 t ha-1). El uso de biofertilizantes (hongos formadores de micorriza y Rhizobium) mejoró los rendimientos en el cultivo del frijol, con los materiales utilizados (volubles y arbustivos) y en las localidades estudiadas. Existe un efecto aditivo en las aplicaciones de los biofertilizantes evaluados, ya que se observó un mayor rendimiento en el cultivo de frijol cuando estos se aplicaron combinados que individualmente.
Palabras clave:
Gallinaza, Micorrizas, Rhizobium, Roca fosfórica.Bean (Phaseolus vulgaris L.) is considered as one of the basic products of the peasant economy of small and medium-sized producers, located especially in the Andean region, with limitations in crop yields, high incidence of pests and diseases, and lack of good quality seeds (Pachón, 2010; Tofiño et al., 2016; FAO, 2016).
According to Fenalce (2016), in 2015 94,341 hectares of bean were planted in Colombia, with a yield of 101,497 tons; 93% of the plantations were located in the Andean region, 5.6% in the Inter-Andean Valleys, and 1.4% in the Caribbean region. Approximately, 65% of the national bean yield comes from the climbing varieties of cold and moderate cold climates, and the remaining 35% corresponds to bush varieties in medium and warm climates. In the other hand, 50% of production is concentrated in the departments of Antioquia, Santander, Huila, Tolima and Nariño.
In the tropics, the majority of the soils are from extremely up to strongly acid (pH<5.5), rich in exchangeable Al, and low in nutrients (Barber, 1995; Zapata, 2004; Toledo, 2012; Osorio, 2018), which restricts agricultural productivity. To compensate these problems, it is necessary to apply high amounts of lime and fertilizers, which increase yield costs (Osorio, 2018).
The medium-climate soils (1000-2000 m of altitude) in Colombia are of low to medium fertility and have some limitations for the normal growth of crops, since in general, their pH tend to be strongly acid (4.2-5.5), high in Al, low to medium of assimilable K (<0.3 cmolc kg-1), low in exchangeable Mg (<1.0 cmolc kg-1), and low in organic matter (<5%). The usable P content presents predominance towards low values (<15 mg kg-1) (Tamayo and Osorio, 2014).
Moderate cold climate soils have high anionic exchange capacity, high phosphate binding, high organic matter content (<15%), but a very low mineralization of the organic matter (<1%). These soils have strongly acidic pH (4.0-5.5) and low levels of exchangeable bases, and in many cases, imbalances among the bases (Tamayo and Osorio, 2014).
It is considered that the use of biofertilizers could improve the quality of the soils and, therefore, the yield of the crops. Corpoica has been working with arbuscular mycorrhizal fungi (AMF), and bacteria of the genus Rhizobium, considered at the moment and worldwide, as biofertilizers for most of the crops. The combined use of both types of microorganisms, improves the yield conditions in more efficiently way than with the individual use of them, and are fundamental in the programs of integrated soil and crop management (Tamayo, 2016). According to what it was mentioned above, a study was established to determine the effect of the application of biofertilizers (mycorrhizal fungi and Rhizobium) on the yield of climbing and bush beans, in different producing localities of this specie in Colombia.
The use of microorganisms in the form of biofertilizers can have a positive effect on the yield in the bean crop in Colombia.
MATERIALS AND METHODS
The study was carried in 2015 (first semester), in different localities in the departments of Antioquia, Cundinamarca and Santander. In Antioquia, two experimental plots were established in two localities: CI La Selva (altitude of 2120 m, annual average temperature of 17 °C, average annual rainfall of 1850 mm, at 06°08'06''N, 75°25'03W), with climbing beans ICA-Viboral and Corpoica LAS-106 (both at a planting distance of 0.23 m among plants and 1.2 m among rows). The other locality was CI El Nus (altitude of 848 m, annual average temperature of 24 °C, average annual rainfall of 2500 mm, at 06°26'17.2''N, 74°49'32.1''W), with the bush bean varieties Quimbaya and Citará (both at a planting distance of 0.15 m among plants and 0.5 m among rows), in which it was evaluated the effect of several treatments with biological fertilizers. The treatments used were: Organic matter (poultry manure) (2 t ha-1); Rhizoglomus sp. (15 g per plant), with a concentration of 250 spores g-1, with 50 infective mycorrhiza propagules g-1; commercial strains of Rhizobium (100 bacteria g-1) (0.01 L per kg of seed) and/or with phosphate rock (PR) (600 kg ha-1), in simple and combined form. All treatments received 20 g of KCl per linear meter, except for the chemical farmer treatment (control) (350 kg ha-1 of 10-30-10). Each experimental unit consisted of six rows, 10 m long and 0.6 m wide each. A randomized complete block experimental design with four replications, was used.
In Cundinamarca, a plot was established in the municipality of Pasca (at an altitude of 2180 m, annual average temperature of 17 °C, an average annual rainfall of 1100 mm, at 4°18'27"N 74°18'03"W), with climbing bean "Cargamanto Rojo" (at a planting distance of 0.23 m among plants and 1.2 m among rows). The treatments used were: Organic matter (poultry manure) (2 t ha-1); with Rhizoglomus sp. (15 g per plant), with a concentration of 250 spores g-1, with 50 infective mycorrhiza propagules g-1; commercial strains of Rhizobium (100 bacteria g-1) (0.01 L per kg of seed) and/or with phosphate rock (PR) (600 kg ha-1), in simple and combined form. All treatments received 20 g of KCl per linear meter, except for the chemical farmer treatment (control) (350 kg ha-1 of 10-30-10). Each experimental unit consisted of six rows, 10 m long and 0.6 m wide each. A randomized complete block experimental design with four replications, was used.
In Santander, two experimental plots were established in two localities: CI El Arsenal (altitude of 1450 m, annual average temperature of 22 °C, average annual rainfall of 1292 mm, at 6°40'05"N 72°42'00"W), with the bush bean variety ICA-Rovirense. The other locality was Curití (at an altitude of 1409 m, annual average temperature of 20 °C, an average annual rainfall of 1500 mm, at 6°36'16"N 73°04'05"W), with the bush bean variety ICA- Radical-J1J1. In both localities were used a planting distance of 0.15 m among plants and 0.5 m among rows, in which the effect of three strains of Rhizobium (P4, P8, and P14), and two inoculum of mycorrhiza MVA (Rhizoglomus occultum and Acaulospora spp.) were evaluated on the yield of bush bean varieties, ICA-Rovirense and Radical-JIJI. Each experimental unit consisted of six rows, 10 m long and 0.6 m wide. A randomized complete block experimental design with four replications was used. The study consisted in the evaluation of seven treatments; in Curiti was included a control, that involved the application of the combination of Trichoderma lignorum, and a mixture of mycorrhizal fungi (Rhizoglomus occultum and Acaulospora spp.), plus the inoculation of the seeds with Rhizobium sp.
RESULTS AND DISCUSSION
At C.I. La Selva, when performing a combined analysis during two consecutive cycles, in Corpoica 106 and ICA-Viboral, significant differences were present among treatments. As it can be seen in Table 1, the yield obtained with chemical fertilization in the variety Corpoica 106 was equal to that obtained with organic and biological fertilization, either with double inoculation, mycorrhizae plus Rhizobium, and/or with the application of PR. This agrees with several authors who report a positive effect of the different strains, both in their simple as in its combined forms, presenting the greatest effects when double inoculations were used (Saravesi et al., 2014; Galindo and Clavijo, 2009; Caldera et al., 2013; Clua et al., 2013; Granda et al., 2016; Romero et al., 2016).
Table 1: Yield of climbing beans Corpoica-LAS 106 and ICA-Viboral, during two consecutive cycles. CI La Selva.

It should be noted that the treatment with less yield was the one in which no poultry manure was applied, for both bean materials. This aspect is important due to the fact that, when the poultry manure is combined with inoculations of Rhizobium and mycorrhizae, the first one can act as a stimulator. In the variety Corpoica LAS-106, chemical fertilization can be replaced with the use of biofertilizers; contrary, the ICA-Viboral variety, responded better to the application of chemical fertilizer (350 kg ha-1 of 10-30-10) than to the application of biofertilizers. According to Osorio (2016), arbuscular mycorrhizal fungi can improve the ability of the root system to absorb nutrients and improve the effect of phosphate amendments. Likewise, the rhizobium-legume association is considered a highly efficient process in biological fixation of atmospheric nitrogen (BNF); it is estimated that nitrogen fixation varies from 24 to 584 kg ha-1; it has the capacity to supply up to 90% of the needs of the plant (Ángeles-Núñez and Cruz-Acosta, 2015). However, Osorio (2018) reports that there are differences in mycorrhizal dependence among cultivars of the same species.
The bean yield with this treatment was statistically superior to the different combinations of Rhizobium, phosphate rock and mycorrhizae (Table 1). As in the variety Corpoica LAS-106, in the ICA-Viboral, there was a significant response when poultry manure was applied, being this an activator of the biological-mineral fertilization. Organic fertilizers are a crucial element for the regulation of many processes related to agricultural productivity and can be a complement or replacement of synthetic fertilizers (Ramos and Terry, 2014). It may be argued that in the poultry manure, the microorganisms producers of organic acids can make more available the phosphate ions released from the phosphate rock, and thus improve yield (Osorio and Habte, 2013; Ramírez et al., 2013; Tamayo and Osorio, 2017). In both materials, yield per hectare during the two growing cycles was acceptable and, in some cases, exceeded the yields of the region (1.2 t ha-1).
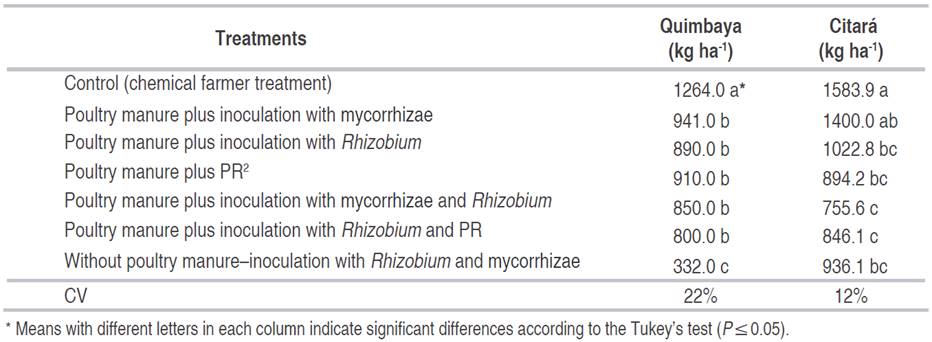
In medium climate conditions (CI El Nus) (Table 2), the Quimbaya and Citara bean materials showed a better yield response, when the control treatment (chemical)was applied, due to the soils of this area are low in fertility, very low in organic matter and exchangeable bases, and with acid pH. Although, it has been reported that in soils with very low organic matter there is a better response to organic applications than when applying chemical sources (Ramírez et al., 2008; Ramos and Terry, 2014; Hartmann et al., 2014; Guénon and Gros, 2015), In this study, the application of the biofertilizers was not enough to obtain the yields that were achieved with the chemical treatment, possibly because the applied doses were low. The treatments without poultry manure produced the lowest yields (936 and 352 kg ha-1) for the bush varieties Citara and Quimbaya, respectively. A similar situation occurred in the locality of C.I. La Selva with climbing materials. The Quimbaya variety did not respond as significantly to the biological-mineral sources as did the climbing beans of moderate cold climate; however, there are reports of other mid-climate locations where their response has been positive. In all the varieties, the effect of the poultry manure on the yields is substantial (Table 2).
Table 2: Effect of biological-mineral fertilization on yield of bush bean in soils of medium climate. CI El Nus.
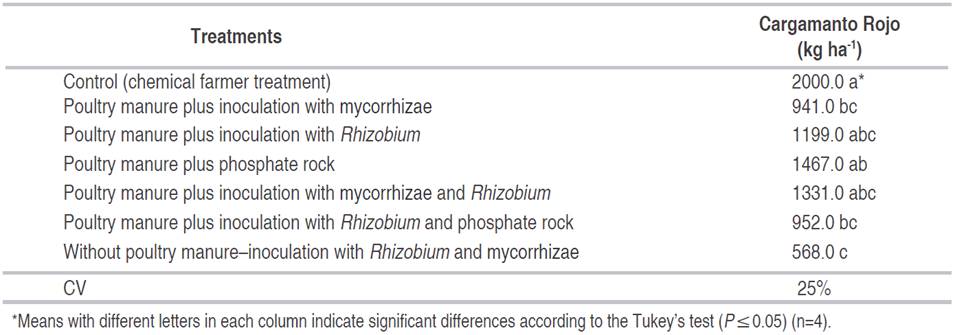
In Pasca, the yield in the bean "Cargamanto Rojo" fluctuated between 568 and 2000 kg ha-1. Table 3 shows significant differences among the treatments; the chemical farmer treatment (control), does not differ statistically from the treatments of poultry manure plus Rhizobium, phosphate rock and mycorrhizae and Rhizobium. These yields, despite being from medium to low, the trend they present is the same of that obtained in C.I. La Selva with the ICA-Viboral bean, probably because poultry manure could improve the physical and biological conditions and help the activity of mycorrhiza and Rhizobium in the soil.
Table 3: Effect of organic and biological fertilization on the yield of climbing bean. Municipality of Pasca.
In Table 4, it is observed that in the locality C.I. "El Arsenal", there were statistical differences (P≤ 0.05) among treatments, with a mean of 2354.5 kg ha-1 and a coefficient of variation of 14.67%.
Table 4: Average yield (kg ha-1) in Santander with regional bean varieties.
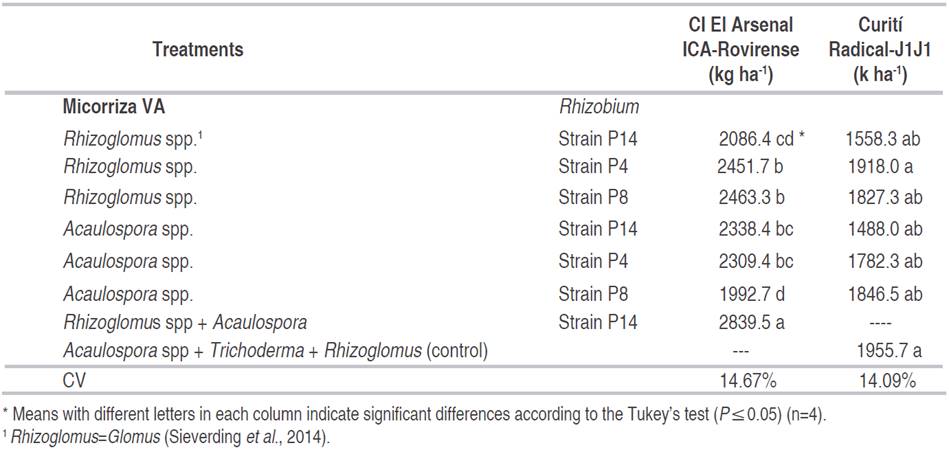
The combination of AMF mycorrhizae (Rhizoglomus spp. + Acaulospora) and Rhizobium P14 strain, presented the highest yield (2839.5 kg ha-1), while the lowest yield was shown in the treatment that included the Acaulospora combination and the Rhizobium P8 strain, with 1992.7 kg ha-1. The combined use of both types of microorganisms (Rhizobium and mycorrhizal fungi) produces better effects than the individual use of them, the use of microorganisms in the form of biofertilizers improves soil nutrition and plant growth (Grageda et al., 2012; Elein et al., 2013; Lozano et al., 2015; Gardezi et al., 2016). In the locality of Curití, no significant differences among treatments were observed, in relation to the average yield of bean in kg ha-1.
The highest effectiveness with respect to the yield was detected in the locality CI "El Arsenal", probably due to the quality of the organic medium, to the presence of existing beneficial microorganisms, which give the root greater capacity to explore the soil in search of water and nutrients, that results in higher yields; these results are similar to those obtained by Flores et al. (2014) in Stylosanthes guianensis. This allows to consider, that the combination of compost and biological agents in the management of the nutrition of the cultivated plants is beneficial, which represents for the farmers of bean, to produce more quantity and quality of food at a lower cost, preserving the environment.
CONCLUSIONS
The use of biofertilizers (mycorrhizae fungi and Rhizobium) improved yields in the bean crop, with the materials used (climbing and bush beans) and in the localities studied.
There is an additive effect in the applications of the biofertilizers evaluated, since a higher yield was observed in the bean crop when these were applied combined than individually.
Disclaimer of Liability
The source of research funding was obtained by the Corporacion Colombiana de investigación Agropecuaria. The authors state that the research was carried out in the absence of commercial or financial relationships that could be interpreted as a possible conflict of interests.
ACKNOWLEDGEMENTS
The authors thank farmers in the municipalities where the evaluations were carried out, for their participation and collaboration in the research trials.
REFERENCES
References
Ángeles-Núñez JG and Cruz-Acosta T. 2015. Aislamiento, caracterización molecular y evaluación de cepas fijadoras de nitrógeno en la promoción del crecimiento de fríjol. Revista Mexicana de Ciencias Agrícolas 6: 929-942.
Barber SA. 1995. Soil Nutrients Bioavailability. A mechanistic approach. New York, John Wiley and sons. 384 p. ISBN-13:978- 0471587477
Caldera E, Acosta K, Garcés G, Petit B, Gutiérrez W and Pérez C. 2013. Respuesta del cultivo fríjol (Vigna unguiculata L. Walp) variedad Catatumbo a la inoculación con micorrizas nativas y comerciales bajo condiciones controladas. Universidad del Zulia, Facultad de Agronomía, Laboratorio de Microbiología Agrícola 3(1- 2): 157-164. ISSN 2244-7334
Clua A, Olgati J and Beltrano J. 2013. Evaluación de la doble inoculación Bradyrhizobium-micorrizas y el uso de fitoterápicos de semilla en el crecimiento, eficiencia de inoculación y el rendimiento de un cultivo de soja. Revista Investigación Agropecuaria 39(3): 250- 258. Disponible en: https://bit.ly/2vkh1vi
FAO. 2016. Estado de inseguridad alimentaria en el mundo 2015. Disponible en: http://www.fao.org/3/a-i4646s.pdf
Federación Nacional de Cultivadores de Cereales y Leguminosas - FENALCE. 2016. Departamento económico y apoyo a la comercialización. Estadísticas. Indicadores cerealistas. Fenalce, Cundinamarca, Colombia. 85 p.
Flores GC, Ramírez JF, González PJ and Hernández I. 2014. Co-inoculation of rhizobium strains and one of the arbuscular micorrhizal fungus on Stylosanthes guianensis cv. CIAT-184. Cuban Journal of Agricultural Science (3): 297-300.
Galindo PJ and Clavijo P. 2009. Phenology of pea crop (Pisum sativum L. var. Santa Isabel) in the Bogotá plateau at open field and under plastic cover Corpoica. Ciencia y Tecnología Agropecuaria 10(1): 5-15.
Gardezi AK, Márquez BS, Martínez M, Flores M, Escalona M, Larque SM and Almaguer VG. 2016. Soil contamination and its effects on beans (Phaseolus vulgaris L.) growth affected by organic matter, and associated with Glomus intraradices. European Scientific Journal 107-118 Special Edition.
Grageda CO, Díaz FA, Pena CJ and Vera NJ. 2012. Impacto de los biofertilizantes en la agricultura. Revista Mexicana de Ciencias Agrícolas 3(6): 1261-1274.
Guénon R and Gros R. 2015. Increasing the maturity of compost used affects the soil chemical properties and the stability of microbial activity along a mediterranean post-fire chronosequence. European Journal of Soil Biology 66: 1-10. doi: 10.1016/j.ejsobi.2014.11.002
Granda KI, Nápoles MC, Robles AR, Alvarado-Capó Y and Torres R. 2016. Respuesta de Phaseolus vulgaris cv. Mantequilla a la inoculación de cepas de Rhizobium nativas de Ecuador en casas de cultivo. Centro Agrícola 43(4): 49-56.
Hartmann M, Frey B, Mayer J, Mäder P and Widmer F. 2014. Distinct soil microbial diversity under long-term organic and conventional farming. Microbial Ecology 9(5): 1177-1194. doi: 10.1038/ismej.2014.210.
Lozano SJ, Armbrecht I and Montoya L. 2015. Hongos formadores de micorrizas arbusculares y su efecto sobre la estructura de los suelos en fincas con manejos agroecológicos e intensivos. Acta Agronómica 64(4): 289-296. doi: 10.15446 /acag. v64n4.46045
Osorio NW and Habte M. 2013. Synergistic effect of a phosphate solubilizing fungus and an arbuscular mycorrhizal fungus on Leucaena seedlings in an oxisol fertilized with rock phosphate. Botany 91(4): 274-281. doi: 10.1139/cjb-2012-0226
Osorio NW. 2016. Biofertilización: Una alternativa sostenible para el manejo de la nutrición vegetal en los suelos tropicales. Pp30. En: Resúmenes. XVIII Congreso Colombiano de la Ciencia del Suelo. Sociedad Colombiana de la Ciencia del Suelo.Villa de Leyva. Boyacá.
Osorio NW. 2018. Manejo de nutrientes en suelos del trópico. Tercera edición. Vieco SAS, Medellín. 439 p.
Pachón H. 2010. El impacto nutricional de cultivos biofortificados o cultivos con mayor calidad nutricional. Cali, Colombia: CIAT. 14 p. ISBN 978-958-694-100-6
Ramírez GM, Roveda HG, Bonilla BR, Cabra JL, Peñaranda RA, López JM, Tamayo VA, Navas GE and Díaz DC. 2008. Uso de microorganismos con potencial como biofertilizantes en el cultivo de mora. Bogotá: Corpoica. C.I. Tibaitatá 64 p. ISBN: 978-958-8311- 76-0
Ramírez JG, Osorno L, Osorio W and Morales JG. 2013. Alternativas microbiológicas para mejorar el crecimiento del Caupí. Revista Facultad Nacional de Agronomía Medellín 66(2): 7035-7044.
Ramos, AD and Terry AE. 2014. Generalidades de los abonos orgánicos: Importancia del bocashi como alternativa Nutricional para suelos y plantas. Cultivos Tropicales 35(4): 52-59.
Romero GV, García OV, Hernández and Sánchez YJ. 2016. Respuesta de Phaseolus vulgaris a microorganismos promotores de crecimiento vegetal. Scientia Agropecuaria 7(3): 313-319. doi: 10.17268/sci.agropecu.2016.03.20
Saravesi K, Ruotsalainen A and Cahill JF. 2014. Contrasting impacts of defoliation on root colonization by arbuscular mycorrhizal and dark septate endophytic fungi of Medicago sativa. Mycorrhiza 24(4): 239–245. doi: 10.1007/s00572-013-0536-5
Sieverding E, Silva GA, Berndt R and Oehl F. 2014. Rhizoglomus, a new genus of the Glomeraceae. Mycotaxon 129: 373-386. doi: 10.5248/129.373
Tamayo VA. 2016. Descomposición de hojarasca y liberación de nutrientes en plantaciones de aguacate cv. Hass en función de la inoculación con un hongo saprofito en tres pisos térmicos. Ph.D. Disertación, Universidad Nacional de Colombia, Facultad de Ciencias Agrarias, Medellín, Colombia. 125 p.
Tamayo VA and Osorio W. 2014. Nutrición y Fertilización. En: Actualización Tecnológica y Buenas Prácticas Agrícolas (BPA) en el Cultivo de Aguacate. Corporación Colombiana de Investigación Agropecuaria–Corpoica; Secretaria de Agricultura y Desarrollo Rural de Antioquia. Segunda edición. Medellín, Colombia. pp. 183-212. ISBN 978-958-8711-50-8.
Tamayo VA and Osorio W. 2017. Coinoculation with an arbuscular mycorrhizal fungus and a phosphate solubilizing fungus promotes plant growth and phosphate uptake of avocado plantlets at nursery. Botany 95(5): 539–545 doi: 10.1139/cjb-2016-0224
Terry E A, Ruiz J, Tejeda T and Díaz de Armas M. 2013. Respuesta del cultivo de la habichuela (Phaseolus vulgaris L. var. Verlili) a la aplicación de diferentes bioproductos. Cultivos Tropicales 34(3): 05-10.
Tofiño-Rivera A, Pastrana-Vargas I, Melo-Ríos A, Beebe S and Tofiño-Rivera R. 2016. Rendimiento, estabilidad fenotípica y contenido de micronutrientes de fríjol biofortificado en el Caribe seco colombiano. Corpoica. Ciencia y Tecnología Agropecuaria 17(3): 309-329 doi: 10.21930/rcta.vol17_num3_art:511
Toledo JM. 2012. Manual para la evaluación agronómica. Red internacional de evaluación de pastos tropicales. Centro Internacional de Agricultura Tropical (CIAT), Cali, CO. 155 p.
Zapata RD. 2004. Química de la acidez del suelo. Universidad Nacional de Colombia, Medellín. 205 p.
How to Cite
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Download Citation
CrossRef Cited-by
1. Hernando José Bolívar-Anillo, Ezzanad Abdellah, Gesiane da Silva Lima, Inmaculada Izquierdo-Bueno, Javier Moraga, Gabriel Franco dos Santos. (2021). Neotropical Endophytic Fungi. , p.93. https://doi.org/10.1007/978-3-030-53506-3_5.
2. Marie Noela Enyoe Olougou, Nora Ambotaba Kungang, Solange Takwi Ndzeshala, Mercy Abwe Ngone, Christopher Ngosong. (2025). Exploring the fertilizer value of vermicompost and poultry manure to enhance soil health and yield of sweet bitter-leaf Vernonia hymenolepis. Discover Soil, 2(1) https://doi.org/10.1007/s44378-025-00073-0.
Dimensions
PlumX
Article abstract page views
Downloads
License
Copyright (c) 2018 Alvaro Tamayo Vélez

This work is licensed under a Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International License.
The journal allows the author(s) to maintain the exploitation rights (copyright) of their articles without restrictions. The author(s) accept the distribution of their articles on the web and in paper support (25 copies per issue) under open access at local, regional, and international levels. The full paper will be included and disseminated through the Portal of Journals and Institutional Repository of the Universidad Nacional de Colombia, and in all the specialized databases that the journal considers pertinent for its indexation, to provide visibility and positioning to the article. All articles must comply with Colombian and international legislation, related to copyright.
Author Commitments
The author(s) undertake to assign the rights of printing and reprinting of the material published to the journal Revista Facultad Nacional de Agronomía Medellín. Any quotation of the articles published in the journal should be made given the respective credits to the journal and its content. In case content duplication of the journal or its partial or total publication in another language, there must be written permission of the Director.
Content Responsibility
The Faculty of Agricultural Sciences and the journal are not necessarily responsible or in solidarity with the concepts issued in the published articles, whose responsibility will be entirely the author or the authors.






















