Publicado
Descripción matemática del desempeño electroanalítico de nanopartículas de derivados de níquel en la determinación cualitativa y cuantitativa de metanol
The mathematical description for the electroanalytical action of Ni-containing nanoparticles by quantitative and qualitative methanol determination
DOI:
https://doi.org/10.15446/rcciquifa.v44n1.54233Palabras clave:
Sensores electroquímicos, Metanol, Nanopartículas de níquel, Polímeros conductores y compositos, Estado estacionario estable (es)Electrochemical sensors, Methanol, Nickel-containing nanoparticles, Conducting polymers and composites, Stable steady-state (en)
Descripción matemática del desempeño electroanalítico de nanopartículas de derivados de níquel en la determinación cualitativa y cuantitativa de metanol
The mathematical description for the electroanalytical action of Ni-containing nanoparticles by quantitative and qualitative methanol determination
Reza Ojani b
Jahanbakhsh Raoof b
Ebrahim Zarei b
Vasyl´ V. Nechyporuk a
Petró I. Yagodynets´ a
Sílvio C. de Oliveira c
a Universidad Nacional de Chernivtsi, Ucrania * Correo electrónico: nightwatcher2401@gmail.com
b Universidad de Mazandarán, República Islámica de Irán
c Universidade Federal de Mato Grosso do Sul, Brasil
Recibido para evaluación: 24 de mayo de 2014.
Aceptado para publicación: 5 de noviembre de 2014.
Resumen
En este trabajo se desarrolló y se analizó, por medio de la teoría de estabilidad lineal y del análisis de bifurcaciones, el modelo matemático con que fue descrito el desempeño de nanopartículas de los derivados de níquel (solas y en compositos con el polímero conductor) en la determinación de metanol en el medio alcalino. Mediante el modelaje matemático, se derivaron las condiciones de estabilidad del estado estacionario, e inferidas las causas generales del comportamiento oscilatorio y monotónico. Los resultados del modelaje se compararon con los datos experimentales.
Palabras clave: sensores electroquímicos, metanol, nanopartículas de níquel, polímeros conductores y compositos, estado estacionario estable.
Summary
In this work, the mathematical model for the electroanalytical action of Ni-containing nanoparticles (by themselves and in a composite with a conducting polymer) in electrochemical qualitative and quantitative methanol detection in alkaline media is developed and analyzed by using of linear stability theory and bifurcation analysis. By the mathematical modeling, the steady-state stability conditions (the most exact sensing action requirements) and the causes for oscillatory and monotonic instabilities are derived. The result of the modeling is compared with the experimental data.
Key words: electrochemical sensors, methanol, nickel-containing nanoparticles, conducting polymers and composites, stable steady-state.
Introducción
La determinación cuantitativa de metanol es de interés relevante en los aspectos químicos de las industrias alimentaria, enzimática y del vino, bien como en investigaciones clínicas y forenses. Por ejemplo, el metanol es usado ilegalmente con mucha frecuencia en las bebidas alcohólicas falsificadas. El consumo de metanol lleva a la intoxicación, causada por la acumulación de metabolitos tóxicos, como formaldehído y ácido fórmico [1]. Otrosí, la oxidación electrocatalítica de metanol es el tema de investigación extensa con énfasis en la construcción de elementos de combustible [2]. Últimamente, estas investigaciones están envolviendo la electrooxidación de metanol en los valores altos de pH [3]. El uso del medio alcalino para la electrooxidación de metanol tiene sus ventajas, como mejor eficiencia y mayor escogencia de materiales de electrodos [4-8].
Sin embargo, para la electrooxidación de metanol sobre la mayoría de los electrodos no modificados es preciso aplicar el sobrevoltaje significante [9]; por eso se procuran los materiales efectivos capaces de disminuirlo y los compuestos de níquel, como materiales relativamente baratos, pueden ser usados para tal caso [10].
Los compuestos de níquel, principalmente sus óxidos e hidróxidos, son ampliamente investigados por causa de su posible aplicación en películas electrocrómicas, materiales ópticos, fotocatalizadores, etc. El uso de muestras recogidas depende de su composición, morfología y estructura; por ejemplo, las nanopartículas tienen mejores aplicaciones electrocatalíticas que las obtenidas en otro estado. Existen muchos reportes sobre la obtención de nanopartículas de compuestos de níquel [11-15], pero las metodologías que incluyen la transformación de polvo, con la dispersión, no dan partículas para su aplicación electroquímica. Entonces, la metodología de la electrodeposición de nanopartículas de níquel sobre un electrodo poroso o la confección de un revestimiento con su próxima oxidación es la mejor técnica.
Recientemente, las nanopartículas de níquel fueron depositadas sobre el electrodo de carbono vítreo y polímeros conductores [16-25] -siendo después oxidadas hasta el hidróxido de níquel (II)- y los compositos obtenidos mostraron la excelente capacidad de catalizar la oxidación de níquel según el mecanismo:
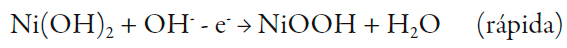 | [1] |
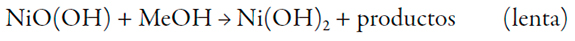 | [2] |
y si las nanopartículas están depositadas sobre la capa del polímero conductor, también ocurren las etapas:
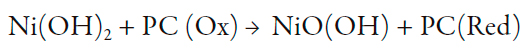 | [3] |
 | [4] |
Otro problema pueden ser las inestabilidades (oscilatoria y monotónica) que se observaron tanto durante la electrooxidación de metanol [26], como en cuanto al desempeño de sensores y biosensores, basados en polímeros conductores [27-29]. Su realización dará influencia tanto en la capacidad electrocatalítica del revestimiento obtenido, como en la exactitud del revestimiento obtenido; así, para evitar su acción negativa, o usar la positiva, es preciso determinar el mecanismo de su realización, o sea, determinar las condiciones generales de su realización. Antes, tales fenómenos tenían explicación fenomenológica, porque faltaba una base teórica fuerte, que solo se puede obtener con el desarrollo y análisis del modelo matemático, capaz de describir de forma adecuada los procesos en el sistema. Otrosí, una explicación fenomenológica solo es válida para un sistema concreto, mientras que el modelo matemático puede describir no solo un sistema concreto, sino también los semejantes.
En este trabajo será representado el modelo de desempeño del sensor electroquímico de metanol, basado en nanopartículas de derivados de níquel, descrito en [16-22], y los resultados de modelaje son comparados con los datos experimentales y con los datos de otros modelos de procesos semejantes, descritos en [30-35].
Este estudio es necesario para la mejor comprensión del proceso de electrooxidación de metanol (catalizada o no), bien como del desempeño de sus sensores electroquímicos, lo que va a servir para hacerlos más precisos, sensibles y exactos, y el proceso más eficiente. También, el estudio matemático sirve para comparar el desempeño de este sistema (y de semejantes) con los otros, sin experimentos difíciles.
Sistema y su modelo
Para la descripción matemática del sensor electroquímico de metanol, basado en nanopartículas de derivados de níquel en el medio alcalino en el modo potenciostático, introducimos tres variables:
c - la concentración del alcohol en la capa presuperficial;
ΘN - el grado de recubrimiento de la superficie por las partículas del óxido de níquel (II);
a - la concentración del álcali en la capa presuperficial.
Para simplificar el modelo, suponemos que la solución esté intensamente agitada y que el electrolito de soporte esté en exceso (para menospreciar las influencias hidrodinámicas). También se supone que el perfil concentrado de la capa presuperficial sea lineal y su espesor constante e igual a δ.
Metanol entra en la capa presuperficial por medio de su difusión y sale de allá por medio de su reacción con el óxido-hidróxido de níquel (III). Así siendo, su ecuación de balance se ve como:
 | [5] |
siendo Δ: el coeficiente de difusión, cb: la concentración de metanol en el interior de la solución y r2: la velocidad de la reacción de metanol.
El hidróxido de níquel (ІІ) se forma en la reacción del oxi-hidroxicompuesto con el alcohol. Su concentración disminuye en cuanto a su oxidación. Así, su ecuación de balance será descrita como:
 | [6] |
Siendo r1 la velocidad de la oxidación de hidróxido de níquel (II),  la concentración máxima de sus partículas.
la concentración máxima de sus partículas.
El hecho de que las nanopartículas dopantes, intercaladas en la matriz, eran menos activas que las depositadas sobre ella (observado en [22]), es explicado por el fenómeno de que la matriz polimérica, en la que las nanopartículas poliméricas son intercaladas, bloquea parcialmente de su contacto con el analito (en este caso, metanol).
El álcali entra en la capa presuperficial por medio de su difusión. Como los alcoholes alifáticos sin grupos aceptores no reaccionan con las bases, su concentración solo disminuye en cuanto a la reacción electroquímica. Así siendo, la ecuación de balance de su concentración será descrita como:
 | [7] |
Siendo D el coeficiente de su difusión y аb su concentración en el interior de la solución. Las velocidades de las respectivas reacciones pueden verse como:
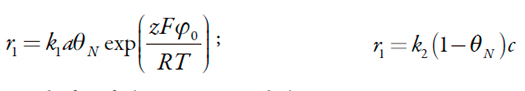 | [8-9] |
Siendo k1 y k2 las constantes de las respectivas reacciones, z la cantidad de electrones transferidos, F el número de Faraday, φ0, el salto de potencial en la capa doble, comparado al de carga cero.
Resultados y discusión
El comportamiento del sistema con la determinación electroquímica de metanol con la ayuda del sensor, basado en las nanopartículas de derivados de níquel, será investigado por medio del análisis del conjunto de ecuaciones (5-7) por medio de la teoría de estabilidad lineal. La matriz funcional de Jacobi, cuyos elementos son calculados para el estado estacionario, puede verse como:
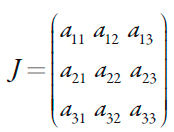 | [10] |
 | [11-19] |
Para evitar la aparición de expresiones grandes, introducimos las nuevas variables, de modo que el determinante de la matriz se escribe así:
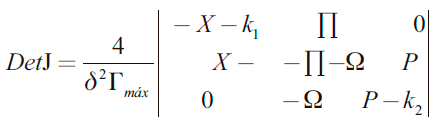 | [20] |
Usando el criterio de estabilidad de Routh-Hurwitz y la inecuación Det J < 0, obtenemos la condición de estabilidad de estado estacionario como:
 | [21] |
Se puede ver que todas las variables en la expresión, menos Ω, solo obtienen los valores positivos, lo que significa que la condición principal de estabilidad de estado estacionario es la ausencia de influencias en la capa doble de la oxidación electroquímica de níquel (II) hasta níquel (III).
La inecuación (21) confirma los datos de los artículos [16] y [22]. El aumento de la velocidad de la formación de sitios activos que se observa en cuanto a la aceleración de la difusión de álcali (aumento del valor de k2) favorece la estabilidad de estado estacionario y, por consecuencia, la precisión del sensor y exactitud de la electrooxidación del alcohol.
Cuando su concentración es pequeña, la alta concentración de álcali y la alta velocidad de la formación de sitios activos hacen con que la velocidad de la reacción será más rápida que la difusión del analito (valores menores de k1 con valores mayores de ∏) y la reacción será controlada por la difusión. Ya cuando la concentración del analito es grande, su difusión será más rápida que su reacción y para compensar la entrada rápida la reacción también deberá ser acelerada por medio de la formación de los nuevos sitios; la estabilidad de estado estacionario será controlada por la cinética de la reacción, lo que fue descrito en [16] y [22].
No habiendo bastante álcali para la formación de complejos (que no se toma en cuenta en el modelo como tal que sucede en el exceso serio del álcali), el aumento de su concentración favorece la estabilidad de estado estacionario, porque beneficia la formación de nuevos sitios activos. En general, la condición de estabilidad se satisface para la vasta región parametral, lo que está de acuerdo con los datos experimentales, descritos en [16-22]. Desde el punto de vista electroquímico, está correspondiendo a la zona lineal de la curva "parámetro electroquímico" "concentración".
En el caso de igualdad de influencias de la oxidación de Ni (II) hasta Ni (III) a la capa doble a las influencias de otros procesos a la estabilidad de estado estacionario, se formará la inestabilidad monotónica, cuya condición de aparición será descrita así:
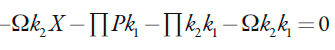 | [22] |
Correspondiendo a la "frontera" entre los estados estacionarios estables e inestables. Esta inestabilidad es definida por la bifurcación de silla y nudo y es correspondiente a los valores paramétricos, para los cuales existen varios estados estacionarios inestables y el sistema escoge apenas uno. Este estado se destruye después del cambio de condiciones.
La inestabilidad oscilatoria para este sistema es posible. Para su realización, la diagonal principal del jacobiano debe contener elementos positivos. Como ninguno de los procesos no es autocatalítico, el único elemento de la diagonal de la matriz, capaz de ser positivo es el l Ω , que es positivo en el caso de la presencia de las influencias de la oxidación en la capa doble. Tal causa es común para todos los sistemas semejantes [30-35] y así se puede explicar la aparición de oscilaciones de baja amplitud que se observaban en [22].
Compósitos. Para la descripción matemática del desempeño del compósito "nanopartículas - polímero conductor" se pueden usar las dos maneras: tomar en cuenta el compósito entero o tomar en cuenta los papeles de cada uno de los componentes. Si se usa la primera manera, se podrá utilizar el presente modelo; en el caso de la segunda manera, se podrá usar (suponiendo el exceso del álcali) el modelo descrito en [35], siendo el polímero conductor tomado en cuenta como mediador.
Conclusiones
El análisis de modelo y su comparación con los datos experimentales dan los siguientes resultados:
1) El proceso de la oxidación de metanol en el electrodo de carbono vítreo, modificado por las nanopartículas de los derivados de níquel o por su compósito con el polímero conductor, fue descrito matemáticamente, siendo que los resultados del modelaje están de acuerdo con los experimentales.
2) La estabilidad de estado estacionario en el sistema es garantizada por la ausencia de las influencias de los procesos de la oxidación electroquímica a la capa doble y se mantiene por el modo estacionario de la concentración del analito en la capa presuperficial. El aumento de la concentración del álcali (sin exceso significante) favorece la estabilidad de estado estacionario.
3) Las inestabilidades electroquímicas solo pueden realizarse en el caso de las influencias grandes a la capa doble de los procesos de la electrooxidación. La posibilidad de la aparición de estructuras disipativas temporales en este sistema ha sido confirmada.
Referencias
1. F. Bindler, E. Voges, P. Laugel, Tem of methanol concentration in distilled food spirits, Food Add. Contam., 5, 343 (1988).
2. T. Iwasita, Electrocatalysis of methanol oxidation, Electrochim. Acta, 47, 3663 (2002).
3. M.A. Abel-Rahim, R.M. Abdel Hameed, M.W. Khalil, Nickel as a catalyst for the electro-oxidation of methanole in alkaline medium, J. Power Sources, 134, 160 (2004).
4. A. Verna, S. Basu, Direct use of alcohols and sodium boronhidride as a fuel in alkaline cells, J. Power Sources, 145, 282 (2005).
5. H. Heli, M. Jafarian, M.G. Mahjani, F. Gobal, electro-oxidation of methanol on copper in alkaline solution, Electrochim. Acta, 49, 4999 (2004).
6. R. Parsons, T. Vandernoot, The oxidation of small organic molecules: A survey of recent fuel cells related research, J. Electroanal. Chem., 257, 9 (1988).
7. K. Nishimura, K. Machida, M. Enyo, Electrooxidation of formate and formaldehyde on electrodes of alloys between Pd and Group IB metals in alkaline media: Part II. The possibility of complete oxidation of formaldehyde in weak alkali, J. Electrochem. Anal., 251, 117 (1998).
8. E. Morallón, F.J. Cases, J.L. Vásquez, A. Aldaz, Irreversible adsorption of methanol on Pt(110) in carbonate solution, Electrochim. Acta, 37, 1883 (1992).
9. J.J. Pietron, M.B., Pomfret C.C. Chervin et al. Direct methanol oxidation at low overpotentials, using Pt nanoparticles electrodeposited at RuO2 ultrathin conductive nanoskins, J. Mat. Chem., 22, 5197 (2012).
10. Y. Zhao, L. Zhan, J. Tian et al. Enhanced electrocatalytic oxidation of methanol on Pd/polypyrrole-graphene in alkaline medium, Electrochim. Acta, 56, 1967 (2011).
11. A.V. Tripkovic, N. Marinkovic, K.D. Popovic, R.R. Adzic, Oxidation of methanol on single-crystal platinum electrodes in alkaline solutions, Russ. J. Electrochem., 31, 993 (1995).
12. M. Chen, Z.B. Wang, Y. Ding, G.P. Yin, Investigation of the Pt-Ni-Pb/C ternary alloy catalysts for methanol electrooxidation, Electrochem. Comm., 10, 443 (2008).
13. S.J. Liu, Kinetics of methanol oxidation on poly(Ni(II)-tetramethyl-dibenzotetraaza[ 14]annulene)-modified electrodes, Electrochim. Acta, 49, 3235 (2004).
14. Y. Wu, Y. He, T. Wu et al. Influence of some parameters on the synthesis of nanosized NiO material by modified sol-gel method, Mater. Lett., 61, 3174 (2007).
15. X. Li, X. Zhang, Z. Li, Y. Qian, Synthesis and characteristics of NiO nanoparticles by thermal decomposition of nickel dimethylglyoximate rods, Solid State Comm., 137, 581 (2006).
16. J.B. Raoof, R. Ojani, S.R. Hosseini, An electrochemical investigation of methanol oxidation on nickel hydroxide nanoparticles, South Afr. J. Chem., 66, 47 (2013).
17. R. Ojani, J.B. Raoof, S.R. Hosseini, Electrochemical oxidation of methanol on carbon paste electrode modified by nickel ions dispersed into poly(1,5-diaminonaphthalene) film, Electrochim. Acta, 53, 2402 (2008).
18. R. Ojani, J.B. Raoof, S. Fathi, Poly(o-aminophenol) film prepared in the presence of sodium dodecyl sulfate: Application for nickel ion dispersion and the electrocatalytic oxidation of methanol and ethylene glycol, Electrochim. Acta, 54, 2190 (2009).
19. R. Ojani, J.B. Raoof, S. Fathi, Nickel-poly(o-aminophenol)-modified carbon paste electrode: An electrocatalyst for methanol oxidation, J. Sol. State Electrochem., 13, 927 (2009).
20. J.B. Raoof, R. Ojani, S.R. Hosseini, A novel, effective and low cost catalyst for methanol oxidation based on nickel ions dispersed onto poly(o-toluidine)/Triton X-100 film at the surface of multi-walled carbon nanotube paste electrode, J. Power Sources, 196, 1855 (2011).
21. J.B. Raoof, M.A. Karimi, S.R. Hosseini, S. Mangelizadeh, Cetyltrimethyl ammonium bromide effect on highly electrocatalysis of methanol oxidation based on nickel particles electrodeposited into poly (m-toluidine) film on the carbon paste electrode, J. Electroanal. Chem., 638, 33 (2010).
22. R. Ojani, J.B. Raoof, A. Ahmady, S.R. Hosseini, High improved methanol oxidation onto carbon paste electrode modified by nickel particles dispersed into poly(2,5-dimethylamine) film, Casp. J. Chem., 2, 45 (2013).
23. H. Idris, J. Wang, S. Chou et al. Effects of polypyrrole on the performance of nickel oxide anode materials for rechargeable lithium-ion batteries, J. Mater. Res., 26, 860 (2011).
24. S.J. Kim, M.K. Hong, J.K. Chung, S.Y. Park, Electrochemical properties of Ni(OH)2/Polypyrrole composite electrode prepared by electrodeposition for pseudo-capacitor, J. Cer. Proc. Res., 13, 274 (2012).
25. T.O. Pavela, "The low potential oxidation of methanol at a platinased platinum anode", Helsinki, 1954.
26. T. McQuade, A. Pullen, T.M. Swager, Conjugated polymer based chemical sensors, Chem. Rev., 100, 2537 (2000).
27. S. Takeda, H. Yagi, S. Mizuguchi et al. A highly sensitive amperometric adenozyne triphosphate sensor, based on moleculary imprinted overoxidized polypyrrole, J. Flow Inj. Anal., 25, 77 (2008).
28. O. Korostynska, K. Arshak, E. Gill, A. Arshak, Review on state-of-the-art in polymer based pH sensors, Sensors, 7, 3027 (2008).
29. R. Singh, Prospects of organic conducting polymer modified electrodes: Enzymosensors, Int. J. Electrochem, N 502707 (2012).
30. V. Tkach, V. Nechyporuk, P. Yagodynets,, A investigação matemática do desempenho de biossensores eletroquímicos enzimáticos, baseados nos polímeros condutores, Rev. Colomb. Cienc. Quím. Farm., 41, 203 (2012).
31. V. Tkach, V. Nechyporuk, P. Yagodynets´, A descrição matemática do processo da detecção de duas substâncias com um grupo funcional comum pelos sensores e biossensores eletroquímicos, baseados nos polímeros condutores, Rev. Colomb. Cienc. Quím. Farm., 42, 215 (2013).
32. V. Tkach, V. Nechyporuk, P. Yagodynets´, I. Rusnak, Los biosensores, basados en los polímeros conductores, y la descripción matemática de su desempeño, Orbital Elec. J. Chem., 4, 136 (2012).
33. V. Tkach, R. Ojani, V. Nechyporuk, P. Yagodynets´, A descrição matemática do desempenho eletroanalítico de nanopartículas do óxido de cobre (II) na eletrodetecção da hidrazina, Orbital Elec. J. Chem., 6, 142 (2014).
34. V.V. Tkach, V.V. Nechyporuk, P.I. Yagodynets´, The mathematical study of the work of isomerization sensors, based on conducting polymers, Anal. Bioanal. Electrochem, 6, 273 (2014).
35. V.V. Tkach, V.V. Nechyporuk, P.I. Yagodynets´, Yu V. Meslyuk, Mathematical model of the work of the mediated conducting polymer sensors with the use of the polymers of heterocyclic compounds, Rev. Soc. Quím. Perú, 77, 259 (2011).
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
Licencia
Derechos de autor 2015 Revista Colombiana de Ciencias Químico-Farmacéuticas

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
El Departamento de Farmacia de la Facultad de Ciencias de la Universidad Nacional de Colombia autoriza la fotocopia de artículos y textos para fines de uso académico o interno de las instituciones citando la fuente. Las ideas emitidas por los autores son responsabilidad expresa de estos y no de la revista.
Todo el contenido de esta revista, excepto dónde está identificado, está bajo una Licencia Creative Commons de Atribución 4.0 aprobada en Colombia. Consulte la normativa en: http://co.creativecommons.org/?page_id=13

















