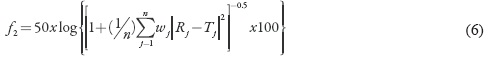Diseño de un sistema bioadhesivo de clorhexidina empleando pullulan como matriz para uso en mucosa oral
Design of a bioadhesive system with chlorhexidine using pullulan as matrix for use in oral mucous
DOI:
https://doi.org/10.15446/rcciquifa.v45n1.58016Palabras clave:
Películas poliméricas, tabletas bioadhesivas, mucoadhesió pullulan (es)Polymer films, Bioadhesive tablets, Mucoadhesion, Pullulan (en)
Se desarrollaron sistemas poliméricos bioadhesivos del tipo película polimérica y comprimido empleando el biopolímero pullulan, para el transporte de digluconato de clorhexidina, el cual es un principio activo utilizado como alternativa terapéutica
en el tratamiento de la gingivitis y de la enfermedad periodontal. Inicialmente, se evaluó la capacidad del polímero para formar películas y tabletas, luego, fueron propuestas formulaciones de cada uno de los sistemas. A las películas y comprimidos obtenidos se les determinaron propiedades mecánicas y de transporte, actividad antiséptica, caracterización de las microestructuras obtenidas, además, se comprobó la liberación del fármaco desde los sistemas estudiados. Con las formulaciones seleccionadas se determinó su capacidad mucoadhesiva in vitro, empleando como sustrato mucosa oral porcina.
As a therapeutic alternative in the transport of active substances in treatment of gingivitis and periodontal disease, bioadhesive polymeric systems type polymeric film and tablet were developed using the biopolymer pullulan. First, the ability of pullulan polymer to form films and tablets was evaluated and formulations were proposed for each system. Mechanical and transport properties, as well as antiseptic activity and microstructures characteristics were determined for these polymeric systems. Drug release behavior in the studied systems was also verified. The in vitro mucoadhesive capacity was determined with the formulations selected, using porcine oral mucous membrane like substrate.
DOI: https://doi.org/10.15446/rcciquifa.v45n1.58016
Diseño de un sistema bioadhesivo de clorhexidina empleando pullulan como matriz para uso en mucosa oral
Design of a bioadhesive system with chlorhexidine using pullulan as matrix for use in oral mucous
Jean M. Castro Ruiz*, Bibiana M. Vallejo Díaz**, Helber J. Barbosa Barbosa***
Departamento de Farmacia, Universidad Nacional de Colombia, Sede Bogotá, Cra. 30 No. 45-03, Bogotá D.C., Colombia
* Correo electrónico: jemcastroru@unal.edu.co
** Correo electrónico: bmvallejod@unal.edu.co
*** Correo electrónico: hdbarbosab@unal.edu.co
Recibido para evaluación: 11 de octubre de 2015. Aceptado para publicación: 4 de febrero de 2016.
Resumen
Se desarrollaron sistemas poliméricos bioadhesivos del tipo película polimérica y comprimido empleando el biopolímero pullulan, para el transporte de digluconato de clorhexidina, el cual es un principio activo utilizado como alternativa terapéutica en el tratamiento de la gingivitis y de la enfermedad periodontal. Inicialmente, se evaluó la capacidad del polímero para formar películas y tabletas, luego, fueron propuestas formulaciones de cada uno de los sistemas. A las películas y comprimidos obtenidos se les determinaron propiedades mecánicas y de transporte, actividad antiséptica, caracterización de las microestructuras obtenidas, además, se comprobó la liberación del fármaco desde los sistemas estudiados. Con las formulaciones seleccionadas se determinó su capacidad mucoadhesiva in vitro, empleando como sustrato mucosa oral porcina.
Palabras clave: películas poliméricas, tabletas bioadhesivas, mucoadhesión, pullulan.
Summary
As a therapeutic alternative in the transport of active substances in treatment of gingivitis and periodontal disease, bioadhesive polymeric systems type polymeric film and tablet were developed using the biopolymer pullulan. First, the ability of pullulan polymer to form films and tablets was evaluated and formulations were proposed for each system. Mechanical and transport properties, as well as antiseptic activity and microstructures characteristics were determined for these polymeric systems. Drug release behavior in the studied systems was also verified. The in vitro mucoadhesive capacity was determined with the formulations selected, using porcine oral mucous membrane like substrate.
Key words: Polymer films, Bioadhesive tablets, Mucoadhesion, Pullulan.
Introducción
Los sistemas bioadhesivos han sido empleados especialmente en aplicaciones odontológicas, ortopédicas, oftálmicas y quirúrgicas y, actualmente, en el estudio sobre reemplazo de tejidos y la liberación controlada y localizada de principios activos sobre mucosas [1]. Las aplicaciones potenciales de este fenómeno exigen un estudio minucioso sobre los fundamentos que rigen el comportamiento de los materiales poliméricos empleados para estos desarrollos, cuando se encuentran en contacto con superficies de tipo biológico, y cómo, a partir del entendimiento de estos principios, es posible desarrollar materiales con mejores propiedades de desempeño y, a la par, proponer formulaciones optimizadas para utilizarlos como sistemas bioadhesivos [2]. El empleo de polímeros sintéticos es común en diversas aplicaciones industriales, sin embargo, la tendencia mundial es la utilización de materiales biodegradables como los polímeros naturales, gracias a sus propiedades y características biológicas, para el mejoramiento de los sistemas terapéuticos farmacéuticos. Los polisacáridos representan una clase importante de biomateriales naturales, que incluyen el almidón, la celulosa, la agarosa, el alginato, el dextrano y la quitina, entre otros [3]. Dentro de los materiales de tipo biopolímero disponibles para la formulación de productos, se encuentra el pullulan; un polisacárido natural soluble en agua, que se obtiene por la fermentación del almidón. Este material puede ser una alternativa como polímero objeto de estudio, para ser utilizado en un sistema de transporte farmacéutico, formulado con un principio activo antiséptico, tal como la clorhexidina, que es ideal por ser un agente antimicrobiano de amplio espectro [4].
El pullulan es un polisacárido lineal neutro formado por enlaces α-(1→6) glicosídicos vinculados a residuos de maltotriosa. Se trata de un exopolisacárido producido por el hongo Aureobasidium pullulans. La masa molecular de este biopolímero se encuentra en el rango de miles a dos millones de daltons, dependiendo de las condiciones de crecimiento del organismo Aureobasidium pullulans. Este polímero es biodegradable, no higroscópico; produce soluciones viscosas y transparentes, también, tiene una alta adherencia y capacidad de formar películas impermeables al oxígeno. Su estructura química se muestra en la figura 1. Las películas con pullulan han sido estudiadas, agregándoles principios activos de extractos de origen natural con propiedades antisépticas, antiinflamatorias, bactericida y antifúngicas, demostrando actividad antimicrobiana [5].
La clorhexidina es uno de los antimicrobianos más utilizados en los tratamientos odontológicos por infecciones bucales [6]; esta biguanida presenta una gran actividad antibacteriana sumada a una alta substantividad [7]; tiene la capacidad de unirse a las proteínas tales como la albúmina presente en el suero o saliva, la película de la superficie dentaria, las glicoproteínas salivales y las membranas mucosas. Es un agente antimicrobiano de amplio espectro, activo contra bacterias Gram-positivas, Gram-negativas y levaduras. Debido a su naturaleza catiónica, la clorhexidina es capaz de unirse electrostáticamente a las superficies de las bacterias cargadas negativamente, dañando así la superficie externa de la pared celular y dejándola permeable.
Dependiendo de su concentración, esta biguanida puede tener efecto bacteriostático o bactericida [4], y ha sido utilizada en enjuagues bucales para el tratamiento de la gingivitis y de la enfermedad periodontal [8–9]. Las sales de clorhexidina pueden emplearse en la profilaxis y el tratamiento de las infecciones de boca como: la estomatitis, la estomatitis ulcerativa y la gingivitis aguda ulcerativa necrotizante, en concentraciones de 0,12% y 0,2% [5, 10–11].
Existe una variedad de sales de clorhexidina, donde se incluyen las formas acetato, gluconato, clorhidrato y digluconato, pero la forma digluconato (figura 2) es la más soluble en agua [12], a pH fisiológico se disocia fácilmente y es una sal muy estable, de allí que en los preparados farmacéuticos se use la sal digluconato [7].
En el mercado se encuentran tabletas para chupar con clorhexidina digluconato [13]. La clorhexidina se absorbe por las superficies orales, incluidos los dientes y luego se libera lentamente en forma activa [7]. En Colombia, la clorhexidina se encuentra comercializada en solución bucal al 0,12 y 0,2% y gel oral al 1%.
Partiendo de la premisa, de que la administración tópica será más efectiva, si permanece el principio activo en contacto con las áreas de la mucosa lesionada durante más tiempo, nos encontramos con que en la cavidad oral este aspecto es especialmente complejo por la intervención de factores como la secreción salival o los movimientos bucolinguales. Por ello, solo se pueda aumentar el tiempo de permanencia del fármaco en la boca de dos maneras: incrementando voluntariamente la retención del mismo por parte del paciente o incorporando a las formulaciones galénicas sustancias que favorezcan la adhesión a la mucosa.
Además, debido a la continua dilución salival del principio activo y la deglución involuntaria por parte del paciente, existe un alto riesgo de que se pierda la mayor parte del medicamento. Este inconveniente se eliminaría o se podría reducir mediante el uso de sustancias adhesivas que facilitaran, aún sin colaboración por parte del paciente, la retención del sistema polimérico ayudando a mantener el fármaco en un contacto mayor con la mucosa oral. Por esta razón, en la presente investigación se busca el desarrollo de un sistema polimérico a base de pullulan cargado con clorhexidina, ya que su capacidad mucoadhesiva permite fijar el fármaco a la dentina, o superficie del diente, gracias a un mayor tiempo de contacto sobre la mucosa oral.
Los sistemas orales con propiedades mucoadhesivas representan matrices adecuadas para incorporar una gran variedad de fármacos, actualmente, estos sistemas son preferidos para el desarrollo de medicamentos de aplicación oral por sus ventajas, como los prolongados tiempos de residencia y la estabilidad de los fármacos [14].
Materiales y métodos
Caracterización de tabletas y películas
En las tablas 1 y 2 presentan las formulaciones para comprimidos y películas.
Determinación de la densidad de las películas
La densidad se calculó a partir de la masa, determinada en una balanza digital con precisión de 0,01 g, y el volumen fue calculado a partir del área y el espesor de las películas. En el cálculo del espesor se realizaron 6 determinaciones por película de cada una de las 3 películas, empleando un micrómetro Teclock, con una precisión de 0,01 mm.
Determinación morfológica de películas por microscopía electrónica de barrido (SEM)
La inspección morfológica de las películas se determinó en un microscopio electrónico de barrido FEI QUANTA 200. Las muestras se sometieron a un tratamiento previo de recubrimiento por metalización, realizado en un Sputter SDC-050 de la marca Balzers.
Evaluación de las propiedades de transporte
Hinchamiento de las tabletas
Las propiedades de hinchamiento y las características de erosión de los comprimidos se evaluaron determinando el porcentaje de hidratación y la erosión matricial. Cada comprimido se pesó w1 (g) y sumergió en un fluido símil salival (2,38 g Na2HPO4; 0,19 g KH2PO4 y 8,00 g NaCl por litro de agua destilada ajustada con ácido fosfórico a pH 6,75). Se hicieron mediciones cada 5 min, los comprimidos se retiraron del medio para ser pesados w2 (g), antes de pesarlos se les quitó el exceso de agua superficial. Los comprimidos hinchados fueron secados durante 24 h a 37 °C. Luego se colocaron en un desecador durante 48 h antes de ser pesados nuevamente w3 (g). Los experimentos se realizaron por triplicado. El porcentaje de hidratación y la erosión matricial se calcularon de acuerdo a las ecuaciones 1 y 2 [15].
Índice de hinchamiento de las películas
Se colocaron películas poliméricas de 20 x 20 mm de diámetro sobre mallas de acero, que previamente fueron pesadas, se sumergieron en agua y medio fisiológico; se realizaron mediciones cada 2 min y se calculó la cantidad de agua atrapada por la película. El grado de hinchamiento se calculó a partir de la ecuación 3 [16].
Donde, Q (t) es el índice de hinchamiento, wt es el peso (g) de la película al tiempo t (h), wo es el peso (g) de la película al tiempo cero.
Permeabilidad al vapor de agua de películas
La permeabilidad al vapor de agua se determinó utilizando un método estándar modificado del procedimiento ASTM designación E 96 M-05 [17]. Las muestras, previamente cortadas en círculos, se colocaron en cápsulas de vidrio conteniendo 2 g de silica gel. Se sellaron de manera hermética con las películas elaboradas y, posteriormente, fueron pesadas y luego introducidas en una cámara con humedad controlada. La prueba se llevó a cabo durante 12 horas, realizando mediciones cada hora. El valor de la permeabilidad al vapor de agua (TVA) es expresado en gramos de agua por unidad de tiempo por unidad de área [g/(h.mm2)], el cual se calculó según la ecuación 4.
Donde TVA es transmisión de vapor de agua, w es el peso final (g), wo es el peso inicial (g), t es el tiempo (h), A es el área expuesta de la película (m2) y (g/t) es la pendiente de la línea recta, gramos/horas.
Determinación de propiedades mecánicas
Dureza y friabilidad de las tabletas
Se realizó la prueba de dureza y friabilidad en 10 tabletas. Cada ensayo se hizo por triplicado, empleando un durómetro Sotax HT1 y un friabilizador Erweka TA3 (USP 36, 2013) para las pruebas de dureza y friabilidad respectivamente.
Resistencia a la ruptura por tensión de las películas
Se tomaron películas de 20 x 70 mm sujetas entre dos mordazas de extremo a extremo, para esta prueba se empleó un analizador de textura TA XT Plus, Texture Analyser, el ensayo de realizó por triplicado. Se realizó la determinación del módulo de elasticidad, denominado también de tracción o de Young.
Resistencia a la ruptura por perforación de las películas
Las películas fueron fijadas a una placa y perforadas por un probador que se mueve a una velocidad de 180 mm/min. Para esta prueba se empleó un analizador de Textura TA XT Plus, Texture Analyser, con una sonda cilíndrica de acero inoxidable, el ensayo se realizó por triplicado.
Ensayos de funcionalidad
Evaluación de la capacidad mucoadhesiva ex-vivo
Estos ensayos constituyen una forma indirecta de estudiar la adhesión de los sistemas poliméricos en la mucosa bucal. Para ello, ha sido utilizado el tejido bucal del cerdo, porque su morfología no queratinizada es bastante similar al epitelio bucal humano. Para llevar a cabo este ensayo se adaptó la metodología de Jiménez y colaboradores [18]. El tejido oral fue pegado en el fondo del vaso del equipo de disolución y los sistemas poliméricos se aplicaron sobre la mucosa oral porcina. Cada sistema polimérico, tanto tabletas como películas, fue humectado con 100 µL de fluido salival y colocado sobre la mucosa, aplicando una fuerza digital durante 20 s. El ensayo fue realizado a una velocidad de agitación de 100 rpm utilizando 600 ml de fluido símil salival, pH 6,75 a 37° C. Se observó el comportamiento de los sistemas poliméricos hasta una completa disolución o desprendimiento de los mismos.
Incorporación del principio activo en los sistemas poliméricos
Preparación de las tabletas con clorhexidina digluconato
De acuerdo a los resultados obtenidos de la formulación con mejores propiedades mecánicas y de transporte, el principio activo se incorporó embebiendo la solución de clorhexidina digluconato en una premezcla de ingredientes sólidos. La mezcla se secó a una temperatura de 50° C hasta alcanzar un 2% de humedad, se mezcló con los demás ingredientes de la formulación y se comprimió utilizando las mismas condiciones antes descritas en obtención de las tabletas.
Preparación de las películas con clorhexidina digluconato
Fue preparada una dispersión polimérica a partir de la escogencia de la formulación con las mejores propiedades mecánicas y de transporte. Se pesó el agua y se adicionó, primero, el plastificante, agitando a 150 rpm hasta homogenizar, luego, el pullulan a temperatura de 50 ºC por 20 min con agitación de 900 rpm, y por último, la clorhexidina digluconato, agitando continuamente con calentamiento por 10 min, luego se dejó enfriar y reposar la dispersión y se almacenó hasta su completa deaireación por 12 h. La dispersión obtenida fue vertida en una superficie acrílica con dimensiones de 15 x 15 cm; se secó a temperatura ambiente de 25±2 °C por 36 h. Las películas formadas se desprendieron de los moldes y fueron almacenadas en condiciones controladas de humedad relativa de 55±2% a 18 °C para las determinaciones posteriores. Las películas fueron cortadas con una dimensión de 2 cm2, área que aportaría 5 mg de dosificación del principio activo, igual dosificación del principio activo en la tableta.
Metodología para evaluar la liberación de la clorhexidina digluconato desde los sistemas poliméricos
Adaptando la metodología de Chiapeta y colaboradores [15] para los estudios de liberación in vitro se empleó el método de la paleta (método II de la USP 36, 2013). Los sistemas poliméricos (comprimidos y películas) fueron introducidos en una canastilla y sumergidos en el fondo de los vasos. El ensayo se realizó empleando como medio de disolución 500 ml de fluido símil salival a una temperatura de 37 °C ± 0,5 ºC. La velocidad de agitación del ensayo fue de 50 rpm, los tiempos de muestreo fueron 15, 30, 60, 120 y 180 min. La determinación cuantitativa de clorhexidina fue realizada mediante espectrofotometría UV a una longitud de onda de 254 nm.
Con el fin de comparar los perfiles de disolución obtenidos a partir de los sistemas poliméricos evaluados en fluido símil salival, y para conocer el efecto de la composición de cada lote sobre la velocidad de liberación del fármaco, se utilizaron los índices propuestos por Moore y Flanner [19]. Este modelo independiente utiliza dos índices matemáticos para calcular los factores de diferencia f1 (ecuación 5) y similitud f2 (ecuación 6) entre los perfiles de disolución:
Donde n es el número de puntos temporales, Rj es el valor de disolución de la tanda de referencia en el tiempo t, y Tj es el valor de disolución de la tanda de prueba en el tiempo t.
Evaluación del efecto antimicrobiano de las películas y tabletas
Adaptando la metodología de Flamenco y Guevara [20] se realizaron medidas a través de un ensayo de inhibición de desarrollo bacteriano, colocando los sistemas poliméricos cargados con el fármaco objeto de estudio en contacto con tres cepas: Escherichia coli (ATCC 8739), Pseudomona aeruginosa (ATCC 9027) y Candida albicans (ATCC 10231).
Análisis estadístico de los datos
La interpretación estadística de los datos fue llevada a cabo mediante un análisis de varianza (ANOVA) y test HSD Tukey con un nivel de confianza del 95%. Se utilizó el software Statgraphics Centurión para Windows.
Resultados y discusión
Evaluación preliminar de las formulaciones para la obtención de tabletas y películas
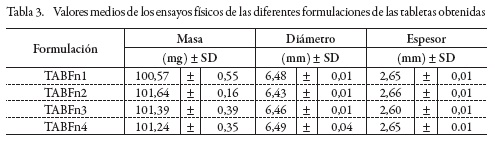
Teniendo en cuenta la codificación determinada para cada una de las formulaciones de las tabletas, a las formulaciones cargadas con el fármaco se le dará la terminación CLX. En la tabla 3 se reportan los valores del peso promedio final y dimensiones de cada una de las formulaciones de las tabletas para las cuatro formulaciones estudiadas. A los datos obtenidos se les realizó el análisis de varianza (ANOVA), con un nivel de confianza del 95%. Después del análisis estadístico se pudo evidenciar que entre los tratamientos de estudio se presentan diferencias estadísticamente significativas (p<0,05) en el peso promedio final y dimensiones. De acuerdo con el análisis del test de Tukey se denota que la formulación TABFn2 tiene características diferentes a las demás formulaciones.
De acuerdo a la codificación dada para cada una de las formulaciones de las películas, a las formulaciones cargadas con el fármaco también se le dará la terminación CLX como a las tabletas.
Se observaron las características físicas de las diferentes películas elaboradas, encontrando que las formulaciones Fn1 y Fn3 tuvieron buena apariencia, formaron películas transparentes y brillantes, lo que indica que es una ventaja en su aplicación sobre la superficie de la mucosa bucal (ver figura 3). No se percibió algún olor característico y presentaron buena flexibilidad. La película obtenida de la formulación Fn2 mostró rugosidad en su superficie y cierto grado de opacidad. Se le atribuyó esta característica a la adición del agar. Las películas obtenidas fueron segmentadas en cuadrados de 2 x 2 cm, en esta área se garantiza que las películas quedarán cargadas con 5 mg de principio activo, igual cantidad con la que se formularon las tabletas.
En la tabla 4 se reportan los valores del peso promedio final de cada una de las tres formulaciones elaboradas, así como el espesor y densidad de las mismas. A los datos obtenidos se les realizó el análisis de varianza (ANOVA), con un nivel de confianza del 95%. Después del análisis estadístico se evidenció que presentan diferencias estadísticamente significativas (p<0,05). El análisis del test de Tukey demuestra que la formulación Fn2 tiene características diferentes para todas las pruebas, demostrando la diferencia en la formulación respecto a Fn1 y Fn3. La formulación Fn2 mostró una diferencia en cuanto a sus valores medios de peso, espesor y densidad, esto se debe a la rugosidad de la película obtenida (provocada por la adición de agar).
Las películas mucoadhesivas, de acuerdo con sus características de textura y diámetro, tendrían ventajas sobre las tabletas. Estas ventajas se asociarían al cumplimiento del tratamiento y preferencia por parte del paciente, al ser más cómodo de colocar y ser casi imperceptible al estar en contacto con las superficies de la boca, ya que, por el tipo de lesión presentada, la tableta pudiese causar algún tipo de molestia por carecer de flexibilidad.
Determinación morfológica de películas por microscopía electrónica de barrido (SEM)
Teniendo en cuenta el criterio de selección acogido para el ensayo de liberación, esta determinación se realizó únicamente sobre las películas blanco, obtenidas de la formulación Fn1 y de las películas cargadas obtenidas de la formulación Fn1CLX. Las cuatro micrografías de la figura 4 corresponden a observaciones hechas en corte transversal y superficial de las películas sin principio activo y cargadas con este, en dos aumentos diferentes. Se observó una buena distribución de los polímeros, no se presentó separación de fases entre estos, y la película mostró una morfología suave, uniforme y sin la presencia de porosidades.
Evaluación de propiedades de transporte de tabletas
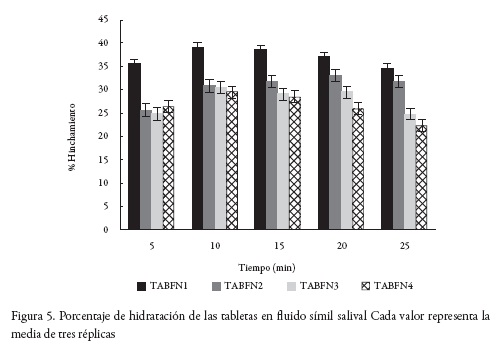
Estudios de hinchamiento
Los perfiles de hidratación observados en la figura 5 fueron similares para las formulaciones TABFn2, TABFn3 y TABFn4 hasta los 10 min, luego se ve una diferencia entre estas, se observa que la formulación TABFn2 sigue hidratándose, mientras que las formulaciones TABFn3 y TABFn4 no retienen más agua. La formulación TABFn2 que contiene Aerosil 200 sigue captando agua debido a que este, por ser de naturaleza hidrofílica, tendría la capacidad de retener agua, por otro lado, su hinchamiento se ve retrasado a diferencia de la formulación TABFn1 que contiene celulosa microcristalina pero no Aerosil 200. Así bien, para el caso de la formulación TABFn1, esta muestra un comportamiento diferente al resto de formulaciones por el alto contenido de celulosa microcristalina en el comprimido. Al representar una alta proporción en el sistema, la estructura interna de la matriz cambia, llegando a ser más porosa y menos restrictiva para que se difunda el agua hacía el interior del comprimido, produciendo de esta manera la relajación de las cadenas poliméricas con posterior hidratación del mismo y la continuación del proceso de erosión.
Con los resultados anteriores, de la hidratación de las tabletas, se evaluó el porcentaje de erosión producido por el desgaste de las mismas (figura 6). Se observó que la formulación TABFn2 no se erosiona tan fácilmente como las otras tres formulaciones. Esto se debe a la capacidad del Aerosil 200 de formar geles y de ejercer algún tipo de control sobre la viscosidad del preparado cuando entra en contacto con un medio acuoso. Es decir, se ve reflejado tanto en la hidratación como en la erosión el marcado efecto que ejerce el uso del Aerosil 200. En la prueba se observó que no hay hinchamiento exagerado de la tableta, este se manifiesta en los primeros 5 min de entrar en contacto con el medio acuoso, a los 10 min ya empieza a erosionarse, disminuyendo su diámetro considerablemente. De lo anterior se deduce que el uso de las tabletas y su aplicabilidad en cualquier superficie de la mucosa bucal no ejercerían ningún tipo de inconveniente como resultado del hinchamiento. Por el contrario, puede ser una ventaja ya que, al relajarse las cadenas del polímero, el fármaco podría difundir desde sus redes de una manera controlada.
Evaluación de propiedades de transporte de películas
Estudios de hinchamiento
En la prueba de hinchamiento, la integridad de las películas de las tres formulaciones ensayadas se vio drásticamente afectada, ya que en un lapso de 2 min, las muestras sumergidas tanto en agua destilada y medio fisiológico pH 6,75 sufrieron un proceso de ablandamiento, tan rápido, que no fue posible realizar las mediciones y pesajes de las mismas, a la vez que se tornaron muy adhesivas.
Se puede decir que las películas compuestas con el biopolímero pullulan se adaptan rápidamente a cualquier superficie de la mucosa oral, lo que las hace funcionales para la entrega de fármacos en la cavidad bucal. El pullulan se puede combinar con diferentes polímeros que le confieran otras características de transporte, por ejemplo, con la gelatina o alginato [5]. Por lo tanto, se evidencia que la película experimenta un mayor cambio conformacional al relajar sus cadenas, favoreciendo así el paso del medio a través de esta.
Estudios de transmisión de vapor de agua de las películas
En la tabla 5 se presentan los resultados obtenidos para el ensayo de la transmisión de vapor de agua. El pullulan es de carácter hidrofílico, lo cual favorece esta propiedad de transporte. La inclusión del agar afecta un poco esta propiedad, debido, probablemente, a que las películas con agar tienen la particularidad de ser insolubles en agua en condiciones ambientales, al igual que el agar solo [21]. Se observó que la película preparada según la formulación Fn1 presenta una mayor transmisión de vapor de agua (5,22 g/h.m2). La formulación Fn3 tuvo una TVA mayor a la formula Fn2, pero no muy lejana, esta última formulación es la que contiene el agar.
De acuerdo con los resultados, se mantuvo un rango uniforme en la transmisión del vapor de agua en todas las preparaciones, pese a que la formulación Fn2 obtuvo la mayor ganancia de agua en función del tiempo, arrojó los menores resultados de transferencia al vapor de agua. Esto podría ser causado por la presencia del agar, el cual capta mucha agua en sus redes poliméricas, pero no deja pasar el vapor de agua de la misma manera que las películas fabricadas sólo con pullulan. Esto indicaría que una película de agar combinada con pullulan podría, eventualmente, retardar la liberación del fármaco desde un soporte polimérico. A los datos obtenidos se les realizó el análisis de varianza (ANOVA), con un nivel de confianza del 95%. Después del análisis estadístico se pudo evidenciar que no se presentan diferencias estadísticamente significativas (p>0,05). El análisis del test de Tukey demuestra que todas las formulaciones tienen rasgos similares para estas pruebas.
Determinación de propiedades mecánicas
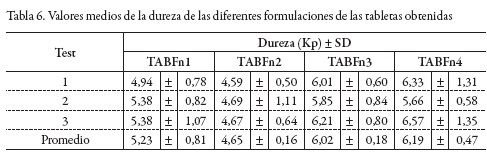
Pruebas de dureza y friabilidad de las tabletas
Las formulaciones preparadas solo con pullulan alcanzaron durezas más altas trabajadas bajo las mismas condiciones (ver tabla 6). Las tabletas mucoadhesivas no deberían ser muy duras ya que podría originar molestias al paciente y por consiguiente el incumplimiento del tratamiento, incluso la liberación del fármaco puede verse afectado. Tampoco deberían ser muy blandas, ya que al entrar en contacto con la humedad de la cavidad bucal podría ocurrir una desintegración muy rápida, donde el fármaco sea arrastrado por la saliva y los movimientos de la boca. Si la tableta no queda adherida el tiempo suficiente, el fármaco no alcanzaría a ser liberado en su totalidad. A los datos obtenidos se les realizó el análisis de varianza (ANOVA), con un nivel de confianza del 95%. El análisis estadístico evidenció que se presentan diferencias estadísticamente significativas (p<0,05). El análisis del test de Tukey demuestra que las formulaciones TABFn1 y TABFn2 tienen rasgos similares, estas tienen celulosa microcristalina en su formulación y estas a su vez fueron diferentes a las formulaciones TABFn3 y TABFn4 las cuales contienen solo pullulan en su composición.
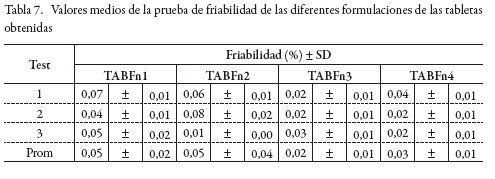
En la tabla 7 se reportan los valores de friabilidad de cada una de las formulaciones de las tabletas obtenidas. Se encuentra que las formulaciones preparadas tienen valores muy bajos en esta prueba, y, se puede decir que tienen excelente friabilidad. Las tabletas que no presentaron buena friabilidad tendían a desgastarse con facilidad, un desgaste alto en los procesos de manufactura conllevaría a obtener tabletas porosas y de mal aspecto, además, en las pruebas de disolución generarían un efecto burst, el cual es la salida abrupta del fármaco de la forma farmacéutica. A los datos obtenidos se les realizó el análisis de varianza (ANOVA), con un nivel de confianza del 95%. El análisis estadístico evidenció que no se presentan diferencias estadísticamente significativas (p>0,05). El análisis del test de Tukey demostró que todas las formulaciones tienen rasgos similares para esta prueba.
Resistencia a la ruptura por tensión de películas
En estos ensayos, ninguna película sufrió ruptura por la tensión aplicada, únicamente elongación, y al finalizar la prueba retornaron a su longitud inicial; el comportamiento de estas películas es del tipo clásico de un material elástico o flexible que podría adaptarse al contorno de las superficies de la cavidad oral.
En la figura 7, se muestran la gráfica de tensión en función de la deformación de las películas evaluadas. La figura 8 demuestra el estiramiento de cada una de las películas cuando es halada desde los extremos, todas las películas tuvieron una elongación similar.
Los valores encontrados en el módulo de Young, de las formulaciones Fn1, Fn2 y Fn3 (tabla 8), muestran valores bajos de este, indicando que las películas no son rígidas, presentan una elevada elasticidad, por ello se deforman con facilidad y presentan gran capacidad de elongación y resistencia. Las fibras de elastina presentes en la dermis también tienen bajos los módulos de Young, con valores de 6x105 N/m2, o bien, 0,6 N/mm2 estirándose hasta un 250% de su longitud inicial.
De otro lado, el colágeno es muy flexible y se rompe cuando el esfuerzo de tensión es de aproximadamente 500 millones de Newtons por metro cuadrado, es decir, que su resistencia es similar a la del acero [22]. A los datos obtenidos se les realizó el análisis de varianza (ANOVA), con un nivel de confianza del 95%. Después del análisis estadístico evaneció que presentan diferencias estadísticamente significativas (p<0,05). El análisis del test de Tukey demuestra la rigidez de la formulación Fn2 ante las demás formulaciones.
Resistencia a la ruptura por perforación de películas
En la figura 9 se muestran la gráfica de perforación-deformación de las películas en las formulaciones evaluadas. Ninguna película fue perforada, pero en la resistencia al esfuerzo aplicado, se observó que la película polimérica formulada con agar (Fn2) tuvo un comportamiento más rígido al tratar de ser perforada en su superficie (ver tabla 9). Lo anterior, de acuerdo a las observaciones realizadas por Cerrada [23], podría atribuirse a numerosos factores estructurales, junto con la composición química, el peculiar comportamiento mecánico de los polímeros: su masa molecular, entrecruzamiento y ramificación, cristalinidad y morfología cristalina, copolimerización, plastificación, orientación molecular, cargas, mezclas, separación de fases y orientación en bloques.
Los polímeros lineales de masas moleculares altas y no iónicos forman películas fuertes, como es el caso del agar, las películas producidas por este polímero presentan una apariencia clara y, en general son fuertes, aunque son frágiles y poco flexibles [21]. Esto demostró el resultado de la película Fn2, la cual contiene agar, que tuvo una menor resistencia a la deformación, sin embargo, fue la que menos elasticidad presentó, confirmando así su rigidez. A los datos obtenidos se les realizó el análisis de varianza (ANOVA), con un nivel de confianza del 95%. Después del análisis estadístico se evidenció que presentan diferencias estadísticamente significativas (p<0,05). El análisis del test de Tukey demostró que la formulación Fn2 tiene rasgos distintos respecto a las demás formulaciones. Se desea, desde el desempeño funcional de productos, que la película no presente excesiva rigidez que dificulte su manipulación durante la colocación sobre la mucosa; los valores obtenidos muestran que la formulación Fn1 presenta el comportamiento mecánico esperado para la aplicación.
Evaluación de la capacidad mucoadhesiva ex-vivo
En el ensayo de mucoadhesión ex vivo, de las cuatro formulaciones ensayadas para las tabletas, las formulaciones que permanecieron adheridas a la mucosa oral hasta su completa erosión y dispersión fueron la TABFn2, TABFn3 y TABFn4, ninguna tableta se despegó de la mucosa oral hasta su completa erosión al final de la prueba (120 min). De la formulación TABFn1, una de las tabletas se desprendió a los 105 min, las restantes permanecieron adheridas a la mucosa oral hasta su completa erosión. Esta última formulación TABFn1 al igual que TABFn2 contenían celulosa microcristalina en su composición, sin embargo, la TABFn1 la contiene en un mayor porcentaje.
La celulosa microcristalina juega un papel fundamental en el complejo matricial, ya que logra mantener la estructura del comprimido casi intacta a través del tiempo, pero, de cierta forma, puede afectar un poco la capacidad bioadhesiva del comprimido. En el ensayo de mucoadhesión ex-vivo para el caso de las películas, las tres formulaciones resultantes, Fn1, Fn2 y Fn3, permanecieron adheridas hasta su completa erosión y dispersión, ninguna se despegó de la mucosa oral porcina. La alta adhesión del pullulan [24] permite que la película fabricada con este polímero quede adherida a la mucosa oral hasta su completa erosión. En la figura 10 se observa tanto la tableta como la película adheridas a la mucosa oral, demostrando que el tamaño de la tableta y la película son apropiados para ser colocadas en la cavidad bucal de un adulto normal. En el caso de las películas se evidencia que, al adherirse a la superficie de la mucosa, estas se adaptan fácilmente y toman la forma del sitio de aplicación, para mayor comodidad del paciente, esto debido a que las películas son delgadas y flexibles, además, la estructura del polímero es fuertemente adhesiva a la mucosa y no se vería afectada por cambios mínimos en las actividades normales de los pacientes, por ejemplo, comer, beber o hablar [14].
La tabla 10 presenta los resultados de mucoadhesión ex -vivo para los dos sistemas poliméricos estudiados.
Incorporación del principio activo en los sistemas poliméricos
Con los resultados obtenidos en los diferentes ensayos llevados a cabo durante el presente estudio, y considerando las propiedades mecánicas, de transporte, así como el resultado de la prueba de mucoadhesión ex-vivo, se optó por evaluar el perfil de liberación del fármaco clorhexidina y su desempeño como antimicrobiano, a partir de la formulación para las películas Fn1 y para los comprimidos a partir de la formulación TABFn2.
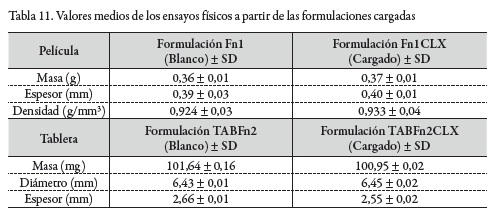
La tabla 11 presenta los resultados de los análisis correspondientes a valores medios de los ensayos realizados a los sistemas poliméricos. La película cargada con el principio activo clorhexidina exhibió una apariencia similar a la de su blanco, de acuerdo a su transparencia y brillantez (ver figura 11).
Se escogió una prueba determinante como es la mucoadhesión ex-vivo y se hicieron los ensayos a los sistemas cargados para películas y tabletas (Fn1CLX y TABFn2CLX) con el fin de evaluar la incidencia del fármaco en los preparados. Las muestras, correspondientes a tres réplicas de cada uno de los dos sistemas poliméricos, permanecieron adheridas a la mucosa oral porcina hasta su completa erosión y dispersión, conservando la propiedad de mucoadhesión.
Liberación de la clorhexidina desde las películas poliméricas y comprimidos a base de pullulan
Con los resultados obtenidos, se optó por evaluar el perfil de liberación a partir de la formulación para las películas Fn1 y de la formulación para los comprimidos TABFn2.
Al aplicar el modelo, independiente de los factores de similitud y diferencia a los perfiles obtenidos de las películas y los comprimidos (figura 12), se encontró que los datos de disolución de ambos perfiles son diferentes, arrojando resultados de similitud (f2) de 41 (50-100) y de diferencia (f1) de 20 (0-15). Sin embargo, la cesión de clorhexidina digluconato a partir de los sistemas poliméricos llega a un 100% de fármaco disuelto. Este marcado efecto prolongado por parte del comprimido se debe a que este se erosionó más lento que la película. Esta se erosiona y dispersa a los pocos minutos, mientras la erosión de la tableta se observó a los 60 min, reteniendo el fármaco por más tiempo en sus redes poliméricas. A los 180 min, ambos perfiles demuestran el 100% de fármaco disuelto. El modelo matemático al cual se ajustan los perfiles de disolución de los dos sistemas poliméricos después de hacer los respectivos ajustes de los datos de liberación, es el de Korsmeyer y Peppas, el cual generalmente es lineal para valores de Mt/M∞<0,6. Este modelo intenta explicar mecanismos de liberación de fármacos donde se presenta erosión o disolución de la matriz, y no es más que una forma generalizada de la ecuación de Higuchi como se expresa en la ecuación 7.
Donde K es la constante de velocidad de liberación que incorpora características estructurales y geométricas del sistema de liberación y n es el exponente que indica el mecanismo mediante el cual ocurre la liberación. El valor del exponente n brinda información sobre la cinética de liberación del fármaco, por lo que, si n es igual a 0,5, la liberación del fármaco tiene lugar a través de un fenómeno de difusión de tipo fickiano, si n toma valores entre 0,5 y 1 indica que la liberación del fármaco es debida a un mecanismo de difusión no fickiano o anómalo, y, cuando n es igual a 1, el mecanismo de liberación del fármaco depende del proceso de relajación de las cadenas poliméricas [25].
Teniendo en cuenta las consideraciones ya descritas y el modelo de Korsmeyer-Peppas, la velocidad de difusión del fármaco y la velocidad de relajación de las cadenas del polímero son del mismo orden de magnitud (ver tabla 12). En este caso, el proceso de difusión no fickiano se denomina anómalo, el cual puede ser interpretado como un proceso complejo, que no puede ser descrito como un modelo simple para predecir las observaciones experimentales [26].
Los datos experimentales fueron evaluados cinéticamente utilizando el programa computacional (KinetDS 3.0®).
Evaluación del efecto antimicrobiano
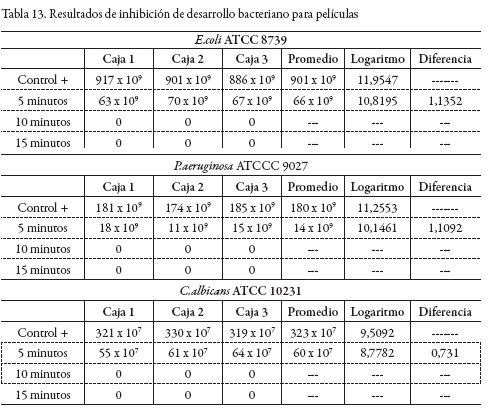
Para la evaluación de la actividad antimicrobiana de los sistemas poliméricos cargados con el fármaco se calculó el promedio de la reducción logarítmica para los tres microorganismos de prueba y para tres tiempos de ensayo. En las tablas 13 y 14 se muestran los resultados de inhibición de desarrollo bacteriano para películas y tabletas. Luego de los 5 min de contacto, se observó en todos los ensayos efectuados que hay una considerable reducción del número de microorganismos sobrevivientes, y a los 10 min de contacto no se encontró ningún sobreviviente, indicando que la clorhexidina digluconato en ambos sistemas poliméricos es efectiva contra los microorganismos de prueba, y confirmando que hay liberación del principio activo desde estos sistemas de transporte diseñados.
Conclusiones
A partir de esta investigación, queda demostrada la utilidad del pullulan (polímero biodegradable) como soporte polimérico versátil en la manufactura de dos tipos de preparados para su uso en la cavidad bucal. Los sistemas poliméricos estudiados, de acuerdo a las propiedades evaluadas, reúnen características que le confieren la posibilidad de incorporar el principio activo clorhexidina digluconato para preparados mucoadhesivos; se logró desarrollar películas poliméricas funcionales como un sistema alternativo de elección para transportar fármacos que sean fijados a la mucosa bucal, indistintamente que se dispersen en medio acuoso en pocos minutos, y tabletas mucoadhesivas que se convertirían en preparados alternativos para liberar fármacos de una manera gradual, propicias para aquellos fármacos que requieren fijarse en las superficies de la mucosa oral por un tiempo de residencia mayor.
Las películas de pullulan, sin estar en combinación con otros polímeros, tienen excelentes propiedades mecánicas y de transporte, lo cual permite que estas se fijen a cualquier superficie de la mucosa bucal y, además, facilitan el paso de los fluidos biológicos a través de sus cadenas poliméricas cediendo el fármaco de elección. Los estudios de liberación demostraron que ambos sistemas poliméricos entregan el principio activo en su totalidad, permitiendo prever su posible eficacia frente a las infecciones de la boca. Los sistemas poliméricos cargados con el principio activo clorhexidina digluconato, objeto de estudio en el presente trabajo, demuestran efectividad, inhibiendo el desarrollo de microorganismos como bacterias y levaduras.
Agradecimientos
Por la colaboración prestada para el desarrollo de la tesis de Maestría de uno de los autores (J.M. Castro Ruiz, "Diseño de un sistema bioadhesivo de clorhexidina empleando pullulan como matriz para uso en mucosa oral", Universidad Nacional de Colombia –Sede Bogotá, 2014) manifestamos nuestros agradecimientos al Departamento de Farmacia de la Universidad Nacional de Colombia, por facilitar los equipos e instalaciones requeridos para adelantar el presente estudio
Referencias
1. A.M. Hillery, A. Lloyd, J. Swarbrick, "Drug Delivery and Targeting", Taylor and Francis, Inc., New York, 2001.
2. B. Vallejo, J. Perilla, Elementos conceptuales para estudiar el comportamiento bioadhesivo en polímeros, Rev. Colomb. Cienc. Quím. Farm. 37(1), 34 (2008).
3. A. Dhanikula, R. Panchagnula, Development and characterization of biodegradable chitosan films for local delivery of paclitaxel, AAPS J., 6, 27 (2004).
4. B. Basrani, Update en Clorhexidina, Canal Abierto: Revista de la Sociedad de Endodoncia de Chile, 20, 6 (2009).
5. A. Rodríguez, "Elaboración de biopelículas a base de quitosan y pululano adicionadas con extractos de cinco diferentes plantas y su evaluación en cultivos de microorganismos periodontopatógenos", Tesis de Doctorado, Universidad Autónoma de Nuevo León, 2011, pp. 6.
6. I. Yévenes, J. Reyes, N. Campos, V. Saragoni, Efecto inhibitorio en placa microbiana y propiedades antibacterianas de enjuagatorios de clorhexidina, Rev. Avances en Periodoncia e Implantología, Universidad de Chile, 15(1), 19 (2003).
7. M. Girón, "Determinación de la concentración, pH, estabilidad y el tiempo en el que permanece estable el principio activo de la clorhexidina preparada en las clínicas de cirugía de la facultad de odontología de la Universidad de San Carlos de Guatemala", Tesis de Grado, Universidad de San Carlos de Guatemala, 2001, pp. 16-19.
8. J. Saavedra, M. Terrón, Antisépticos, Guía ABE. Infecciones en Pediatría, 1, 2007.
9. R. Rowe, P. Sheskey, S. Owen, "Handbook of Pharmaceutical Excipients", 5th ed, Pharmaceutical Press and American Pharmacists Association, Washington, 2006, pp. 163-166.
10. A. Martín, "Diseño y formulación de películas poliméricas como sistema de transporte de clorhexidina", Tesis de Grado, Universidad Nacional de Colombia, 2009, p. 3.
11. J. Arévalo, J. Arribas, M. Hernández, M. Lizan, R. Herruzo, "Guía de utilización de antisépticos", Sociedad Española de Medicina Preventiva, Salud Pública e Hgiene, Madrid, 1998, p. 1-11.
12. F. Masquio, M. Correa, H. Nunes, Development and validation of a microbiological assay for determination of clorhexidine digluconate in aqueous solution, Braz. J. Pharm. Sci., 49(2), 351 (2013).
13. Agencia Española de Medicamentos y Productos Sanitarios. URL: http://www.aemps.gob.es/medicamentosUsoHumano/portada/home.htm, julio de 2014.
14. J. Gajdziok, S. Holešová, J. Štembírek, E. Pazdziora, H. Landová, Petr Dolezel, D. Vetchý, Carmellose mucoadhesive oral films containing vermiculite/chlorhexidine nanocomposites as innovative biomaterials for treatment of oral infections, BioMed Res. Int., 2015(1), Article ID 580146 (2015).
15. D. Chiappetta, E. Gergic, M. Legaspi, G. Cantarelli, M. Garcia, C. Bregni, Comprimidos bioadhesivos formulados con excipientes hidrofílicos para uso bucofaríngeo, Acta Farm. Bonaerense, 25(3), 360 (2006).
16. W. Li, N. Wu, Poly (vinyl alcohol) nanoparticles prepared by freezing-thawing process for protein/peptide drug delivery, J. Control. Rel., 56, 117 (1998).
17. N. Arévalo, M. Alemán, M. Rojas, R. Morales, Películas biodegradables a partir de residuos de cítricos: propuesta de empaques activos, Rev. Latinoamer. Biotecnol. Amb. Algal., 1(2), 124 (2010).
18. R. Jiménez, C. Mora, "Estudios de liberación in-vitro y permeación ex-vivo de microesferas de alginato-quitosano conteniendo benzocaína", Tesis de Grado, Universidad del Atlántico, Barranquilla, 2013.
19. J. Moore, H. Flanner, Mathematical comparison of dissolution profiles, Pharm. Tech., 20, 64 (1996).
20. J. Flamenco, G. Guevara, "Formulación de tres productos desinfectantes y evaluación de su actividad antimicrobiana", Tesis de Grado, Universidad de El Salvador, 2011, pp. 47.
21. A. López, "Diseño, desarrollo y aplicación de envases comestibles potencialmente bioactivos", Tesis de Doctorado, Universidad Complutense de Madrid, 2013, pp. 11-13.
22. M. Gutiérrez, "Biomecánica: la física y la fisiología", Instituto de Ciencia de Materiales, Consejo Superior de Investigaciones Científicas, Madrid, 2000.
23. M. Cerrada, "Propiedades mecánicas, comportamiento viscoelástico y anisotropía de copolímeros de alcohol vinílico y etileno", Tesis de Doctorado, Universidad Complutense de Madrid, 1995, pp.57-59.
24. M. Rekha, C. Sharma, Pullulan as a promising biomaterial for biomedical applications: A perspective, Trends Biomater. Artif. Organs, 20(2), 1 (2007).
25. J. Aragón, R. González, N. Brizuela, L. Oliver, Estudio cinético de liberación in vitro en un biomaterial compuesto por HAP-200/POVIAC/CaCO3, Rev. Iberoamer. Polím., 10, 2 (2009).
26. C. Maderuelo, A. Zarzuelo, J.M.Lanao, Critical factors in the release hydrophilic matrices, J. Control. Rel., 154, 2 (2011).
Referencias
(1) A.M. Hillery, A. Lloyd, J. Swarbrick, “Drug Delivery and Targeting”, Taylor and Francis, Inc., New York, 2001.
(2) B. Vallejo, J. Perilla, Elementos conceptuales para estudiar el comportamiento bioadhesivo en polímeros, Rev. Colomb. Cienc. Quím. Farm. 37(1), 34 (2008).
(3) A. Dhanikula, R. Panchagnula, Development and characterization of biodegra- dable chitosan films for local delivery of paclitaxel, AAPS J., 6, 27 (2004).
(4) B. Basrani, Update en Clorhexidina, Canal Abierto: Revista de la Sociedad de Endodoncia de Chile, 20, 6 (2009).
(5) A. Rodríguez, “Elaboración de biopelículas a base de quitosan y pululano adicionadas con extractos de cinco diferentes plantas y su evaluación en cultivos de microorganismos periodontopatógenos”, Tesis de Doctorado, Universidad Autónoma de Nuevo León, 2011, pp. 6.
(6) I. Yévenes, J. Reyes, N. Campos, V. Saragoni, Efecto inhibitorio en placa microbiana y propiedades antibacterianas de enjuagatorios de clorhexidina, Rev. Avances en Periodoncia e Implantología, Universidad de Chile, 15(1), 19 (2003).
(7) M. Girón, “Determinación de la concentración, pH, estabilidad y el tiempo en el que permanece estable el principio activo de la clorhexidina preparada en las clínicas de cirugía de la facultad de odontología de la Universidad de San Carlos de Guatemala”, Tesis de Grado, Universidad de San Carlos de Guatemala, 2001, pp. 16-19.
(8) J. Saavedra, M. Terrón, Antisépticos, Guía ABE. Infecciones en Pediatría, 1, 2007.
(9) R. Rowe, P. Sheskey, S. Owen, “Handbook of Pharmaceutical Excipients”, 5th ed, Pharmaceutical Press and American Pharmacists Association, Washington, 2006, pp. 163-166.
(10) A. Martín, “Diseño y formulación de películas poliméricas como sistema de transporte de clorhexidina”, Tesis de Grado, Universidad Nacional de Colombia, 2009, p. 3.
(11) J. Arévalo, J. Arribas, M. Hernández, M. Lizan, R. Herruzo, “Guía de utilización de antisépticos”, Sociedad Española de Medicina Preventiva, Salud Pública e Higiene, Madrid, 1998, p. 1-11.
(12) F. Masquio, M. Correa, H. Nunes, Development and validation of a microbiological assay for determination of clorhexidine digluconate in aqueous solution, Braz. J. Pharm. Sci., 49(2), 351 (2013).
(13) Agencia Española de Medicamentos y Productos Sanitarios. URL: http://www.aemps.gob.es/medicamentosUsoHumano/portada/home.html , julio de 2014.
(14) J. Gajdziok, S. Holešová, J. Štembírek, E. Pazdziora, H. Landová, Petr Dolezel, D. Vetchý, Carmellose mucoadhesive oral films containing vermiculite/chlorhexidine nanocomposites as innovative biomaterials for treatment of oral infections, BioMed Res. Int., 2015(1), Article ID 580146 (2015).
(15) D. Chiappetta, E. Gergic, M. Legaspi, G. Cantarelli, M. Garcia, C. Bregni, Comprimidos bioadhesivos formulados con excipientes hidrofílicos para uso bucofaríngeo, Acta Farm. Bonaerense, 25(3), 360 (2006).
(16) W. Li, N. Wu, Poly (vinyl alcohol) nanoparticles prepared by freezing-thawing process for protein/peptide drug delivery, J. Control. Rel., 56, 117 (1998).
(17) N. Arévalo, M. Alemán, M. Rojas, R. Morales, Películas biodegradables a partir de residuos de cítricos: propuesta de empaques activos, Rev. Latinoamer. Biotecnol. Amb. Algal., 1(2), 124 (2010).
(18) R. Jiménez, C. Mora, “Estudios de liberación in-vitro y permeación ex-vivo de microesferas de alginato-quitosano conteniendo benzocaína”, Tesis de Grado, Universidad del Atlántico, Barranquilla, 2013.
(19) J. Moore, H. Flanner, Mathematical comparison of dissolution profiles, Pharm. Tech., 20, 64 (1996).
(20) J. Flamenco, G. Guevara, “Formulación de tres productos desinfectantes y evaluación de su actividad antimicrobiana”, Tesis de Grado, Universidad de El Salvador, 2011, pp. 47.
(21) A. López, “Diseño, desarrollo y aplicación de envases comestibles potencialmente bioactivos”, Tesis de Doctorado, Universidad Complutense de Madrid, 2013, pp. 11-13.
(22) M. Gutiérrez, “Biomecánica: la física y la fisiología”, Instituto de Ciencia de Materiales, Consejo Superior de Investigaciones Científicas, Madrid, 2000.
(23) M. Cerrada, “Propiedades mecánicas, comportamiento viscoelástico y anisotropía de copolímeros de alcohol vinílico y etileno”, Tesis de Doctorado, Universidad Complutense de Madrid, 1995, pp.57-59.
(24) M. Rekha, C. Sharma, Pullulan as a promising biomaterial for biomedical applications: A perspective, Trends Biomater. Artif. Organs, 20(2), 1 (2007).
(25) J. Aragón, R. González, N. Brizuela, L. Oliver, Estudio cinético de liberación in vitro en un biomaterial compuesto por HAP-200/POVIAC/CaCO3, Rev. Iberoamer. Polím., 10, 2 (2009).
(26) C. Maderuelo, A. Zarzuelo, J.M.Lanao, Critical factors in the release hydrophilic matrices, J. Control. Rel., 154, 2 (2011).
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
CrossRef Cited-by
1. Efraín Armenta Rojas, José Manuel Cornejo Bravo, Aracely Serrano Medina , Eduardo Alberto López Maldonado , Amelia Olivas Sarabia, Nydia Alejandra Castillo Martínez, Ayla Carolina Vea Barragán. (2021). Películas mucoadhesivas de quitosano para la liberación sostenida de nistatina en la cavidad bucal . REVISTA DE CIENCIAS TECNOLÓGICAS, 4(1), p.1. https://doi.org/10.37636/recit.v41118.
Dimensions
PlumX
Visitas a la página del resumen del artículo
Descargas
Licencia
Derechos de autor 2016 Revista Colombiana de Ciencias Químico-Farmacéuticas

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
El Departamento de Farmacia de la Facultad de Ciencias de la Universidad Nacional de Colombia autoriza la fotocopia de artículos y textos para fines de uso académico o interno de las instituciones citando la fuente. Las ideas emitidas por los autores son responsabilidad expresa de estos y no de la revista.
Todo el contenido de esta revista, excepto dónde está identificado, está bajo una Licencia Creative Commons de Atribución 4.0 aprobada en Colombia. Consulte la normativa en: http://co.creativecommons.org/?page_id=13