Publicado
Terapia Larval con Musca Domestica en el Tratamiento de la úlcera Leishmánicaen un Modelo Murino
Larval therapy with Musca domesticain the treatment of leishmanian ulcerin a murine model
DOI:
https://doi.org/10.15446/abc.v25n1.77177Palabras clave:
Antimonial, cicatrización, Leishmaniasis, moscas, tratamiento, úlcera (es)Antimonial, cicatrization, Leishmaniosis, maggot, treatment, ulcer (en)
Descargas
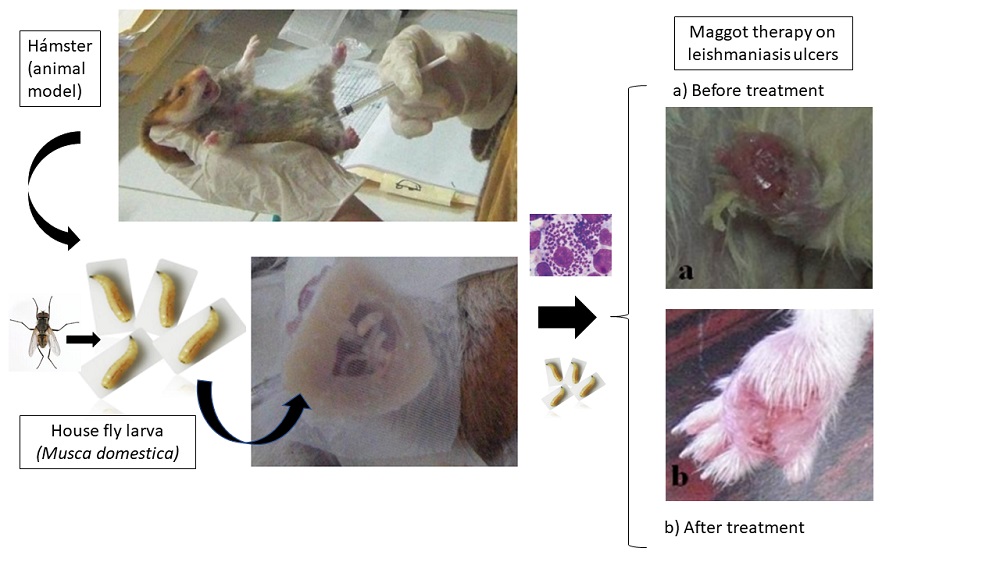
La leishmaniosis es una enfermedad con gran impacto en salud pública dado a las características de las lesiones tegumentarias. El tratamiento experimental con terapia larval (TL) ha mostrado su uso potencial para la cura de la leishmaniosis, sin embargo, se han utilizado especies de moscas para TL en heridas causadas por Leishmania que no son de fácil colecta y cultivo bajo condiciones de laboratorio como Lucilia sericata o Calliphora vicina. El objetivo del presente trabajo fue usar una especie de mosca de fácil colecta, y de alta fecundidad como la Musca domestica para aplicarlas en TL de úlceras leishmánicas. Se realizó un estudio cuali-cuantitativo, de tipo descriptivo, mediante un diseño experimental empleado un modelo animal (Mesocricetus auratus), infectado con Leishmania amazonensis para evaluar el efecto terapéutico de la TL y comparar los resultados con el tratamiento químico antimonial de la droga experimental “Ulamina”. Se evidencia cicatrización y cura de la úlcera leishmánica en el 66,66 % de los animales tratados con TL en aplicación simple y del 100 % en TL combinada con Ulamina. El uso combinado de TL+Ulamina, muestra un efecto potenciador de la cura clínica de las úlceras, pero con persistente inflamación. Se observó una efectividad óptima de la TL con M. domestica, sobre las úlceras, aunque no se evidenció un efecto sobre L. amazonensis dado a la presencia de amastigotes en los frotis y a los amplicones obtenidos de 480 bp desde las improntas de los animales.
Leishmaniasis is a disease with significant impact on public health, given the characteristics of the tegumentary lesions. Experimental treatment with larval therapy (LT) has shown its potential use for the cure of leishmaniosis. However, fly species not easy to collect and/or colonize have been used. The objective of the present work was to use a fly of accessible collection and high fecundity, not a producer of human myiasis, such as Musca domestica. A qualitative-quantitative study of a descriptive type was carried out through an experimental design with an animal model (Mesocricetus auratus) with infection by Leishmania amazonensis to evaluate the therapeutic effect of LT and compare the results with the antimonial chemical treatment of the drug experimental “Ulamina”. Scarring were observed with the use of LT in 66.66 % with TL-simple and 100 % with TL-combined. However, the combined use of LT + Ulamina, shows an enhancing effect of the clinical cure of the lesions, but with persistent inflammation. Optimal effectiveness of TL with M. domestica was observed on the ulcers; however, an effect on L. amazonensis was not observed given the presence of amastigotes in the smears and the 480 bp amplicons from the tissue of the ulcers of animals.
Referencias
Andersen S, Sandvang D, Schnorr MK, Kruse T, Neve S, Joergensen B, et al. A novel approach to the antimicrobial activity of maggot debridement therapy. J Antimicrob Chemother. 2010;65(8):1-9. Doi:https://doi.org/10.1093/jac/dkq165
Arrivillaga J, Rodríguez J, Oviedo M. Evaluación preliminar en un modelo animal de la terapia con larvas de Lucilia sericata para el tratamiento de la leishmaniasis cutánea. Biomédica. 2008;28(2):305-10. Doi: https://doi.org/10.7705/biomedica.v28i2.102
Azad AK, Azizi WS, Yee BL. Maggot debridement therapy for diabetic foot ulcer: Experience from Maggot treatment Centers. Asian J Pharm Pharmacol. 2016;2(1):23-25.
Brambilla P.B.T. Terapia larval e divulgação científica no Brasil: até quando serão negligenciadas? (Bachelor's thesis, Universidade Federal do Rio Grande do Norte). Ciudad Natal: Universidade Federal do Rio Grande do Norte; 2018. p. 29.
Baumann A, Skaljac M, Lehmann R, Vilcinskas A, Franta Z. Urate Oxidase produced by Lucilia sericata medical maggots is localized in Malpighian tubes and facilitates allantoin production. Insect Biochem. Mol. Biol. 2017;83:44-53. Doi: 10.1016/j.ibmb.2017.02.007
Bonfante R. Leishmanias y leishmaniasis tegumentaria en América Latina. Bol. Oficina Sanit. Panam. 1983;95(5):418-423.
Calderón-Arguedas O, Belfort K, Troyo A, Gamboa M. Terapia larval con Lucilia eximia (Diptera: Calliphoridae) de Costa Rica en un modelo experimental. Rev Chilena Ent. 2014;39(1):57-65.
Carrero Rangel JA, Borges HR, Convit García J, Avilan Rovira J, de Lima H. Inmunoterapia de la leishmaniasis cutánea: factores que influencian su efectividad. Bol Mal Salud Amb. 2011;51(1):25-33.
Cazander G, Pritchard DI, Nigam Y, Jung W, Nibbering PH. Multiple actions of Lucilia sericata larvae in hard‐to‐heal wounds: larval secretions contain molecules that accelerate wound healing, reduce chronic inflammation and inhibit bacterial infection. Bioessays. 2013;35(12):1083-1092. Doi: https://doi.org/10.1002/bies.201300071
Chu F, Jin X, Ma H, Lu X, Zhu J. Effect of Musca domestic maggot polypeptide extract on HUVEC dysfunction induced by early activated macrophages. Pharm Biol. 2016;54(4):572–575. Doi: https://doi.org/10.3109/13880209.2015.1060506
Convit J, Ulrich M, Pérez M, Hung J, Castillo J, Rojas H, et al. Atypical cutaneous leishmaniasis in Central America: possible interaction between infectious and environmental elements. Trans R Soc Trop Med Hyg. 2005;99(1):13-17. Doi: https://doi.org/10.1016/j.trstmh.2004.02.005
Cruz-Saavedra L, Díaz-Roa A, Gaona M.A, Cruz M.L, Ayala M, Cortés-Vecino JA, et al. The effect of Lucilia sericata-and Sarconesiopsis magellanica-derived larval therapy on Leishmania panamensis. Acta Trop. 2016;164:280-289. Doi: https://doi.org/10.1016/j.actatropica.2016.09.020
de Jesus R, Quiñones W, O´Callaghan J. Identificación de proteínas de la membrana glicosomal de Leishmania mexicana con fines de diagnóstico. Rev. Ecol. Lat. Am. 1999;6(2):9-17.
De Moura T, Novais F, Oliveira F, Clarêncio J, Noronha A, Barral A et al. Toward a novel experimental model of infection to study American cutaneous leishmaniasis caused by Leishmania braziliensis. Infect Immun. 2005;73(9):5827-5834. Doi: https://doi.org/10.1128/IAI.73.9.5827-5834.2005
Díaz-Roa A, Gaona M.A, Segura N.A, Ramirez H.A, Cortés V.J.A, Patarroyo M.A, et al. Evaluating Sarconesiopsis magellanica blowfly-derived larval therapy and comparing it to Lucilia sericata-derived therapy in an animal model. Acta Trop. 2016;154:34-41. Doi: https://doi.org/10.1016/j.actatropica.2015.10.024
Evans DA. In Vitro Cultivation and Biological Cloning of Leishmania. En Protocols in Molecular Parasitology. New Jersey: U.S.A; 1994. p. 29-41
Figueroa L, Flores J, Rodríguez S. Método de cultivo de larvas de moscas Lucilia sericata para terapia larval. Paras latinoam. 2007;62(1-2):79-82. Doi: http://dx.doi.org/10.4067/S0717-77122007000100014
Fu P, Wu J, Guo G. Purification and Molecular Identification of an Antifungal Peptide from the Hemolymph of Musca domestica (housefly). Cell Mol Immunol. 2009;6(4):245-251. Doi: https://doi.org/10.1038/cmi.2009.33.
Golczer G, Arrivillaga J. Modificación de un protocolo estándar de extracción de ADN para flebotominos pequeños (Phlebotominae: Lutzomyia). Rev. Colomb. Entomol. 2008;34(2):199-203.
Góngora J, Díaz-Roa A, Gaona MA, Cortés VJ, Bello F. Evaluación de la actividad antibacterial de los extractos de cuerpos grasos y hemolinfa derivados de la mosca Sarconesiopsis magellanica (Diptera: Calliphoridae). Infectio. 2015;19(1):3-9. Doi: https://doi.org/10.1016/j.infect.2014.09.003
González-de Paz, L., Fortes-Bordas, M., de Pedro-Elvira, B. Descripción de dos casos de herida, con diferente etiología, tratadas mediante terapia larval desbridante. Enferm Clin. 2010;20(1):47-53. Doi: https://doi.org/10.1016/j.enfcli.2009.10.004
Henao H, Osorio Y, Saravia N, Gómez A, Travi B. Eficacia y toxicidad de los antimoniales pentavalentes (Glucantime y Pentostam) en un modelo animal de leishmaniasis cutánea americana: aplicación de la luminometría. Biomédica. 2004;24(4):393-402. Doi: https://doi.org/10.7705/biomedica.v24i4.1289
Jaklic D, Lapanje A, Zupanc K, Smrke D, Cimerman N. Selective antimicrobial activity of maggots against pathogenic bacteria. J Med Microbiol. 2008;57(5):617–625. Doi: https://doi.org/10.1099/jmm.0.47515-0
Jiménez CE. Curación avanzada de heridas. Rev col Cir. 2008;23(3):146-155.
Jin X, Mei H, Li X, Ma Y, Zeng AH, Wang Y et al. Apoptosis-inducing activity of the antimicrobial peptide cecropin of Musca domestica in human hepatocellular carcinoma cell line BEL-7402 and the possible mechanism. Acta Biochim Biophys Sin. 2010;42(4):259-265. Doi: https://doi.org/10.1093/abbs/gmq021.
Jun-Cheng W, Ren-rong L, Ran H, Hong-bin F, Shuang-ming S. Maggot therapy for repairing serious infective wound in a severely burned patient. Chin J Traumatol. 2012;15(2):124-125.
Laverde-Paz MJ, Echeverry MC, Patarroyo MA, Bello FJ. Evaluating the anti-leishmania activity of Lucilia sericata and Sarconesiopsis magellanica blowfly larval excretions/secretions in an in vitro model. Acta trop. 2018;177:44-50. Doi: https://doi.org/10.1016/j.actatropica.2017.09.033
Li Q, Lu R, Huo R, Fu H. Maggots of Musca domestica in treatment of acute intractable wound. Surgery. 2008;145(1):122-123. Doi: https://doi.org/10.1016/j.surg.2008.08.016.
López-Carvajal L, Palacio-Barco MA, Cardona-Arias JC. Eficacia de los azoles en el tratamiento de la leishmaniasis cutánea. Arch de Med. 2016;12(2):1-10. Doi: https://doi.org/10.3823/1289
Maldonado A, Pérez OG. Leishmaniasis: nuevos tratamientos, mecanismos de acción y sus implicaciones. Rev. INBIOM. 2016;1(3):22-30.
Martiradonna G, Soto A, González J. Protocolo de cría de Musca domestica en laboratorio. Bol Mal Salud Amb. 2009;49(2):317-319.
Ministerio de Ciencia y Tecnología [MCT]. Código de Bioética y Bioseguridad. Caracas: Editorial MCT; 2002. 1-35p.
Montalvo AM, Fraga J, Rodríguez O, Blanco O, Llanos C.A, García A et al. Detección de Leishmania spp. en base al gen que codifica la proteína HSP20. Rev. perú. med. exp. Salud. 2014;31(4):635-643
Narváez D, Moreno E, Scorza J. Acción del Glucantime y del Camolar en hámsteres infectados con cepas de Leishmanias dermotropas andino –venezolanas. Bol Mal Salud Amb. 1979;19(3):110-118.
Nieves MP, Díaz E, Romero A, Machuca C, Sucre AP. Valor pronóstico de los cambios fisiológicos asociados a la quimio-resistencia en Leishmania. Vitae: Acad Bioméd Digital. 2007;(33):1-22.
OMS. Modelo OMS de información sobre prescripción de medicamentos: Medicamentos utilizados en las enfermedades parasitarias. Ginebra: OMS. 2ª ed. 1998. p. 160
Parnés A, Lagan KM. Larval therapy in wound management: a review. Int. J. Clin. Pract.. 2007;61(3):488-493. Doi: http://dx.doi.org/10.1111/j.1742-1241.2006.01238.x
Patarroyo M.A. Larval therapy in wound healing. Infectio. 2015;19(1):1-2. Doi: http://dx.doi.org/10.1016/j.infect.2014.12.003
Pinardi ME, Barrios M. Diagnóstico parasitológico de leishmaniasis cutánea americana. Dermatol Venez. 1993;31(2):18–21.
Pinheiro MA, Ferraz JB, Junior MA, Moura AD, Da Costa ME, Costa FJ et al. Use of maggot therapy for treating a diabetic foot ulcer colonized by multidrug resistant bacteria in Brazil. Indian J Med Res. 2015;141(3):340–342. Doi: https://doi.org/10.4103/0971-5916.156628
Pinilla YT, Moreno PDA, Patarroyo MA, Bello FJ. Proteolytic activity regarding Sarconesiopsis magellanica (Diptera: Calliphoridae) larval excretions and secretions. Acta Trop. 2013;128(3):686-691. Doi: https://doi.org/10.1016/j.actatropica.2013.09.020
Pinto EG, Tempone AG. Activity of the antiarrhythmic drug amiodarone against Leishmania (L.) infantum: an in vitro and in vivo approach. J Venom Anim Toxins Incl Trop Dis. 2018;24:29-34. Doi: https://doi.org/10.1186/s40409-018-0166-7
Polat E, Cakam H, Aslan M, Sirekbasan S, Kutlubay Z, Ipek T, et al. Detection of anti-leishmanial effect of the Lucilia sericata larval secretions in vitro and in vivo on Leishmania tropica: First work. Exp. Parasitol. 2012;132(2):129-134. Doi: https://doi.org/10.1016/j.exppara.2012.06.004
Polat E, Kutlubay Z. Four cutaneous leishmaniosis case resistant to meglumine antimoniate treatment. Turkiye Parazitol Derg. 2014;38(3):177-180. Doi: https://doi.org/10.5152/tpd.2014.3410
Ponte-Sucre A, Faber JH, Gulder T, Kajahn I, Pedersen SE, Schultheis M et al. Activities of naphthylisoquinoline alkaloids and synthetic analogs against Leishmania major. Antimicrob Agents Chemother. 2007;51(1):188-94. Doi: https://doi.org/10.1128/AAC.00936-06
Pöppel AK, Koch A, Kogel KH, Vogel H, Kollewe C, Wiesner J, et al. Lucimycin, an antifungal peptide from the therapeutic maggot of the common green bottle fly Lucilia sericata. Biol. Chem. 2014;395(6):649-656. Doi: https://doi.org/10.1515/hsz-2013-0263
Prezzavento G, Racca LL, Bottai HM. Cicatrización: evaluación de dos tratamientos tópicos de uso habitual en la cicatriz postcirugía estética. Cir. plást. iberolatinoam. 2017;43(3):255-263. Doi: https://doi.org//10.4321/s0376-78922017000400006
Rezzano S, Scorza JV. Comportamiento de Leishmania chagasi, L. mexicana y L. braziliensis en hámsteres machos inoculados subcutáneamente. Bol. Dir. Malariol y Saneam. Amb. 1985;25(3-4):59-66.
Ríos YJM, Mercadillo PP, Yuil RE, Rios CM. Terapia con larvas de mosca para heridas crónicas: alternativa en una época de creciente resistencia a los antimicrobianos. Dermatología CMQ. 2013;11(2):134-141.
Salomón OD, Sosa S, Rossi, G, Spinelli G. Presencia de Lutzomyia longipalpis y situación de la Leishmaniosis visceral en Argentina. Medicina. 2001;61(2):174-178.
Sánchez MC, Chuaire L, Narváez R, Segura NA. Biocirugía: utilización de larvas de insectos necrófagos en la curación de heridas. La terapia larval. Rev. Cienc. Salud. 2004;2(2):156-164.
Sanei-Dehkordi A, Khamesipour A, Akbarzadeh K, Akhavan AA, Mohammadi AMA, Mohammadi Y et al. Anti Leishmania activity of Lucilia sericata and Calliphora vicina maggots in laboratory models. Exp Parasitol. 2016;170:59-65. Doi: https://doi.org/10.1016/j.exppara.2016.08.007
Senet P. Fisiología de la cicatrización cutánea. EMC-Dermatología. 2008;42(1):1-10. Doi: https://doi.org/10.1016/S1761-2896(08)70356-XScorza Dagert JV, Morales C, Petit de Peña Y, Vásquez L, Rojas E, Scorza B. JV. Síntesis de un complejo antimonial pentavalente (Ulamina) y su aplicación experimental para el tratamiento de leishmaniasis cutánea localizada en Venezuela. Bol Mal Salud Amb. 2006;46(1):59-65.
Serrano-Martín X, García-Marchan Y, Fernández A, Rodriguez N, Rojas H, Visbal G, et al. Amiodarone Destabilizes Intracellular Ca2+ Homeostasis and Biosynthesis of Sterols in Leishmania mexicana. Antimicrob. Agents Chemother. 2009;53(4):1403-1410. Doi: https://doi.org/10.1128/AAC.01215-08
Sherman RA, Pechter EA. Maggot therapy: a review of the therapeutic applications of fly larvae in human medicine, especially for treating osteomyelitis. Med. Vet. Emtomol. 1988;2(3):225-230. Doi: https://doi.org/10.1111/j.1365-2915.1988.tb00188.x
Sherman RA. Maggot Therapy Takes Us Back to the Future of Wound Care: New and Improved Maggot Therapy for the 21st Century. J Diabetes Sci Technol. 2009;3(2):336-344. Doi: https://doi.org/10.1177/193229680900300215
Sherman RA, Mumcuoglu KY, Grassberger M, Tantawi TI. Maggot therapy. En: Biotherapy-History, Principles and Practice. Dordrecht: Springer, 2013. p. 5-29.
Shittu OK, Olayemi IK, Omalu ICJ, Adeniyi AK. Anti-plasmodial properties of methanolic extract of Musca domestica maggot on P. berghei – infected mice. IJBPAS. 2013;2(5):1064-1070.
Soto J, Soto P. Estado actual y futuro de la terapia anti-leishmaniásica en Colombia. Biomédica. 2006;26(Supl1):194-206. Doi: https://doi.org/10.7705/biomedica.v26i1.1513
Wang Y, Zhao Y, Lei C, Zhu F. Antiviral and antitumor activities of the protein fractions from the larvae of the housefly, Musca domestica. Afr. J. Biotechnol.. 2012;11(39):9468-9474. Doi: http://dx.doi.org/10.5897/AJB12.077
WHO. World Health Organization. Plan de acción mundial para la contención en el laboratorio de los poliovirus salvajes. Ginebra Suiza: Organización Mundial de la Salud. 2000. p. 35
Wolff Echeverri MI, Rivera Álvarez C, Herrera Higuita SE, Wolff Idárraga JC, Escobar Franco MM. Lucilia eximia (Diptera: Calliphoridae), una nueva alternativa para la terapia larval y reporte de casos en Colombia. Iatreia. 2010;23(2):107-116.
Zapata C, Bello FJ, Rey M, Castañeda A, González J, Acero V et al. Evaluación de la terapia larval en el proceso de curación de heridas infectadas con Pseudomonas aeruginosa en conejos. Rev Cienc Salud. 2008;6(2):9-24.
Zhu L, Wang P, Qin QL, Zhang H, Wu YJ. Protective effect of polypeptides from larva of housefly (Musca domestica) on hydrogen peroxideinduced oxidative damage in HepG2 cells. Food Chem Toxicol. 2013;60(1):385–390. Doi: https://doi.org/10.1016/j.fct.2013.07.074
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
CrossRef Cited-by
1. Shahida Anusha Siddiqui, Chujun Li, Owusu Fordjour Aidoo, Ito Fernando, Moawiya A. Haddad, Jorge A.M. Pereira, Andrey Blinov, Andrey Golik, José S. Câmara. (2023). Unravelling the potential of insects for medicinal purposes – A comprehensive review. Heliyon, 9(5), p.e15938. https://doi.org/10.1016/j.heliyon.2023.e15938.
2. Carlos H. Marchiori, Klebert P. Malheiros, Marco V.O. Santana, Marco V.O. Santana. (2024). Use of Fly Larvae (Insecta: Diptera) as an Alternative Treatment for Wounds. European Journal of Ecology, Biology and Agriculture, 1(2), p.71. https://doi.org/10.59324/ejeba.2024.1(2).06.
3. Frank Stadler. (2022). A Complete Guide to Maggot Therapy. https://doi.org/10.11647/obp.0300.
Dimensions
PlumX
Visitas a la página del resumen del artículo
Descargas
Licencia
Derechos de autor 2019 Acta Biológica Colombiana

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial-CompartirIgual 4.0.
1. La aceptación de manuscritos por parte de la revista implicará, además de su edición electrónica de acceso abierto bajo licencia Attribution-NonCommercial-ShareAlike 4.0 (CC BY NC SA), la inclusión y difusión del texto completo a través del repositorio institucional de la Universidad Nacional de Colombia y en todas aquellas bases de datos especializadas que el editor considere adecuadas para su indización con miras a incrementar la visibilidad de la revista.
2. Acta Biológica Colombiana permite a los autores archivar, descargar y compartir, la versión final publicada, así como las versiones pre-print y post-print incluyendo un encabezado con la referencia bibliográfica del articulo publicado.
3. Los autores/as podrán adoptar otros acuerdos de licencia no exclusiva de distribución de la versión de la obra publicada (p. ej.: depositarla en un archivo telemático institucional o publicarla en un volumen monográfico) siempre que se indique la publicación inicial en esta revista.
4. Se permite y recomienda a los autores/as difundir su obra a través de Internet (p. ej.: en archivos institucionales, en su página web o en redes sociales cientificas como Academia, Researchgate; Mendelay) lo cual puede producir intercambios interesantes y aumentar las citas de la obra publicada. (Véase El efecto del acceso abierto).



















