Eficacia y seguridad de la terbinafina oral en pauta intermitente o pulsátil versus pauta continua para el tratamiento de la onicomicosis en mayores de 18 años
Efficacy and safety of oral terbinafine in intermittent or pulsatile pattern versus continuous pattern for the treatment of Onychomycosis in patients older than 18 years
DOI:
https://doi.org/10.15446/revfacmed.v64n1.47890Palabras clave:
Onicomicosis, Ensayo clínico, Trichophyton, Efectividad, Revisión. (es)Onychomycosis, Clinical Trial, Trichophyton, Review, Effectiveness (en)
Antecedentes. La onicomicosis es una enfermedad que compromete las uñas y afecta el 5% de la población mundial.
Objetivo. Determinar la efectividad y seguridad de la terbinafina oral en pauta intermitente versus continua para la onicomicosis en mayores de 18 años.
Materiales y métodos. A través de una búsqueda sistemática electrónica en Cochrane, Medline, Embase, LILACS y Opengrey se identificaron ensayos clínicos aleatorizados paralelos, excluyendo cruzados, conglomerados o clúster. Se aplicó el RevMan 5.3 para revisiones sistemáticas de ensayos clínicos.
Mediante búsqueda sistemática se identificaron ensayos clínicos aleatorizados paralelos en pacientes mayores de 18 años, de sexo masculino o femenino, humanos, en idioma inglés y español, sin límite de tiempo de publicación y cuyo desenlace fue la curación clínica y micológica, incluyendo efectos adversos leves. Se valoró el riesgo de sesgo; se utilizó RR como medida del efecto, IC95% para variables dicotómicas; la unidad de análisis fue el paciente y la estimación agrupada se calculó usando un modelo de efectos aleatorios para variables dicotómicas —método de Mantel-Haenszel en RevMan 5.3—.
Resultados. El RR agrupado fue de 1.13 (IC95%: 1.06-1.2) indicando que la falla del tratamiento con terbinafina intermitente es 1.1 veces más probable que con terbinafina continua. Su RR agrupado dio 0.923 (IC95%: 0.77-1.09) indicando 7.7% de mayor probabilidad de desarrollar eventos adversos con terbinafina continua que con intermitente.
Conclusiones. La terbinafina intermitente tiene menor éxito de cura clínica y micológica que la continua; su RR corregido demuestra que la pauta intermitente es 13% menos eficiente que la continua. Clínicamente los hallazgos son significativos pero estadísticamente falta poder en los estudios y un mayor tamaño de muestra agrupado para mejorar la evidencia.
Background. Onychomycosis is a disease involving nails. It affects 5% of the world population.
Objective. To determine the effectiveness and safety of oral terbinafine in intermittent pattern versus a continuous pattern for onychomycosis in patients older than 18 years.
Materials and Methods. Through an online systematic search in Cochrane, MEDLINE, EMBASE, Latino-Americana [Literature] (LILACS) and Opengrey, parallel randomized clinical trials, excluding crusaders, conglomerates or cluster, were identified. RevMan 5.3 for systematic reviews of clinical trials was applied.
Through a systematic search were identified parallel randomized clinical trials in ≥18 years, male or female, human, in English and Spanish, without time limit of publication and whose outcome was clinical and mycological cure, including mild adverse effects. The risk of bias was assessed. RR was used as a measure of effect, 95% CI for dichotomous variables. The unit of analysis was the patient and the pooled estimate was calculated using a random effects model for dichotomous variables, Mantel-Haenszel method in RevMan 5.3.
Results. The pooled RR was 1.13 [95% CI: 1.06 - 1.2] which indicates that treatment failure with intermittent terbinafine is 1.1 times more likely to happen than that with continuous terbinafine. In turn, continuous terbinafine pooled RR was 0.923 [95% CI: 0.77 - 1.09] indicating a 7.7% higher chance of developing adverse events for the treatment with continuous terbinafine.
Conclusions. Intermittent terbinafine is less successful in terms of clinical and mycological cure than the continuous treatment. Its corrected RR shows that the intermittent pattern is 13% less efficient than the continuous one. Clinically, these findings are significant but the studies lack power statistically and a larger clustered sample is necessary to improve the evidence.
INVESTIGACIÓN ORIGINAL
DOI: https://doi.org/10.15446/revfacmed.v64n1.47890
Eficacia y seguridad de la terbinafina oral en pauta intermitente o pulsátil versus pauta continua para el tratamiento de la onicomicosis en mayores de 18 años
Efficacy and safety of oral terbinafine in intermittent or pulsatile pattern versus continuous pattern for the treatment of Onychomycosis in patients older than 18 years
Ernesto Andrade-Cerquera1
Recibido: 16/12/2014 Aceptado: 16/06/2015
1 Universidad Nacional de Colombia - Sede Bogotá - Facultad de Medicina - Instituto de Investigaciones Clínicas - Bogotá, D.C. - Colombia.
Correspondencia: Ernesto Andrade-Cerquera. Calle 43 No. 19-107. Teléfono: +57 3142190723. Neiva. Colombia. Correo electrónico: eandradec@unal.edu.co.
| Resumen |
Antecedentes. La onicomicosis es una enfermedad que compromete las uñas y afecta el 5% de la población mundial.
Objetivo. Determinar la efectividad y seguridad de la terbinafina oral en pauta intermitente versus continua para la onicomicosis en mayores de 18 años.
Materiales y métodos. A través de una búsqueda sistemática electrónica en Cochrane, Medline, Embase, LILACS y Opengrey se identificaron ensayos clínicos aleatorizados paralelos, excluyendo cruzados, conglomerados o clúster. Se aplicó el RevMan 5.3 para revisiones sistemáticas de ensayos clínicos.
Mediante búsqueda sistemática se identificaron ensayos clínicos aleatorizados paralelos en pacientes mayores de 18 años, de sexo masculino o femenino, humanos, en idioma inglés y español, sin límite de tiempo de publicación y cuyo desenlace fue la curación clínica y micológica, incluyendo efectos adversos leves. Se valoró el riesgo de sesgo; se utilizó RR como medida del efecto, IC95% para variables dicotómicas; la unidad de análisis fue el paciente y la estimación agrupada se calculó usando un modelo de efectos aleatorios para variables dicotómicas —método de Mantel-Haenszel en RevMan 5.3—.
Resultados. El RR agrupado fue de 1.13 (IC95%: 1.06-1.2) indicando que la falla del tratamiento con terbinafina intermitente es 1.1 veces más probable que con terbinafina continua. Su RR agrupado dio 0.923 (IC95%: 0.77-1.09) indicando 7.7% de mayor probabilidad de desarrollar eventos adversos con terbinafina continua que con intermitente.
Conclusiones. La terbinafina intermitente tiene menor éxito de cura clínica y micológica que la continua; su RR corregido demuestra que la pauta intermitente es 13% menos eficiente que la continua. Clínicamente los hallazgos son significativos pero estadísticamente falta poder en los estudios y un mayor tamaño de muestra agrupado para mejorar la evidencia.
Palabras clave: Onicomicosis; Ensayo clínico; Trichophyton; Efectividad; Revisión (DeCS).
Andrade-Cerquera E. Eficacia y seguridad de la terbinafina oral en pauta intermitente o pulsátil versus pauta continua para el tratamiento de la onicomicosis en mayores de 18 años. Rev. Fac. Med. 2016;64(1):59-66. Spanish. doi: https://doi.org/10.15446/revfacmed.v64n1.47890.
Summary
Background. Onychomycosis is a disease involving nails. It affects 5% of the world population.
Objective. To determine the effectiveness and safety of oral terbinafine in intermittent pattern versus a continuous pattern for onychomycosis in patients older than 18 years.
Materials and Methods. Through an online systematic search in Cochrane, MEDLINE, EMBASE, Latino-Americana [Literature] (LILACS) and Opengrey, parallel randomized clinical trials, excluding crusaders, conglomerates or cluster, were identified. RevMan 5.3 for systematic reviews of clinical trials was applied.
Through a systematic search were identified parallel randomized clinical trials in ≥18 years, male or female, human, in English and Spanish, without time limit of publication and whose outcome was clinical and mycological cure, including mild adverse effects. The risk of bias was assessed. RR was used as a measure of effect, 95% CI for dichotomous variables. The unit of analysis was the patient and the pooled estimate was calculated using a random effects model for dichotomous variables, Mantel-Haenszel method in RevMan 5.3.
Results. The pooled RR was 1.13 [95% CI: 1.06 - 1.2] which indicates that treatment failure with intermittent terbinafine is 1.1 times more likely to happen than that with continuous terbinafine. In turn, continuous terbinafine pooled RR was 0.923 [95% CI: 0.77 - 1.09] indicating a 7.7% higher chance of developing adverse events for the treatment with continuous terbinafine.
Conclusions. Intermittent terbinafine is less successful in terms of clinical and mycological cure than the continuous treatment. Its corrected RR shows that the intermittent pattern is 13% less efficient than the continuous one. Clinically, these findings are significant but the studies lack power statistically and a larger clustered sample is necessary to improve the evidence.
Keywords: Onychomycosis; Clinical Trial; Trichophyton; Review; Effectiveness (MeSH).
Andrade-Cerquera E. [Efficacy and safety of oral terbinafine in intermittent or pulsatile pattern versus continuous pattern for the treatment of Onychomycosis in patients older than 18 years]. Rev. Fac. Med. 2016;64(1):59-66. Spanish. doi: https://doi.org/10.15446/revfacmed.v64n1.47890.
Introducción
La onicomicosis es una enfermedad que compromete las uñas de manos y pies, afecta el 5% de la población mundial y es la principal patología de las uñas. La tasa de prevalencia es determinada por la edad, la clase social, la ocupación, el clima, el ambiente de vida y la frecuencia de viajes. Las inmunodeficiencias como el HIV y la diabetes pueden aumentar su prevalencia, al igual que problemas circulatorios periféricos, sedentarismo, trauma frecuente y uso prolongado de antibióticos sistémicos (1).
En Estados Unidos su prevalencia varía entre 2-3% y su incidencia varia con la edad, siendo aproximadamente 30% en mayores de 60 años y 0.2% en menores de 16 años. Los dermatofitos son los principales microorganismos causales con cerca del 90 y 50% de afección de uñas de pies y manos, respectivamente. El dermatofito con más frecuencia aislado es el trichophyton rubrum (2).
Los criterios diagnósticos son clínico —afección de la consistencia y apariencia de la uña— y micológico —identificación por examen microscópico directo con aislamiento en cultivo—.
La terbinafina es un medicamento sistémico perteneciente al grupo de las alilaminas, interfiere en la síntesis del ergosterol con efecto fungistático y genera una acumulación tóxica intracelular de escualeno con efecto fungicida (3).
Su dosis vía oral aprobada por la Agencia de Alimentos y Medicamentos (FDA por sus siglas en inglés) se puede dar en dos pautas: la forma continua de 250mg al día y la intermitente o pulsátil de 250mg cada 12 horas por una semana al mes y tres siguientes de descanso por un periodo total de 12 semanas de tratamiento.
Con esta revisión sistemática se pretende determinar la efectividad y seguridad de la terbinafina oral en pauta intermitente o pulsátil versus pauta continua para el tratamiento de la onicomicosis en mayores de 18 años, con el fin de tomar decisiones basadas en la evidencia de ensayos clínicos aleatorizados, evitando efectos adversos del medicamento y costos elevados por pautas de tratamiento prolongadas.
Metodología
Se realizó una búsqueda sistemática en Cochrane, Medline, Embase, LILACS y Opengrey para identificar ensayos clínicos aleatorizados paralelos —excluyendo cruzados, conglomerados o clúster— en pacientes mayores de 18 años, sexo masculino o femenino, humanos, en idioma inglés y español, sin límite de tiempo de publicación, con intervención de terbinafina vía oral en pauta intermitente o pulsátil versus continua con tiempo máximo de 12 semanas de tratamiento. Su desenlace a evaluar fue la curación clínica y micológica, incluyendo los efectos adversos leves como nausea, disgeusia, dispepsia y cefalea.
Dos revisores evaluaron la elegibilidad y la calidad metodológica de los ensayos sin considerar los resultados. La evaluación de los ensayos no fue cegada ya que se conocía el nombre del autor, la institución y la fuente de publicación, las razones de exclusión se detallan en la Tabla 1. Cualquier desacuerdo se resolvió hasta alcanzar un consenso.
Se valoró el riesgo de sesgo en bajo riesgo, alto riesgo o riesgo poco claro de los estudios seleccionados; se utilizó el RR como medida del efecto con un IC95% para variables dicotómicas y su unidad de análisis fue el paciente. La estimación agrupada de los estudios fue calculada usando un modelo de efectos aleatorios para variables dicotómicas con el método de Mantel-Haenszel en RevMan 5.3 (4). Los resultados se analizaron sobre análisis por protocolo.
Se evaluó la heterogeneidad estadística con el I²=>30% indicando heterogeneidad y >50% heterogeneidad significativa. Se realizó un análisis de sensibilidad por tiempo de seguimiento de 48 y 72 semanas para la efectividad y seguridad del medicamento; igualmente se realizó análisis de sensibilidad por alto o bajo riesgo de sesgo.
Resultados
Se identificaron 130 estudios en la búsqueda electrónica, pero solo 9 se seleccionaron para su lectura completa, cuatro fueron excluidos porque no cumplieron con los criterios y objetivo de la revisión (5-8) (Tabla 1) y cinco ensayos clínicos se incluyeron en el análisis cualitativo y cuantitativo (9-13) (Tabla 2 y Figura 1). No se evidenciaron ensayos clínicos en literatura gris electrónica o manual ni se realizó un análisis de sesgo de publicación, teniendo en cuenta que se encontraron muy pocos estudios disponibles en la literatura que cumplieran con los criterios de inclusión de la presente revisión y algunos de ellos presentaban alta heterogeneidad.
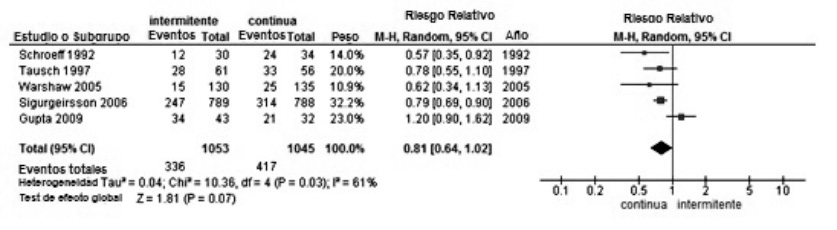
Figura 1. Prisma. Fuente: Elaboración propia.
Tabla 1. Características de los estudios clínicos excluidos.
|
Título |
Efficacy and safety of terbinafine for nondermatophyte and mixed nondermatophyte and dermatophyte toenail onychomycosis |
Oral terbinafine in the treatment of toenail onychomycosis: North American Multicenter Trial |
Treatment of dermatophyte nail infections: An open randomized study comparing intermittent terbinafine therapy with continuous terbinafme treatment and intenmittent itraconazole therapy |
Short-duration therapy with terbinafine for dermatophyte onychomycosis: A multicentre trial |
|
ID |
Lebwohl 2001 (5) |
Drake 1997 (6) |
Tosti 1996 (7) |
Goodfield 1992 (8) |
|
Intervención |
Terbinafina 250mg/día por 12 semanas seguida de 12 semanas de pausa. Total 24 semanas (intermitente) |
Terbinafina 250mg/día por 12 semanas vs por 24 semanas seguidas. Total 24 semanas (no intermitente) |
Terbinafina 500mg día por 1 semana cada mes. Total 16 semanas (intermitente) |
Terbinafina 250mg/día por 12 semanas. |
|
Razón de exclusión |
Se excluye porque el tiempo de tratamiento excede las 12 semanas. |
Se excluye porque el tiempo de tratamiento excede las 12 semanas y no es intermitente. |
Se excluye porque el tiempo de tratamiento excede las 12 semanas. |
Se excluye porque su grupo de comparación es el placebo. |
Fuente: Elaboración propia.
Tabla 2. Características de los estudios clínicos incluidos.
|
ID Estudio |
Gupta 2009 (9) |
Sigurgeirsson 2006 (10) |
Warshaw 2005 (11) |
Tausch 1997 (12) |
Schroeff 1992 (13) |
|
Tiempo del estudio |
Agosto 1999-Junio 2003 |
Septiembre 2002-Noviembre 2003 |
Septiembre 1998-Febrero 2000 |
No referido |
No referido |
|
Lugar |
Canadá |
Multicéntrico |
USA |
Multicéntrico |
Multicéntrico |
|
Intervención |
Terbinafina 250mg/día por 4 semanas seguida de 4 semanas de pausa. Total 12 semanas |
Terbinafina 350mg/día por 2 semanas seguida de 2 semanas de pausa. Total 12 semanas |
Terbinafina 500mg día por 1 semana cada mes. Total 12 semanas |
Terbinafina 250mg/día por 6 semanas seguida de 6 semanas de pausa. Total 12 semanas |
Terbinafina 250mg/día por 6 semanas, placebo siguientes semanas. Total 12 semanas |
|
Comparador |
Terbinafina 250mg/día por 12 semanas |
Terbinafina 250mg/día por 12 semanas |
Terbinafina 250mg/día por 12 semanas |
Terbinafina 250mg/día por 12 semanas |
Terbinafina 250mg/día por 12 semanas |
|
Diseño del estudio |
ECA paralelo |
ECA paralelo |
ECA paralelo |
ECA paralelo |
ECA paralelo |
|
Aleatorización |
Sí, no describen procedimiento. |
Sí, realizada por Novartis con sistema automatizado validado con números aleatorizados. |
Sí, generada por computador en bloques de 50 participantes. |
Sí, por múltiples bloques de cuatro números de identificación del paciente. |
Sí, no se explica el proceso de aleatorización. |
|
Cegamiento |
Del staff de evaluadores clínicos cegados. El laboratorio de evaluación de muestras fue cegado. No es claro el cegamiento de los pacientes pues refieren administración del medicamento desde una farmacia local con prescripción y autoadministración. |
Doble ciego, no se explica cómo fue el enmascaramiento. |
Triple ciego: médicos, participantes y personal investigador. Enmascaramiento de las capsulas con placebo e indiferenciadas en su presentación. Doble capsula los primeros siete días de cada mes (placebo-medicamento) |
Doble ciego a los pacientes con placebo enmascarado en las segundas seis semanas en el grupo de intervención. |
Doble ciego, no se explica el enmascaramiento. |
|
Desenlace |
Cura micológica (KOH y cultivo negativo) + cura clínica (≤10% placa uña comprometida). |
Cura micológica (KOH y cultivo negativo) + cura clínica (≤10% placa uña comprometida). |
Cura micológica (KOH y cultivo negativo) + cura clínica (crecimiento normal de las 10 uñas). |
Cura micológica (KOH y cultivo negativo) + cura clínica (crecimiento progresivo uña). |
Cura micológica (KOH y cultivo negativo) + cura clínica (crecimiento progresivo uña). |
|
Seguimiento |
72 semanas |
48 semanas |
72 semanas |
48 semanas |
48 semanas |
|
Edad |
≥18 años |
≥18 años |
≥18 años |
≥18 años |
≥18 años |
|
Análisis |
Por protocolo |
Por protocolo |
Por protocolo |
Por protocolo |
Por protocolo |
|
Financiación |
No declarada, conflicto de interés no declarado. |
No declarada. |
Declarada, centro médico veterano de Minneapolis. |
Sandoz AG Nuremberg; conflicto de dos autores: trabajan para Sandoz. |
No declarada |
|
Intervención |
34 |
247 |
15 |
28 |
12 |
|
Total |
43 |
789 |
130 |
61 |
30 |
|
Comparador |
21 |
314 |
25 |
33 |
24 |
|
Total |
32 |
788 |
135 |
56 |
34 |
|
Efectos Adversos intervención |
22 |
140 |
8 |
28 |
Total de 32 no discriminados por grupo. |
|
Efectos Adversos comparador |
8 |
164 |
10 |
30 |
|
|
Perdidas del seguimiento |
14/63: intervención 5/40: comparador |
107/1011: intervención 94/994: comparador |
23/153: intervención 18/153: comparador |
11/72: intervención 20/76:comparador |
8/38:intervención 8/42:comparador |
Fuente: Elaboración propia.
Tres estudios tuvieron seguimiento de 48 semanas y dos de 72 semanas; cuatro tuvieron doble cegamiento y uno cegamiento triple. En los cinco estudios el desenlace fue la cura clínica y micológica simultánea y su análisis fue por protocolo. Tres de los cinco estudios fueron multicéntricos.
El RR agrupado para cura clínica y micológica de los cinco estudios fue 0.81 (IC95%: 0.64-1.02) con un I²=61%, lo cual muestra heterogeneidad alta y no es estadísticamente significativo (Figura 2). El RR independiente para cada estudio muestra que es menor de 1, evidenciando que los expuestos a la intervención tienen menor probabilidad de éxito que los expuestos a la comparación, sin embargo sus intervalos de confianza pasan por la unidad lo cual los hace estadísticamente no significativos.

Figura 2. Cura clínica y micológica. Fuente: Elaboración propia.
Tres estudios incluidos con bajo riesgo de sesgo para cura clínica y micológica obtuvieron un RR agrupado de 0.78 (IC95%: 0.69-0.88) a favor de la terbinafina continua con un I²=0%, el cual puede ser tomado en cuenta para su análisis por tratarse de estudios clínicos homogéneos (Figura 3). Otros tres estudios demostraron la cura clínica y micológica a las 48 semanas de seguimiento con RR agrupado de 0.77 (IC95%: 0.68-0.87) a favor de la comparación con I²=0%, demostrando que son estudios homogéneos. Dos estudios de 72 semanas de seguimiento demostraron la cura clínica y micológica con RR agrupado de 0.90 (IC95%: 0.43–1.89) con I²=80% mostrando la más alta heterogeneidad.
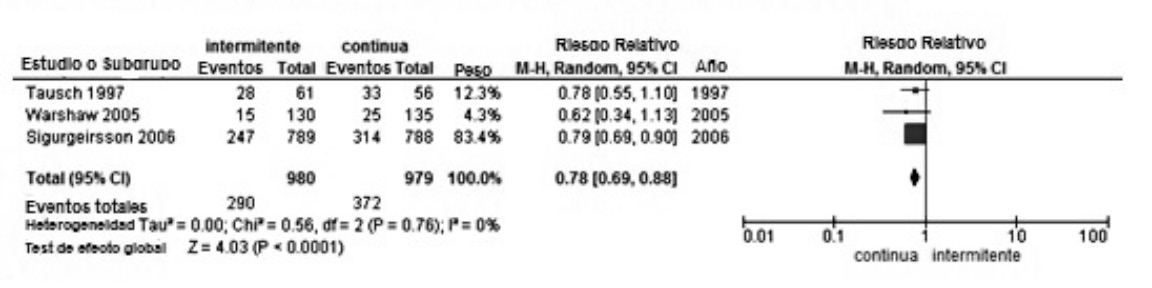
Figura 3. Cura clínica y micológica en estudios de bajo riesgo de sesgo. Fuente: Elaboración propia.
El RR agrupado corregido para los cinco estudios fue de 1.13 (IC95%: 1.06-1.2) indicando que la falla del tratamiento con terbinafina intermitente es 1.1 veces más probable que con terbinafina continua, resultado muy similar al analizar los tres estudios con cura clínica y micológica a las 48 semanas de seguimiento con un RR 1.16 (IC95%: 1.08-1.25), sin embargo no son estadísticamente significativos (Tabla 3). Los efectos adversos mostraron un RR agrupado de 0.98 (IC95%: 0.71-1.34) en cuatro estudios incluidos, siendo los efectos adversos más frecuentes en la terbinafina continua con un I²=52%, mostrando heterogeneidad significativa pero estadísticamente no significativos (Figura 4). Su RR agrupado corregido da 0.923 (IC95%: 0.77-1.09) indicando 7.7% de mayor probabilidad a desarrollar eventos adversos con la terbinafina continua que con la intermitente.
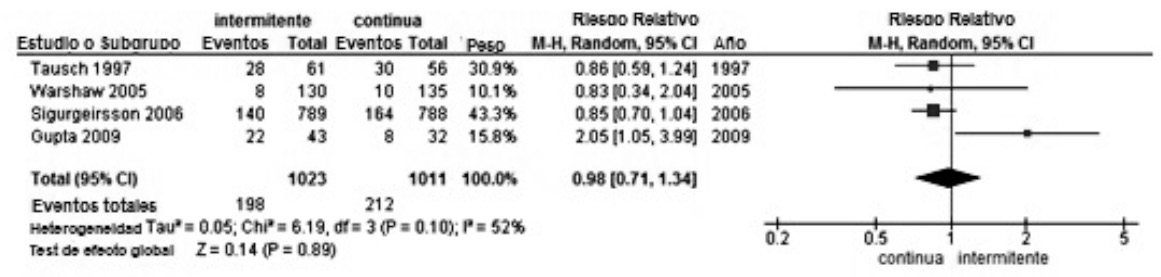
Figura 4. Efectos adversos leves. Fuente: Elaboración propia.
Tabla 3. GRADE de cura clínica, micológica y efectos adversos leves.
|
Evaluación de calidad |
Número de pacientes |
Efecto |
Cali- dad |
Impor-tancia |
||||||||
|
Número de Estudios |
Diseño |
Riesgo de sesgos |
Inconsis- tencia |
Incerti- dumbre |
Impre-cisión |
Otras conside- raciones |
Terbinafina oral pauta pulsátil o intermitente |
Terbinafina oral pauta continua |
Relativo (95% CI) |
Abso- luto |
||
|
Cura clínica y micológica (seguimiento 48-72 semanas ) |
||||||||||||
|
5 |
Ensayos aleatorios |
Serios1 |
Serios2 |
Sin seria incertidumbre3 |
Sin seria imprecisión4 |
Ninguno5,6 |
717/1053 (68.1%) |
628/1045 (60.1%) |
RR 1.13 (1.06 a 1.2) |
78 más por 1000 (desde 36 a más de 120) |
BAJA |
CRÍTICA |
|
|
0% |
|
||||||||||
|
Efectos adversos leves (gastrointestinal, cefalea, mareo) (seguimiento 48-72 semanas) |
||||||||||||
|
4 |
Ensayos aleatorios |
Sin riesgo grave de sesgos1 |
Serios2 |
Sin seria incertidumbre3 |
Sin seria imprecisión4 |
Ninguno5,6 |
198/1030 (19.2%) |
212/1011 (21%) |
RR 0.923 (0.77 a 1.09) |
16 menos por 1000 (desde 48 a menos de 19) |
MODERADA |
CRÍTICA |
|
|
0% |
|
||||||||||
1 Uno de los cinco estudios presenta un dominio de sesgo valorado por no ser claro el proceso de aleatorización y ocultamiento de la asignación.
2 Se considera que existe heterogeneidad en la visión global de los estudios con reporte de I2=52%, además la comparación con terbinafina continua es igual para todos los estudios en 250mg/día por 12 semanas, mientras la intervención de terbinafina pulsátil o intermitente es diferente tanto en dosis como en tiempo de pausas.
3 No se presenta indirección en los estudios ya que abordan de manera directa las comparaciones de las dos pautas de tratamiento con terbinafina sin utilizar comparaciones indirectas con placebo; de igual manera las edades son aplicables al objetivo del estudio y sus criterios de inclusión y exclusión son adecuados acordes a los objetivos de la revisión.
4 Se evidencian intervalos de confianza estrechos que pasan por el 1 indicando que no son estadísticamente significativos. Clínicamente son resultados importantes, pero se requiere aumentar el tamaño de muestra para mejorar su significancia estadística.
5 No se considera evidencia de sesgo de publicación en los estudios y la evaluación de los riesgos de sesgos es baja.
6 No se expusieron en los estudios posibles factores confusores que sobreestimen o subestimen el efecto teniendo en cuenta los criterios de inclusión y exclusión estrictos para la ejecución de los ECAS.
Fuente: Elaboración propia.
Se encuentran en el análisis de riesgo de sesgo dos estudios con dos o más dominios comprometidos en su evaluación por riesgo de sesgo poco claro (Figura 5).
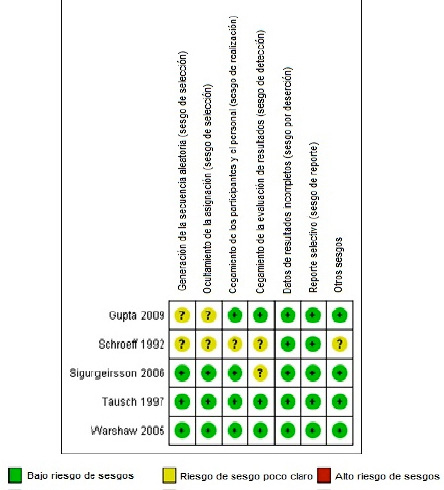
Figura 5. Resumen del riesgo de sesgo. Fuente: Elaboración propia.
Discusión
Esta revisión sistemática muestra que la terbinafina intermitente tiene menor éxito de cura clínica y micológica que la continua. Su RR corregido de 1.13 demuestra que la pauta intermitente es 13% menos eficiente que la continua. Según Gupta et al. (14), el resultado concuerda con la presente revisión en que el uso de terbinafina continua es significativamente superior al uso de terbinafina intermitente para cura micológica, pero requiere mayor número de estudios clínicos y tamaño de muestra para el análisis de costos del tratamiento, efectos adversos y recurrencia de la enfermedad.
En la práctica clínica se puede utilizar cualquiera de las dos pautas de tratamiento con terbinafina, ya que su efectividad es alta con relación a la cura micológica y tiene efectos adversos leves; aunque no resulta concluyente con relación a los costos del tratamiento y a los múltiples antimicóticos mixtos existentes para el manejo de la onicomicosis.
Los efectos adversos muestran mayor probabilidad de presentarse en la pauta continua que en la intermitente. Clínicamente los hallazgos son significativos pero estadísticamente falta poder en los estudios y un mayor tamaño de muestra agrupado para mejorar la evidencia.
Se requiere de mayor investigación para la pauta intermitente con ensayos clínicos controlados aleatorizados, menos riesgo de sesgos y una dosis especifica con periodos de pausa establecidos para evitar la alta heterogeneidad mostrada con el I² en los RR agrupados, y así poder establecer la cura clínica y micológica, el costo y los eventos adversos asociados comparados con la pauta continua.
Conflicto de intereses
Ninguno declarado por los autores.
Financiación
Ninguna declarada por los autores.
Agradecimientos
A los doctores Juan Pablo Alzate Granados y Cesar Ricardo Huérfano Herrera, estudiantes de la maestría de epidemiologia clínica de la Universidad Nacional; reconocimiento especial al equipo de docentes de la catedra de revisiones sistemáticas en cabeza del médico ginecólogo Hernando Guillermo Gaitán Duarte, de esta misma maestría.
Referencias
1. Kaur R, Kashyap B, Bhalla P. Onychomycosis - epidemiology, diagnosis and management. Indian J. Med. Microbiol. 2008;26(2):108-116. http://doi.org/cwb6tq.
2. Mendoza N, Palacios C, Cardona N, Gómez LM. Onicomicosis: afección común de difícil tratamiento. Rev. Asoc. Colomb. Dermatol. 2012;20(2): 149-158.
3. Garmendia JL, Idigoras-Viedma P, Mendiola-Arza J. Onicomicosis: diagnóstico y tratamiento. Inf. Ter. Sist. Nac. Salud. 2008;32(3):83-92.
4. Higgins JPT, Green S, editors. Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0. The Cochrane Collaboration, 2011. [updated 2011 Mar; Cited 2014 Dec 8]. Available from: http://goo.gl/bYXxCW.
5. Lebwohl MG, Daniel CR, Leyden J, Mormon M, Shavin JS, Tschen E, et al. Efficacy and safety of terbinafine for nondermatophyte and mixed nondermatophyte and dermatophyte toenail onychomycosis. Int. J. Dermatol. 2001;40(5):358-60. http://doi.org/d75xkk.
6. Drake LA, Shear NH, Arlette JP, Cloutier R, Danby FW, Elewski BE, et al. Oral terbinafine in the treatment of toenail onychomycosis: North American multicenter trial. J. Am. Acad. Dermatol. 1997;37(5):740-5. http://doi.org/dqhr9c.
7. Tosti A, Piraccini BM, Stinchi C, Venturo N, Bardazzi F, Colombo MD. Teatment of dermatophyte nail infections: an open randomized study comparing intermittent terbinafine therapy with continuous terbinafine treatment and intermittent itraconazole therapy. J. Am. Acad. Dermatol. 1996;34(4):595-600. http://doi.org/c7b7qn.
8. Goodfield MJ. Short-duration therapy with terbinafine for dermatophyte onychomycosis: a multicentre trial. Br. J. Dermatol. 1992;126(Suppl 39): 33-5. http://doi.org/fcxgfq.
9. Gupta AK, Lynch LE, Kogan N, Cooper EA. The use of an intermittent terbinafine regimen for the treatment of dermatophyte toenail onychomycosis. J. Eur. Acad. Dermatol. Venereol. 2009;23(3):256-62. http://doi.org/dzfmnq.
10. Sigurgeirsson B, Elewski BE, Rich PA, Opper C, Cai B, Nyirady J, et al. Intermittent versus continuous terbinafine in the treatment of toenail onychomycosis: A randomized, double-blind comparison. J. Dermatolog Treat. 2006;17(1):38-44. http://doi.org/bt796x.
11. Warshaw EM, Fett DD, Bloomfield HE, Grill JP, Nelson DB, Quintero V, et al. Pulse versus continuous terbinafine for onychomycosis: A randomized, double-blind, controlled trial. J. Am. Acad. Dermatol. 2005;53(4):578-84. http://doi.org/bfbjg5.
12. Tausch I, Brautigam M, Weidrnger G, Jones TC. Evaluation of 6 weeks treatment of terbinafine in tinea unguium in a double-blind trial comparing 6 and 12 weeks therapy. he Lagos V Study Group. Br. J. Dermatol. 1997;136(5):737-42. http://doi.org/djn4z5
13. van der Schroeff JG, Cirkel PK, Crijns MB, Van Dijk TJ, Govaert FJ, Groeneweg DA, et al. A randomized treatment duration-finding study of terbinafine in onychomycosis. Br. J. Dermatol. 1992;126(Suppl 39):36-9. http://doi.org/dsh2gv.
14. Gupta AK, Paquet M, Simpson F, Tavakkol A. Terbinafine in the treatment of dermatophyte toenail onychomycosis: a meta-analysis of efficacy for continuous and intermittent regimens. J. Eur. Acad. Dermatol. Venereol. 2013;27(3):267-72. http://doi.org/bbhp.
Referencias
Kaur R, Kashyap B, Bhalla P. Onychomycosis - epidemiology, diagnosis and management. Indian J. Med. Microbiol. 2008;26(2):108-116. http://doi.org/cwb6tq.
Mendoza N, Palacios C, Cardona N, Gómez LM. Onicomicosis: afección común de difícil tratamiento. Rev. Asoc. Colomb. Dermatol. 2012;20(2): 149-158.
Garmendia JL, Idigoras-Viedma P, Mendiola-Arza J. Onicomicosis: diagnóstico y tratamiento. Inf. Ter. Sist. Nac. Salud. 2008;32(3):83-92.
Higgins JPT, Green S, editors. Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0. The Cochrane Collaboration, 2011. [updated 2011 Mar; Cited 2014 Dec 8]. Available from: http://goo.gl/bYXxCW.
Lebwohl MG, Daniel CR, Leyden J, Mormon M, Shavin JS, Tschen E, et al. Efficacy and safety of terbinafine for nondermatophyte and mixed nondermatophyte and dermatophyte toenail onychomycosis. Int. J. Dermatol. 2001;40(5):358-60. http://doi.org/d75xkk.
Drake LA, Shear NH, Arlette JP, Cloutier R, Danby FW, Elewski BE, et al. Oral terbinafine in the treatment of toenail onychomycosis: North American multicenter trial. J. Am. Acad. Dermatol. 1997;37(5):740-5. http://doi.org/dqhr9c.
Tosti A, Piraccini BM, Stinchi C, Venturo N, Bardazzi F, Colombo MD. Teatment of dermatophyte nail infections: an open randomized study comparing intermittent terbinafine therapy with continuous terbinafine treatment and intermittent itraconazole therapy. J. Am. Acad. Dermatol. 1996;34(4):595-600. http://doi.org/c7b7qn.
Goodfield MJ. Short-duration therapy with terbinafine for dermatophyte onychomycosis: a multicentre trial. Br. J. Dermatol. 1992;126(Suppl 39): 33-5. http://doi.org/fcxgfq.
Gupta AK, Lynch LE, Kogan N, Cooper EA. The use of an intermittent terbinafine regimen for the treatment of dermatophyte toenail onychomycosis. J. Eur. Acad. Dermatol. Venereol. 2009;23(3):256-62. http://doi.org/dzfmnq.
Sigurgeirsson B, Elewski BE, Rich PA, Opper C, Cai B, Nyirady J, et al. Intermittent versus continuous terbinafine in the treatment of toenail onychomycosis: A randomized, double-blind comparison. J. Dermatolog Treat. 2006;17(1):38-44. http://doi.org/bt796x.
Warshaw EM, Fett DD, Bloomfield HE, Grill JP, Nelson DB, Quintero V, et al. Pulse versus continuous terbinafine for onychomycosis: A randomized, double-blind, controlled trial. J. Am. Acad. Dermatol. 2005;53(4):578-84. http://doi.org/bfbjg5.
Tausch I, Brautigam M, Weidrnger G, Jones TC. Evaluation of 6 weeks treatment of terbinafine in tinea unguium in a double-blind trial comparing 6 and 12 weeks therapy. he Lagos V Study Group. Br. J. Dermatol. 1997;136(5):737-42. http://doi.org/djn4z5.
van der Schroeff JG, Cirkel PK, Crijns MB, Van Dijk TJ, Govaert FJ, Groeneweg DA, et al. A randomized treatment duration-finding study of terbinafine in onychomycosis. Br. J. Dermatol. 1992;126(Suppl 39):36-9. http://doi.org/dsh2gv.
Gupta AK, Paquet M, Simpson F, Tavakkol A. Terbinafine in the treatment of dermatophyte toenail onychomycosis: a meta-analysis of efficacy for continuous and intermittent regimens. J. Eur. Acad. Dermatol. Venereol. 2013;27(3):267-72. http://doi.org/bbhp.
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
CrossRef Cited-by
1. Kenia Caridad Sánchez Espinosa, Lilivet Díaz Vázquez, Michel Almaguer, Carlos Manuel Fernández Andreu. (2022). Dermatofitosis: un desafío creciente de salud internacional. Revista Salud y Desarrollo, 6(1), p.149. https://doi.org/10.55717/JRZR1886.
Dimensions
PlumX
Visitas a la página del resumen del artículo
Descargas
Licencia
Derechos de autor 2016 Revista de la Facultad de Medicina

Esta obra está bajo una licencia Creative Commons Reconocimiento 3.0 Unported.
-





















