Synthesis of acyl-hydrazone from usnic acid and isoniazid and its anti-Mycobacterium tuberculosis activity
Síntesis de acil-hidrazona a partir del ácido úsnico e isoniazida y su actividad anti-Mycobacterium tuberculosis
DOI:
https://doi.org/10.15446/rev.colomb.quim.v46n3.61980Palabras clave:
Evernia prunastri, condensation reaction, TEMA, MIC. (en)Evernia prunastri, reacción de condensación, TEMA, MIC (es)
Descargas
Compound usnic acid (1), isolated from lichen Evernia prunastri (Cajamarca-Peru) and the synthesis and characterization of its acyl-hydrazone (2), from the condensation reaction between usnic acid and isoniazid in an ethanol solution under reflux, giving an overall yield of 95%, were evaluated. Both compounds were evaluated and compared with isoniazid according to its anti-Mycobacterium tuberculosis activity based on the tetrazolium microplate assay (TEMA). Compound 1 had MIC (minimal inhibitory concentration) value of 16.0 μg/mL in each test of H37Rv (susceptible type), TB DM 97 (resistant wild type) and MDR DM 1098 (multi drug resistances type) strains. In similar tests, compound 2 MIC values were 2.0, 64.0 and 64.0 μg/mL respectively.

Network of Scientific Journals from Latin America and the Caribbean, Spain and Portugal
Orgánica y Bioquímica
Synthesis of acyl-hydrazone from usnic acid and isoniazid and its anti-Mycobacterium tuberculosis activity
Síntesis de acil-hidrazona a partir del ácido úsnico e isoniazida y su actividad anti-Mycobacterium tuberculosis
Síntese de acilhidrazona a partir de ácido úsnico e isoniazida e sua atividade anti-Mycobacterium tuberculosis
Synthesis of acyl-hydrazone from usnic acid and isoniazid and its anti-Mycobacterium tuberculosis activity
Revista Colombiana de Química, vol. 46, no. 3, 2017
Universidad Nacional de Colombia
Received: 10 January 2017
Accepted: 29 March 2017
Abstract: Compound usnic acid (1), isolated from lichen Evernia prunastri (Cajamarca-Peru) and the synthesis and characterization of its acyl-hydrazone (2), from the condensation reaction between usnic acid and isoniazid in an ethanol solution under reflux, giving an overall yield of 95%, were evaluated. Both compounds were evaluated and compared with isoniazid according to its anti-Mycobacterium tuberculosis activity based on the tetrazolium microplate assay (TEMA). Compound 1 had MIC (minimal inhibitory concentration) value of 16.0 µg/mL in each test of H37Rv (susceptible type), TB DM 97 (resistant wild type) and MDR DM 1098 (multi drug resistances type) strains. In similar tests, compound 2 MIC values were 2.0, 64.0 and 64.0 µg/mL respectively.
Keywords: Evernia prunastri, condensation reaction, TEMA, MIC.
Resumen: Se evaluó el ácido úsnico (1), aislado del liquen Evernia prunastri (Cajamarca-Perú), producto natural conocido por sus actividades biológicas, y, del mismo modo, se evaluó la síntesis de su derivado acil-hidrazona (2), obtenido a partir de una reacción de condensación entre el ácido úsnico y la isoniazida en solución etanólica a reflujo, con un rendimiento global de 95%. Ambos compuestos fueron evaluados y comparados con la isoniazida según su actividad anti-Mycobacterium tuberculosis basada en el ensayo de susceptibilidad mediante el método TEMA. Los resultados mostraron que el compuesto 1 presenta valores de MIC de 16,0 µg/mL frente a las cepas H37Rv, TB DM 97 y MDR DM 1098, mientras que el compuesto 2 presenta valores de MIC de 2,0; 64,0 y 64,0 µg/mL respectivamente.
Palabras clave: Evernia prunastri, reacción de condensación, TEMA, MIC.
Resumo: Foi avaliado o ácido úsnico (1), um produto natural conhecido pelas suas atividades biológicas, isolado a partir do líquen Evernia prunastri (Cajamarca-Peru), assim mesmo foi avaliada a síntese do seu derivado, a acil-hidrazona (2), obtido a partir de uma reação de condensação com refluxo entre o ácido úsnico e a isoniazida em solução etanólica, com um rendimento global de 95%. A atividade anti-Mycobacterium tuberculosis de ambos compostos foi avaliada e comparada com a isoniazida mediante testes de sensibilidade obtidos pelo método TEMA. Os resultados mostraram que o composto 1 apresenta o valor de MIC de 16,0 µg/mL contra variedades H37Rv, TB DM 97 e MDR DM 1098; enquanto que para o composto 2 os valores de MIC são de 2,0; 64,0 e 64,0 µg/mL, respectivamente.
Palavras-chave: Evernia prunastri, reação de condensação, TEMA, MIC.
Introduction
Tuberculosis (TB), caused by the bacteria Mycobacterium tuberculosis, is a major public health problem that annually kills approximately 3 million people worldwide. It is worsened if there is co-infection with HIV ( 1 ). Approximately, one third of the world’s population is infected with latent TB ( 1 , 2 ). The therapy against tuberculosis is based on the use of combined drugs such as rifampicin, isoniazid (INH), and pyrazinamide, which are also employed as components of currently applied multidrug therapy of TB ( 3 ). Generally, MDR-TB includes the strains resistant to at least isoniazid and rifampin, considered as the more efficient first-line drugs against TB. The occurrence of mutations within several genes is responsible for the MDR-phenotype. For example, in the case of INH resistance, mutations within katG, inhA, ahpC, kasA, genes are involved ( 4 ).
Despite the global availability of drugs against tuberculosis, there are still some issues to address: the long duration of the treatment, the serious side effects, and the development of multidrug-resistant strains ( 5 , 6 ). This reveals the urgent need to identify novel, safe, and effective candidates for the determination of an optimized and efficient drug against the M. tuberculosis.
Over the last decade, there has been extensive research on antibacterial compounds from natural products, since they are considered to be the major source of active metabolites. These may provide lead structures for the development of new drugs ( 7 ), for example, usnic acid (UA) appears to be a promising medical application. Usnic acid is a yellowish, highly functionalized dibenzofuran metabolite found in various lichen genera distributed in species of Cladonia, Usnea, Lecanora, Ramalina, Evernia and Parmotrema. It can exist as (+) and (-) enantiomers, but most of its biological activity is attributed to the (+) enantiomer ( 8 , 9 ). Usnic acid displays a wide range of multiple biological effects, including: anti-bacterial, anti-parasitic, anti-viral, anti-mycotic, anti-protozoal, anti-proliferative, anti-inflammatory, anti-pyretic, and citotoxicity against human cancer cell lines ( 10 , 11 ).
Furthermore, earlier studies reveal that (+)-usnic acid exhibits activity against M. tuberculosis, showing a MIC value of 32 µg/mL, which was not considered potent enough ( 12 ). Considering the fact that the functional groups found within the molecule make of usnic acid a good target for structural modifications ( 2 ), a reaction between UA and INH was suggested in order to evaluate the enhancement or not of its activity against M. tuberculosis.
In this context, this research presents the synthesis and characterization of an acyl-hydrazone (2) [(R,E)-N'-(1-(6-acetyl-3,7,9-trihydroxy-8,9b-dimethyl-1-oxo-1,9b-dihydrodibenzo[b,d]furan-2-yl)ethylidene)isonicotinohydrazide], obtained from a condensation reaction between usnic acid (1) and isoniazid, and the study of its anti-mycobacterial activity into M. tuberculosis strains.
Materials and methods
In general, all solvents and reagents (Acros Organics or Sigma Aldrich) were used without prior purification. The isolation and purification were monitored by thin layer chromatography (TLC) on silica gel plate (Merck 60 F254), preparative chromatography (Merck 60 F254), and by column chromatography using silica gel (Gel 60 silica particle size 0.063-0.200 mm).
Compounds 1 and 2 were analyzed and characterized in CDCl3 and DMSO-d6, respectively, by 1H-NMR 300 MHz, 1H-NMR 600 MHz and 13C-NMR 150 MHz with a Varian Unity Inova AS600 spectrometer. The notations used for the spectral analysis are: s (singlet), d (doublet), m (multiplet). Chemical shifts are reported in δ (ppm) using tetramethylsilane (TMS) as the internal standard. The determination of the exact molecular weights was performed by high resolution mass spectrometry (HRMS) on an Agilent Technologies Model 6210 LC-MSD-TOF (Time-of-Flight mass spectrometer) instrument. The molecular ions were protonated [M+H]+ or [M-H]- for the confirmation of their empirical formula. Infrared spectra were recorded on a JASCO FT/IR-410 spectrophotometer. The optical rotation was measured using a JASCO P-1010 polarimeter.
The M. tuberculosis isolates: H37Rv, TB DM97, and MDR DM1098 were obtained from Cayetano Heredia University Hospital. Their suspensions were prepared in 10% (v/v) Tween 80 (Sigma Chemical Co., St. Louis, Mo.) so that their turbidities matched that of the McFarland Nº1 turbidity standard (approximately 3 x 107 CFU/mL). Therefore, suspensions were diluted 1:25 in 7H9 broth (4.7 g of Middlebrook 7H9 broth base [Difco, Detroit, Mich.], 20 mL of 10% glycerol, 1 g of Bacto Casitone [Difco], 880 mL of distilled water, 100 mL of oleic acid, albumin, dextrose, and catalase [Remel, Lenexa, Kans.]) ( 13 , 14 ).
Extraction, isolation, and elucidation of usnic acid
The branched thallus of Evernia prunastri were collected at Porcon farm, located 30 km from the city of Cajamarca-Peru and identified by Dr. Luis Dávila of National University of Cajamarca, Cajamarca, Peru.
The branched dried thallus of Evernia prunastri (100 g) was crushed into a powder and extracted with an increasing polarity order of solvents using hexane (72 h (3x)), ethyl ether (72 h (x2)), chloroform (72 h (2x)), ethyl acetate (72 h (x2)), methanol (72 h (3x)), and water (72 h (3x)) at room temperature. The ethyl ether extract (4.8 g) was separated using repeatedly flash column chromatography with hexane/ethyl acetate (7:3) and hexane/toluene/ethyl acetate (85:5:15), obtaining four fractions A, B, C and D. Fraction D was cooled at room temperature then filtered whereby a precipitate was obtained as a greenish yellow solid. This precipitate was separated out and recrystallized in ethanol 99% (v/v), from which the major compound was obtained as yellow crystals and identified as usnic acid (2.8 g), confirmed by 1H-NMR and 13C-NMR spectrums and by comparison with reported data ( 12 ).
Synthesis of acyl-hydrazone obtained from usnic acid and isoniazid
Usnic acid (500 mg, 1.45 mmol, 1 eq) and isoniazid (250 mg, 1.74 mmol, 1.2 eq) were added to a solution of 50 mL of absolute ethanol. The solution was stirred and heated at reflux for 12 h. The solution was cooled at room temperature and stored in a refrigerator for two days. The precipitate formed was filtered and dried in an oven at 25 °C for 24 h. The final product (acyl-hydrazone) was obtained as orange crystals ( 15 ).
Biological activity evaluation
The activity of usnic acid, isoniazid, and their acyl-hydrazone against susceptible (H37Rv), resistant wild type (DM 97) and multidrug resistance (DM 1098) M. tuberculosis strains were tested by tetrazolium microplate assay (TEMA), which uses tetrazoliumbromide [3-(4,5-dimethylthiazol-2-yl)-2,5diphenyl-tetrazolium bromide] (Aldrich Chemical Co., Milwaukee, Wis.) as a rapid, simple, and low-cost qualitative method to determine the antibiotic susceptibility ( 11 ). The assay was performed in duplicate (two plates). The procedure is described below ( 13 , 14 ).
Preparation of culture inoculum
Cultivation of M. tuberculosis was performed in Middlebrook 7H9 broth during four weeks. The inoculation of the strains was achieved by using a sterile loop into a glass bead tube with 100 μL of mix-Tween and mixed in a vortex for 2 min. Three mL of 10% (w/w) Tween 80 was added and stirred in a vortex for 20 s. The supernatant was transferred to a glass tube without beads. The turbidity was adjusted to McFarland Nº1 with a mix-Tween solution. The McFarland Nº1 strain was combined with Middlebrook 7H9 broth medium (12 mL of 7H9 + 0.5 mL of the strain) and diluted 1:25 in a Falcon tube.
Plate preparation and inoculation of drug and strain
Sterile water (200 μL) was added to all outer wells of sterile 96-well plates (Falcon 3072; Becton Dickinson, Lincoln Park, N.J.). Middlebrook 7H9 broth (100 μL) was added to the wells in rows B to G in columns 3 to 11 (labeled as commercially stamped on the plates). Drugs solutions (usnic acid, isoniazid and their acyl-hydrazone) (100 μL) were added to wells in columns 1 and 2; each two rows correspond to a different drug solution.
By using a multichannel pipette, 100 μL of solution was transferred from column 2 to column 3. The drug solutions were serially diluted 1:2 in consecutive columns through column 10, where 100 μL of excess medium was discarded. Final drug concentration ranges were 64 to 0.12 μg/mL. 100 μL of the diluted 1:25 strain was added to the wells in rows B to G in columns 1 to 11. The wells in column 11 served as inoculum-only controls. The plates were sealed with parafilm and then incubated at 37 °C for five days. Fifty microliters of a 1:1 mixture of the tetrazolium-Tween 80 mixture was added to well B11. The plates were reincubated at 37 °C for 12 h.
The following day, if well B11 turned purple, tetrazolium-Tween 80 was added to all wells and the color was recorded at 24 h. If well B11 remained yellow, the plates were incubated for another 24h, after which tetrazolium-Tween 80 solution was added to well C11 before the plate was incubated for another 24 h. If well C11 remained yellow, incubation was continued and tetrazolium-Tween 80 solution was added to wells D11, E11, F11, and G11 on days 9, 11, 13, and 15, respectively. A yellow color in the well was interpreted as no growth, and a purple color was scored as growth. The MIC was defined as the lowest drug concentration, which prevented a color change from yellow to purple.
Results and discussion
Extraction, isolation and elucidation of usnic acid
Usnic acid (2.8 g) was obtained as yellow crystals from dried thallus of lichen Evernia prunastri (100 g), using repeatedly flash column chromatography with hexane/ethyl acetate (7:3) and hexane/toluene/ethyl acetate (85:5:15). The IR spectrum showed bands at 2929 (CH-stretching), 1687 (elongation of the carbonyl group), 1628 (C=C, enol ether), 1540, 1455, 1421 cm-1 (aromatic ring). It should be mentioned that a wide band was present between 3500 and 2600 cm-1, due to the many hydrogen bonds present in the solid state.
The 1H-NMR spectrum shows characteristic signals at δ 13.31 and δ 11.02 ppm corresponding to the hydroxyl groups C8-OH and C10-OH respectively; δ 5.97 ppm corresponding to the H-4 from the double bond; finally δ 2.67, 2.66, 2.10; and 1.75 ppm corresponding to the methyl substituents. The hydroxyl group C3-OH appears at 18.84 ppm (Figure 1).
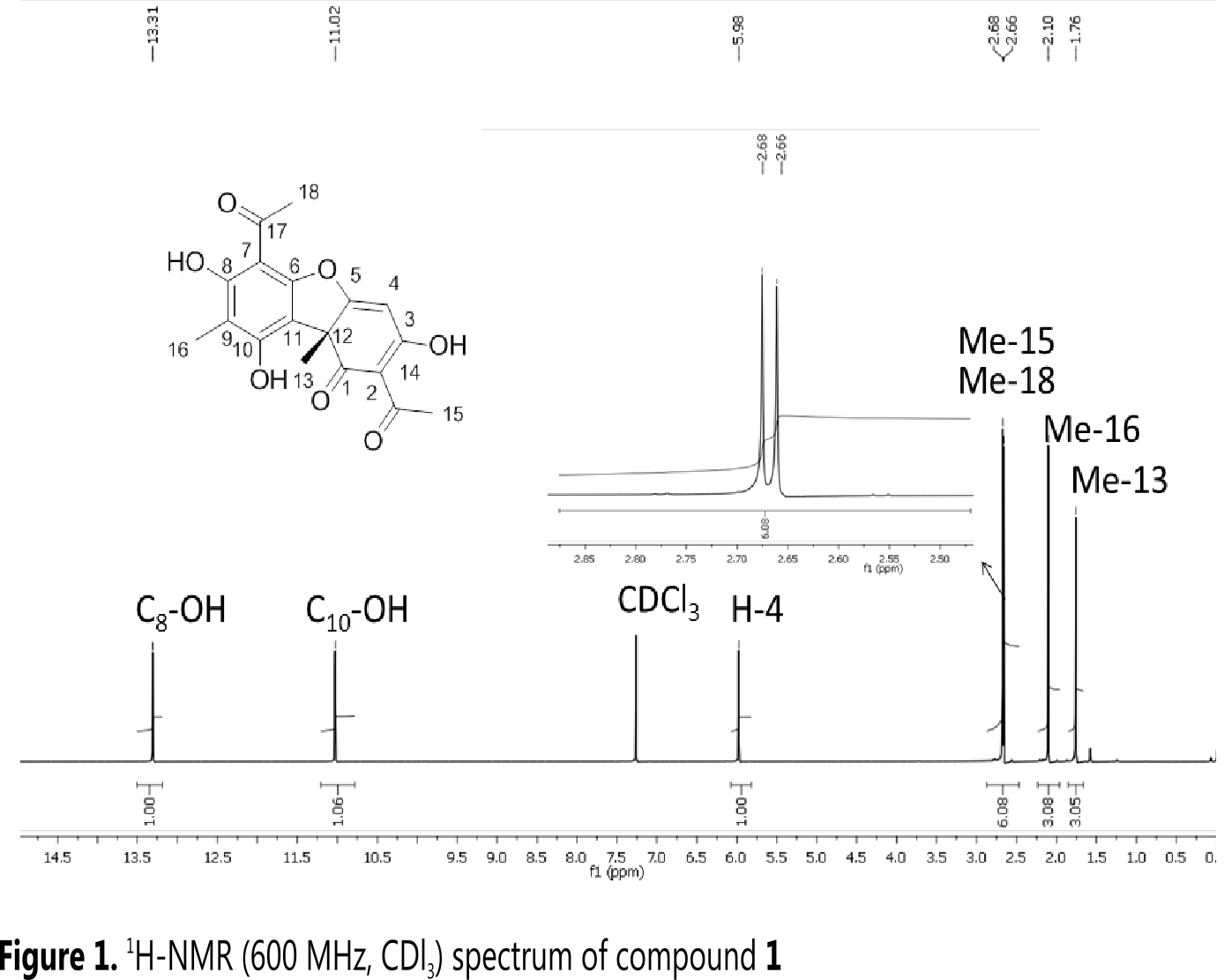
Usnic Acid: [α]D25 (c = 0.7, CHCl3) = +451. Rf = 0.32 (hexane/ethyle acetate 7:3). 1 H-NMR (600 MHz, CDCl3): δ = 13.31 (s, 1H, OH), 11.02 (s, 1H, OH), 5.97 (s, 1H, CCH), 2.67 (s, 3H, CH 3), 2.66 (s, 3H, CH 3), 2.10 (s, 3H, CH 3), 1.75 ppm (s, 3H,CH 3). 13C- NMR (75 MHz, CDCl3): δ = 201.9 (CO), 200.4 (CO), 198.2 (CO), 191.8 (COH), 179.5, 164.0, 157.6, 155.3, 109.4, 105.3, 104.1, 101.6, 98.5, 59.2 (C dibenzofuran), 32.3 (COCH3), 31.4 (COCH3), 28.1 (CH3), 7.7 ppm (CH3). ESI--HRMS: m/z calculated for C18H15O7 [M - H]-: 343.102; found: 343.100.
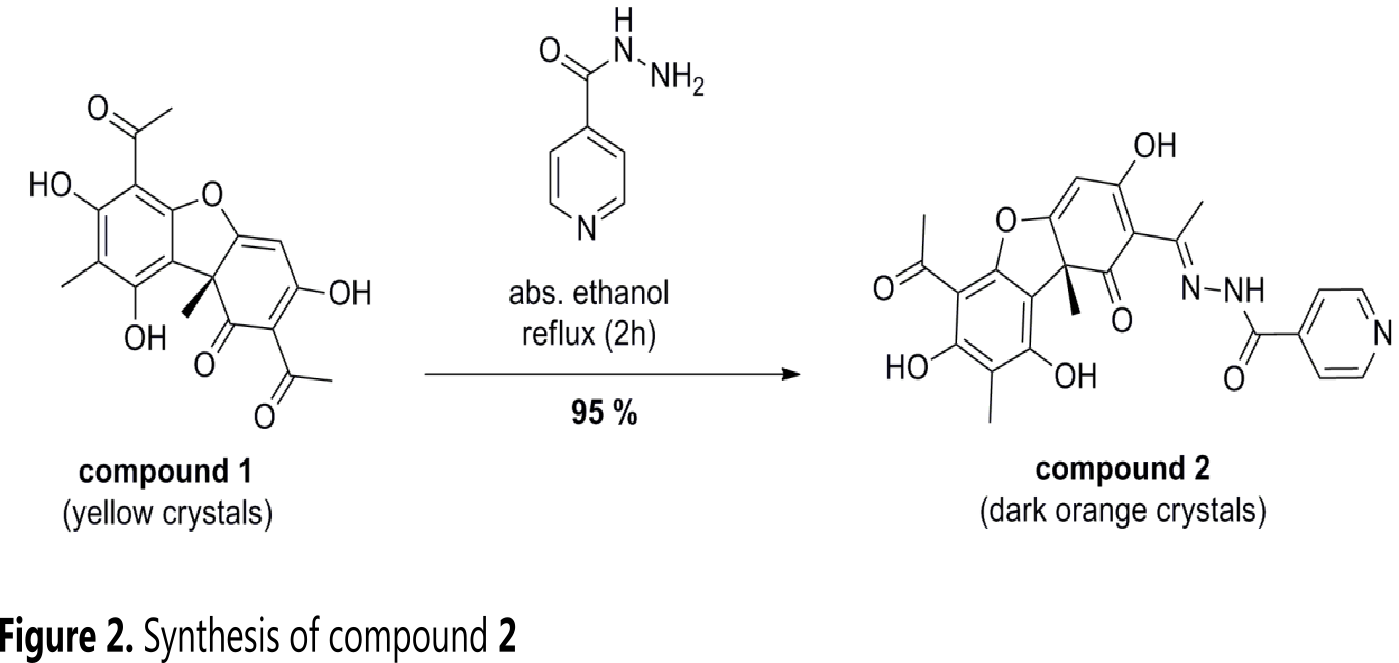
Synthesis of acyl-hydrazone obtained from usnic acid and isoniazid
The synthesis of the acyl-hydrazone was obtained with an overall yield of 95% (1.38 mmol) as orange crystals (Figure 2). The IR spectrum showed bands at 3415 (tension due to N-H), 2925 (CH-stretching), 1706 (tension due to carbonyl group), 1630 (C=N; C=C, enol ether, aromatic ring), 1549, 1362, 1220 cm-1. It should be noted that the NH group at 3415 cm-1 mask the signals of the OH groups present in the molecule.
The 1H-NMR spectrum shows characteristic signals of usnic acid and the corresponding signals of the protons belonging to the pyridine group, which appear upfield (Figure 3). The signals at δ 14.80, δ 13.40, and δ 12.13 ppm correspond to the hydroxyl groups C3-OH, C8-OH, and C10-OH respectively; δ 8.84 ppm, H-22, and H-23; δ 7.93 ppm, H-21 and H-24; δ 5.95 ppm, H-4; δ 3.45, NH. Signals at δ 2.71, 2.65, 1.98 and 1.69 ppm correspond to the methyl substituents.

The comparison of 1H-NMR spectrum of usnic acid and acyl-hydrazone revealed that the chemical shift of C3-OH is due to the presence of the imine group in the structure; the presence of this amine group also influences the electron density of the methyl group (Me-15), which appears shifted to downfield (δ 2.68 to δ 2.71).
Acyl-hydrazone: [α]D23 (c = 0.25, acetone) = +205,6. Rf = 0.35 (hexane/toluene/ ethyle acetate/methanol 4:1:5:1). 1H-NMR(600 MHz, DMSO-d6): δ = 14.80 (s, 1H, OH), 13.40 (s, 1H, OH), 12.13 (s, 1H, OH), 8.84 (m, 2H, 2CH), 7.93 (d, 2H, 2CH), 5.95 (s, 1H, CCH), 3.45 (m, 1H, NH), 2.71 (s, 3H, CH 3), 2.65 (s, 3H, CH 3), 1.98 (s, 3H,CH3), 1.69 ppm (s, 3H, CH 3). 13C-NMR (75 MHz, DMSO-d6): δ = 201.0 (CO), 197.5 (CO), 188.7 (COH), 173.6 (CO), 170.3 (CCO), 163.4 (CO), 157.7 (CO), 155.9 (CN), 149.4 (CN)pyr, 122.2 (CCN)pyr, 106.5 (CCC), 105.2 (CCC), 102.4 (CCHC), 101.0 (CCC), 100.9 ppm (CCC). ESI+-HRMS: m/z calculated for C24H22N3O7 [M + H]+: 464.1452; found: 464.1475.
Biological activity against M. tuberculosis
The activity of isoniazid, usnic acid, and their acyl-hydrazone against susceptible (H37Rv), resistant wild type (DM 97) and multidrug resistances (DM 1098) M. tuberculosis strains were evaluated (Figure 4). The tetrazolium microplate assay was performed in duplicate (two rows) based on the methodology already mentioned (see Materials and methods part). The MIC values obtained by compound 1 provide a better prospect to be potentially active compared to compound 2, the results are shown in Table 1.

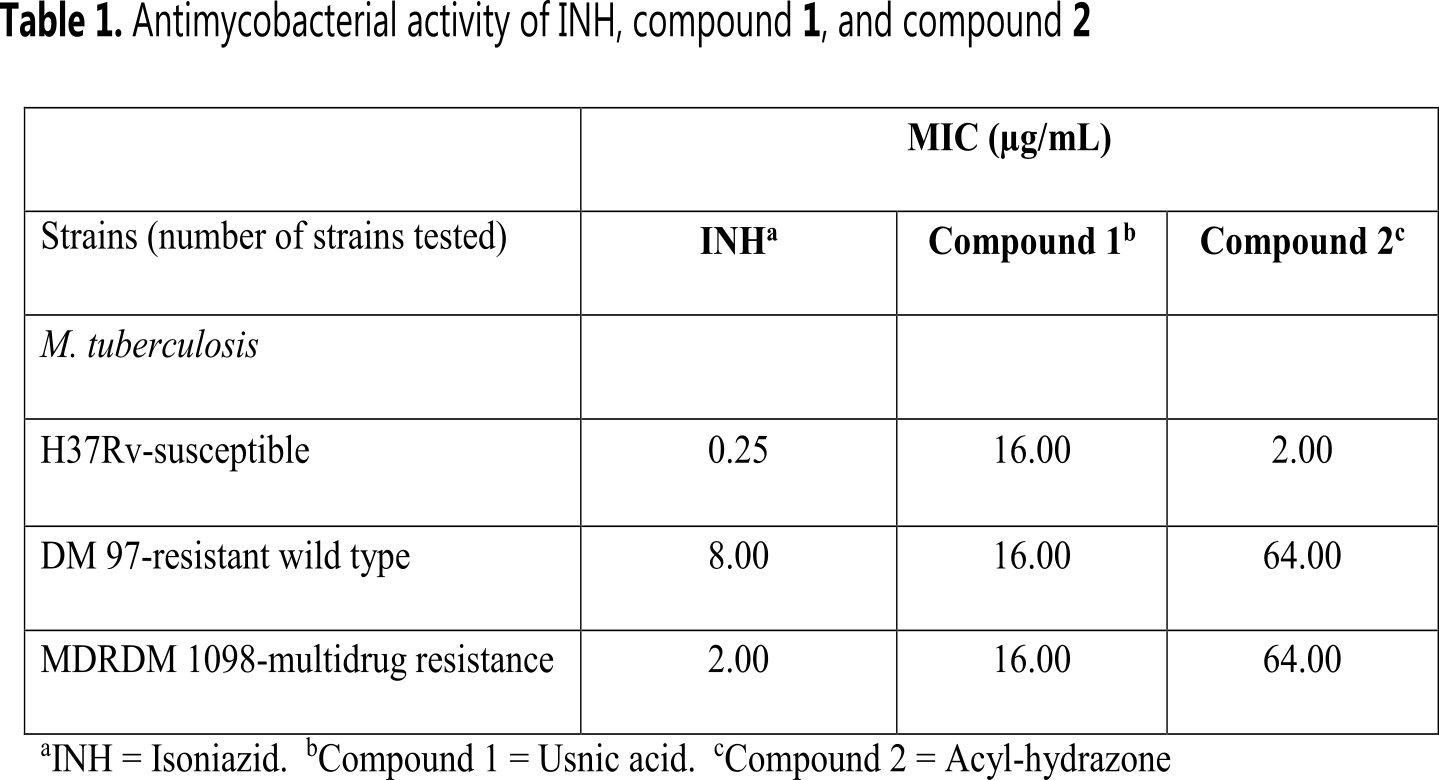
As it is shown in Table 1, acyl-hydrazone does not ameliorate the antimycobacterial activity of usnic acid for DM 97-resistant wild type, nor of H37Rv-susceptible strains, but, contrastingly, acyl-hydrazone showed an enhancement of its antimycobacterial activity, as compared to usnic acid on H37Rv-susceptible.
Conclusions
The synthesis of compound 2 (acyl-hydrazone) was achieved by a condensation reaction using commercial isoniazid and usnic acid, isolated from lichen Evernia prunastri, giving an overall yield of 95% (w/w). The isolation of usnic acid was performed using standard protocols of extractions and column chromatographic purifications. Their chemical structures were elucidated using 1D NMR spectroscopy and mass spectrometry, thus corroborating spectroscopic data reported in the literature ( 15 , 16 , 17 , 18 ).
According to the results obtained by TEMA method, usnic acid (1) exhibited MIC value of 16.0 μg/mL for each test of H37Rv, TB DM 97, and MDR DM 1098 strains. Instead, the corresponding acyl-hydrazone (2) exhibited MIC values of 2.0 μg/mL against H37Rv, and 64.0 μg/mL against resistant strain and multidrug resistance from M. tuberculosis.
The MIC values obtained by compound 1 provide a better prospect to be potentially active as compared to compound 2. However, both compounds exhibit less activity than isoniazid. Apparently, compound 2 does not meet initial expectations of increasing sensitivity on TB strains. However, these are preliminary in vitro results, and further in vivo studies should be carried out to confirm its antitubercular activity.
References
1. Sheen, P.; Lozano, K.; Gilman, R. H.; Valencia, H. J.; Loli, S.; Fuentes, P. et al. pncA gene expression and prediction factors on pyrazinamide resistance in Mycobacterium tuberculosis. Tuberculosis (Edinb). 2013, 93 (5), 515-522. DOI: https://doi.org/10.1016/j.tube.2013.03.005.
2. Bekker, O. B.; Sokolov, D. N.; Luzina, O. A.; Komarova, N. I.; Gatilov, Y. V.; Andreevskaya, S. N. Synthesis and activity of (+)-usnic acid and (−)-usnic acid derivatives containing 1,3-thiazole cycle against Mycobacterium tuberculosis. Med. Chem. Res. 2015, 24 (7), 2926-2938. DOI: https://doi.org/10.1007/s00044-015-1348-2.
3. Rodrigo, L.; Tozatti, M. G.; de Oliveira Salloum, A. I.; Crotti, A. E. M.; Silva, M. L. A.; Gimenez, V. M. M. et al. Antimycobacterial activity of Usnea steineri and its major constituent (+)-usnic acid. Afr. J. Biotechnol. 2012, 11 (20), 4636-4639. DOI: https://doi.org/10.5897/ajb11.3551.
4. Ali, I. F. A.; Babak, F.; Fazlollah, M. S.; Nematollah, J. J. Rapid detection of MDR-Mycobacterium tuberculosis using modified PCR-SSCP from clinical Specimens. Asian Pac. J. Trop. Biomed. 2014, 4 (1), 165-170. DOI: https://doi.org/10.12980/apjtb.4.2014c1186.
5. Solis, L.; Coronel, J.; Rueda, D.; Gilman, R. H.; Sheen, P.; Zimic, M. Evaluation of a lens-free imager to facilitate tuberculosis diagnostics in MODS. Tuberculosis (Edinb). 2016, 97, 26-32. DOI: https://doi.org/10.1016/j.tube.2015.12.001.
6. Horvati, K.; Bacsa, B.; Kiss, E.; Gyulai, G.; Fodor, K.; Balka, G. et al. Nanoparticle encapsulated lipopeptide conjugate of antitubercular drug isoniazid: in vitro intracellular activity and in vivo efficacy in a Guinea pig model of tuberculosis. Bioconjugate Chem. 2014, 25 (12), 2260-2268. DOI: https://doi.org/10.1021/bc500476x.
7. Luzina, O. A.; Sokolov, D. N.; Pokrovskii, M. A.; Pokrovskii, A. G.; Bekker, O. B.; Danilenko, V. N. et al. Synthesis and biological activity of usnic acid enamine derivatives. Chem. Nat. Compd. 2015, 51 (4), 646-651. DOI: https://doi.org/10.1007/s10600-015-1376-7
8. Segatore, B.; Bellio, P.; Setacci, D.; Brisdelli, F.; Piovano, M.; Garbarino, J. A. et al. In vitro interaction of usnic acid in combination with antimicrobial agents against methicillin-resistant Staphylococcus aureus clinical isolates determined by FICI and ΔE model methods. Phytomedicine. 2012, 19 (3-4), 341-347. DOI: https://doi.org/10.1016/j.phymed.2011.10.012.
9. Lira, M. C. B.; Ferraz, M. S.; Silva, D. G. V. C.; Cortes, M. E.; Teixeira, K. I.; Caetano, N. P. et al. Inclusion complex of usnic acid with β-cyclodextrin: characterization and nanoencapsulation into liposomes. J. Inclusion Phenom. and Macrocyclic Chem. 2009, 64 (3-4), 215-224. DOI: https://doi.org/10.1007/s10847-009-9554-5.
10. Backor, M.; Klemova, K.; Backorova, M.; Ivanova, V. Comparison of the phytotoxic effects of usnic acid on cultures of free-living alga Scenedesmus quadricauda and aposymbiotically grown lichen photobiont Trebouxia erici. J. Chem. Ecol. 2010, 36 (4), 405-411. DOI: https://doi.org/10.1007/s10886-010-9776-4.
11. Brisdelli, F.; Perilli, M.; Sellitri, D.; Piovano, M.; Garbarino, J. A.; Nicoletti, M. et al. Cytotoxic activity and antioxidant capacity of purified lichen metabolites: an in vitro study. Phytother. Res. 2013, 27 (3), 431-437. DOI: https://doi.org/10.1002/ptr.4739.
12. Ingólfsdóttir, K. Usnic Acid. Phytochemistry. 2002, 61, 729-736. DOI: https://doi.org/10.1016/s0031-9422(02)00383-7.
13. Franzblau, S. G.; Witzig, R. S.; McLaughlin, J. C.; Torres, P.; Madico, G.; Hernandez A. et al. Rapid, Low-Technology MIC Determination with Clinical Mycobacterium tuberculosis Isolates by Using the Microplate Alamar Blue Assay. J. Clin. Microbiol. 1998, 36 (2), 362-366.
14. Caviedes, L.; Delgado, J.; Gilman, R. H. Tetrazolium Microplate Assay as a Rapid and Inexpensive Colorimetric Method for Determination of Antibiotic Susceptibility of Mycobacterium tuberculosis. J. Clin. Microbiol. 2002, 40 (5), 1873-1874. DOI: https://doi.org/10.1128/jcm.40.5.1873-1874.2002.
15. Natic, M.; Tesic, Z.; Andelkovic, K.; Brceski, I.; Radulovic, S.; Manic, S. et al. Synthesis and Biological Activity of Pd (II) and Cu (II) Complexes with Acylhydrazones of Usnic Acid. Synth. React. Inorg. Met. -Org. Chem. 2004, 34 (1), 101-113. DOI: https://doi.org/10.1081/SIM-120027320.
16. Lane, C. A.; Green T. K. Usnic Acid and the Intramolecular Hydrogen Bond. A Computational Experiment for the Organic Laboratory. J. Chem. Educ. 2006, 83 (7), 1046. DOI: https://doi.org/10.1021/ed083p1046.
17. Castro, O. N. Aislamiento del ácido úsnico de Flavoparmelia caperata y su determinación cuantitativa por espectroscopía UV, en diez líquenes. Rev. Soc. Quím. 2010, 74 (4), 389-399.
18. Kutney, J. P.; Sanchez, I. H. Studies in the usnic acid series. I. The condensation of (+) - usnic acid with aliphatic and aromatic amines. Canadien J. Chem. 1976, 54 (17), 2795-2803. DOI: https://doi.org/10.1139/v76-395.
Author notes
barreratomasmelissa@gmail.com
Referencias
Sheen, P.; Lozano, K.; Gilman, R. H.; Valencia, H. J.; Loli, S.; Fuentes, P. et al. pncA gene expression and prediction factors on pyrazinamide resistance in Mycobacterium tuberculosis. Tuberculosis (Edinb). 2013, 93 (5), 515-522. DOI: https://doi.org/10.1016/j.tube.2013.03.005.
Bekker, O. B.; Sokolov, D. N.; Luzina, O. A.; Komarova, N. I.; Gatilov, Y. V.; Andreevskaya, S. N. Synthesis and activity of (+)-usnic acid and (−)-usnic acid derivatives containing 1,3-thiazole cycle against Mycobacterium tuberculosis. Med. Chem. Res. 2015, 24 (7), 2926-2938. DOI: https://doi.org/10.1007/s00044-015-1348-2.
Rodrigo, L.; Tozatti, M. G.; de Oliveira Salloum, A. I.; Crotti, A. E. M.; Silva, M. L. A.; Gimenez, V. M. M. et al. Antimycobacterial activity of Usnea steineri and its major constituent (+)-usnic acid. Afr. J. Biotechnol. 2012, 11 (20), 4636-4639. DOI: https://doi.org/10.5897/ajb11.3551.
Ali, I. F. A.; Babak, F.; Fazlollah, M. S.; Nematollah, J. J. Rapid detection of MDR-Mycobacterium tuberculosis using modified PCR-SSCP from clinical Specimens. Asian Pac. J. Trop. Biomed. 2014, 4 (1), 165-170. DOI: https://doi.org/10.12980/apjtb.4.2014c1186.
Solis, L.; Coronel, J.; Rueda, D.; Gilman, R. H.; Sheen, P.; Zimic, M. Evaluation of a lens-free imager to facilitate tuberculosis diagnostics in MODS. Tuberculosis (Edinb). 2016, 97, 26-32. DOI: https://doi.org/10.1016/j.tube.2015.12.001.
Horvati, K.; Bacsa, B.; Kiss, E.; Gyulai, G.; Fodor, K.; Balka, G. et al. Nanoparticle encapsulated lipopeptide conjugate of antitubercular drug isoniazid: in vitro intracellular activity and in vivo efficacy in a Guinea pig model of tuberculosis. Bioconjugate Chem. 2014, 25 (12), 2260-2268. DOI: https://doi.org/10.1021/bc500476x.
Luzina, O. A.; Sokolov, D. N.; Pokrovskii, M. A.; Pokrovskii, A. G.; Bekker, O. B.; Danilenko, V. N. et al. Synthesis and biological activity of usnic acid enamine derivatives. Chem. Nat.Compd. 2015, 51 (4), 646-651. DOI: https://doi.org/10.1007/s10600-015-1376-7
Segatore, B.; Bellio, P.; Setacci, D.; Brisdelli, F.; Piovano, M.; Garbarino, J. A. et al. In vitro interaction of usnic acid in combination with antimicrobial agents against methicillin-resistant Staphylococcus aureus clinical isolates determined by FICI and ΔE model methods. Phytomedicine. 2012, 19 (3-4), 341-347. DOI: https://doi.org/10.1016/j.phymed.2011.10.012.
Lira, M. C. B.; Ferraz, M. S.; Silva, D. G. V. C.; Cortes, M. E.; Teixeira, K. I.; Caetano, N. P. et al. Inclusion complex of usnic acid with β-cyclodextrin: characterization and nanoencapsulation into liposomes. J. Inclusion Phenom. and Macrocyclic Chem. 2009, 64 (3-4), 215-224. DOI: https://doi.org/10.1007/s10847-009-9554-5.
Backor, M.; Klemova, K.; Backorova, M.; Ivanova, V. Comparison of the phytotoxic effects of usnic acid on cultures of free-living alga Scenedesmus quadricauda and aposymbiotically grown lichen photobiont Trebouxia erici. J. Chem. Ecol. 2010, 36 (4), 405-411. DOI: https://doi.org/10.1007/s10886-010-9776-4.
Brisdelli, F.; Perilli, M.; Sellitri, D.; Piovano, M.; Garbarino, J. A.; Nicoletti, M. et al. Cytotoxic activity and antioxidant capacity of purified lichen metabolites: an in vitro study. Phytother. Res. 2013, 27 (3), 431-437. DOI: https://doi.org/10.1002/ptr.4739.
Ingólfsdóttir, K. Usnic Acid. Phytochemistry. 2002, 61, 729-736. DOI: https://doi.org/10.1016/s0031-9422(02)00383-7.
Franzblau, S. G.; Witzig, R. S.; McLaughlin, J. C.; Torres, P.; Madico, G.; Hernandez A. et al. Rapid, Low-Technology MIC Determination with Clinical Mycobacterium tuberculosis Isolates by Using the Microplate Alamar Blue Assay. J. Clin. Microbiol. 1998, 36 (2), 362-366.
Caviedes, L.; Delgado, J.; Gilman, R. H. Tetrazolium Microplate Assay as a Rapid and Inexpensive Colorimetric Method for Determination of Antibiotic Susceptibility of Mycobacterium tuberculosis. J. Clin. Microbiol. 2002, 40 (5), 1873-1874. DOI: https://doi.org/10.1128/jcm.40.5.1873-1874.2002.
Natic, M.; Tesic, Z.; Andelkovic, K.; Brceski, I.; Radulovic, S.; Manic, S. et al. Synthesis and Biological Activity of Pd (II) and Cu (II) Complexes with Acylhydrazones of Usnic Acid. Synth. React. Inorg. Met. -Org. Chem. 2004, 34 (1), 101-113. DOI: https://doi.org/10.1081/SIM-120027320.
Lane, C. A.; Green T. K. Usnic Acid and the Intramolecular Hydrogen Bond. A Computational Experiment for the Organic Laboratory. J. Chem. Educ. 2006, 83 (7), 1046. DOI: https://doi.org/10.1021/ed083p1046.
Castro, O. N. Aislamiento del ácido úsnico de Flavoparmelia caperata y su determinación cuantitativa por espectroscopía UV, en diez líquenes. Rev. Soc. Quím. 2010, 74 (4), 389-399.
Kutney, J. P.; Sanchez, I. H. Studies in the usnic acid series. I. The condensation of (+) - usnic acid with aliphatic and aromatic amines. Canadien J. Chem. 1976, 54 (17), 2795-2803. DOI: https://doi.org/10.1139/v76-395.
Cómo citar
IEEE
ACM
ACS
APA
ABNT
Chicago
Harvard
MLA
Turabian
Vancouver
Descargar cita
CrossRef Cited-by
1. L. Yabo-Dambagi, A. Cakir, A. Karaküçük-İyidoğan. (2024). Antidiabetic, Antidepressant, Antiparkinson’s, Neuroprotective, and Antioxidant Potentials of Novel Schiff Base Derivatives of a Lichen Metabolite, Usnic Acid. Russian Journal of Bioorganic Chemistry, 50(5), p.1863. https://doi.org/10.1134/S1068162024050078.
2. Ana Cecilia Valderrama Negrón, Rocio I. Ramirez Panti, Christian M. Aliaga Paucar, Fernando Grandez Arias, Patricia Sheen Cortovaria, Mirko Juan Zimic Peralta, Yudith Cauna Orocollo. (2022). Pyrazinamide–isoniazid hybrid: synthesis optimisation, characterisation, and antituberculous activity. Revista Colombiana de Química, 50(3), p.16. https://doi.org/10.15446/rev.colomb.quim.v50n3.96424.
3. Miah Roney, Gagandeep Singh, A. K. M. Moyeenul Huq, Md Shaekh Forid, Wan Maznah Binti Wan Ishak, Kamal Rullah, Mohd Fadhlizil Fasihi Mohd Aluwi, Saiful Nizam Tajuddin. (2024). Identification of Pyrazole Derivatives of Usnic Acid as Novel Inhibitor of SARS-CoV-2 Main Protease Through Virtual Screening Approaches. Molecular Biotechnology, 66(4), p.696. https://doi.org/10.1007/s12033-023-00667-5.
4. Daniela Cirillo, Emanuele Borroni, Irene Festoso, Diego Monti, Sergio Romeo, Dominique Mazier, Luisella Verotta. (2018). Synthesis and antimycobacterial activity of (+)‐usnic acid conjugates. Archiv der Pharmazie, 351(12) https://doi.org/10.1002/ardp.201800177.
5. Shasank S. Swain, Sudhir K. Paidesetty, Rabindra N. Padhy, Tahziba Hussain. (2020). Isoniazid–phytochemical conjugation: A new approach for potent and less toxic anti‐TB drug development. Chemical Biology & Drug Design, 96(2), p.714. https://doi.org/10.1111/cbdd.13685.
6. Fernando Carrasco, Wilfredo Hernández, Oscar Chupayo, Patricia Sheen, Mirko Zimic, Jorge Coronel, Celedonio M. Álvarez, Sergio Ferrero, Sandra Oramas-Royo, Evgenia Spodine, Jesus M. Rodilla, Juan Z. Dávalos, Marcelino Maneiro. (2021). Phenylisoxazole-3/5-Carbaldehyde Isonicotinylhydrazone Derivatives: Synthesis, Characterization, and Antitubercular Activity. Journal of Chemistry, 2021, p.1. https://doi.org/10.1155/2021/6014093.
7. Fernando Carrasco, Wilfredo Hernández, Juan Z. Dávalos, Jackeline Mosquera, Oscar Chupayo, Nelly Sivipaucar, Jaime Tamayo, Eduardo Carrasco-S, Jorge Coronel, Osvaldo Yañez, William Tiznado, Anjali Chauhan. (2026). Synthesis, Antitubercular Activity, and Computational Characterization of Novel Phenylpyrazole‐Isoniazid Derivatives. Advances in Pharmacological and Pharmaceutical Sciences, 2026(1) https://doi.org/10.1155/adpp/2155127.
8. Wen-Zhe Nie, Qing-Kun Shen, Zhe-Shan Quan, Hong-Yan Guo, Ya-Mei Li. (2024). Bioactivities and Structure-Activity Relationships of Usnic Acid Derivatives: A Review. Mini-Reviews in Medicinal Chemistry, 24(14), p.1368. https://doi.org/10.2174/0113895575277085231123165546.
9. María Cristina Martínez-Habibe, Pierine Espana-Puccini, Ricardo Miranda-González. (2025). Little Giants: Lichens in Tropical Dry Forests. Forests, 16(9), p.1364. https://doi.org/10.3390/f16091364.
Dimensions
PlumX
Visitas a la página del resumen del artículo
Descargas
Licencia
Derechos de autor 2017 Melissa Barrera Tomas, Gloria Eva Eva Tomas Chota, Patricia Sheen Cortavarría., Patricia Fuentes Bonilla, Miguel Angel Inocente Camones, Julio Cesar Santiago Contreras

Esta obra está bajo una licencia internacional Creative Commons Atribución 4.0.
Los autores/as conservarán sus derechos de autor y garantizarán a la revista el derecho de primera publicación de su obra, el cuál estará simultáneamente sujeto a la Licencia de reconocimiento de Creative Commons (CC. Atribución 4.0) que permite a terceros compartir la obra siempre que se indique su autor y su primera publicación en esta revista.
Los autores/as podrán adoptar otros acuerdos de licencia no exclusiva de distribución de la versión de la obra publicada (p. ej.: depositarla en un archivo telemático institucional o publicarla en un volumen monográfico) siempre que se indique la publicación inicial en esta revista.
Se permite y recomienda a los autores/as difundir su obra a través de Internet (p. ej.: en archivos telemáticos institucionales o en su página web) antes y durante el proceso de envío, lo cual puede producir intercambios interesantes y aumentar las citas de la obra publicada. (Véase El efecto del acceso abierto).













